Giải bài 4 tr 132 sách GK Hóa lớp 12
Có 28,1 gam hỗn hợp MgCO3 và BaCO3 trong đó MgCO3 chiếm a% khối lượng. Cho hỗn hợp trên tác dụng hết dụng với dung dịch axit HCl để lấy khí CO2 rồi đem sục vào dung dịch có chứa 0,2 mol Ca(OH)2 được kết tủa b. Tính a để kết B thu được là lớn nhất?
Hướng dẫn giải chi tiết bài 4
Nhận định & Phương pháp
Đây là dạng bài sục CO2 vào dung dịch bazơ kiềm/ kiềm thổ. Tùy theo tỉ lệ CO2 và kiềm/ kiềm thổ mà thu được muối CO32- hoặc muối HCO3- hoặc cả hai. Như vậy muốn thu được nhiều kết tủa nhất thì sản phẩm chỉ tạo CO32-
Các bước giải như sau:
- Bước 1: Viết các phương trình phản ứng hóa học
- Bước 2: Suy luận điều kiện để lượng kết tủa B thu được là lớn nhất
- Bước 3: Thiết lập phương trình theo ẩn a → Giá trị a.
Lời giải:
Các phương trình phản ứng xảy ra là:
MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
\(n_{CO_{2}}= n_{MgCO_{3}} + n_{BaCO_{3}} = 0,2 \ mol\)
Ta có:
\(\\ \frac{28,1.a}{100.84} + \frac{28,1. (100 - a)}{100.197} = 0,2 \\ \\ \Rightarrow a = 29,89\)
-- Mod Hóa Học 12 HỌC247
Video hướng dẫn giải bài 4 SGK
-


Cho m gam hỗn hợp Na và Al (tỉ lệ mol 1 : 1) vào H2O dư thu được X. Cho từ từ 200ml HCl 1M vào X thì thu được t gam kết tủa. Nếu cho từ từ 300ml HCl 1M vào dung dịch X thì thu được 1,25t gam kết tủa. Giá trị của m là?
bởi Mai Rừng
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Đá vôi sau một thời gian nung thì thu được chất rắn có khối lượng bằng 67% khối lượng miếng đá vôi ban đầu. Hiệu suất của phản ứng nhiệt phân là?
bởi Phí Phương
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


Chọn dãy kim loại tan trong nước nhiệt độ thường.
bởi Nguyễn Ngọc Sơn
 16/05/2022
16/05/2022
A. Na, Fe.
B. Mg, Zn.
C. K, Ba.
D. Cr, Ni.
Theo dõi (0) 1 Trả lời -


Nhóm những chất đều không có tính lưỡng tính:
bởi Thùy Trang
 15/05/2022
15/05/2022
A. Fe2O3, CaO.
B. Al2O3, Al(OH)3.
C. Cr2O3, Cr(OH)3.
D. NaHCO3, Ca(HCO3)2.
Theo dõi (0) 1 Trả lời -


Cho những ion Na+ (0,04 mol); Mg2+ (0,02 mol); Ca2+ (0,03 mol); Cl– (0,02 mol); HCO3– (0,1 mol) và SO42- (0,01 mol). Đun sôi cốc nước trên cho đến khi phản ứng xảy ra hoàn toàn thì nước còn lại trong cốc là?
bởi Minh Thắng
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho Na, K hòa tan hết vào nước được dung dịch A và 0,672 lít khí H2 (đktc). Thể tích HCl 0,2M cần để trung hòa hết một nửa dung dịch A là?
bởi nguyen bao anh
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -

 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Nung 31,8 gam X gồm 2 muối cacbonat hóa trị II (hóa trị không đổi) đến khối lượng không đổi, lại 16,4 gam chất rắn. Hấp thụ toàn bộ khối lượng khí CO2 sinh ra vào dung dịch Y chứa 0,1 mol Ba(OH)2 và 0,2 mol NaOH. Khối lượng kết tủa thu được sau phản ứng là?
bởi Hồng Hạnh
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


A. Fe, K, Ca.
B. Li, K, Cs.
C. Be, Na, Ca.
D. Zn, Na, Ba.
Theo dõi (0) 1 Trả lời -

 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Cho chất A gồm CaCO3 và CaSO3 tới phản ứng hoàn toàn được chất rắn B có khối lượng bằng 504% khối lượng A. A có % khối lượng hai chất lần lượt là?
bởi Nguyễn Minh Minh
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho CaCO3 → CaO → CaC2 → C2H2 → vinyl axetilen → CH2+CH-CH=CH2 → Cao su buna. Số phản ứng oxi hóa khử?
bởi Nhật Nam
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


250 ml X chứa Na2CO3 và NaHCO3 khi tác dụng H2SO4 dư cho ra 2,24 lít CO2 (Đktc). 500 ml X với CaCl2 dư cho ra 16 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong X lần lượt là?
bởi Mai Vi
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


Cho NH4NO3, NaHSO4, NH4HCO3, Al2(SO4)3. Số chất tác dụng dung dịch Ba(OH)2 dư thu được kết tủa ?
bởi Anh Nguyễn
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho A chứa 0,2 mol Na2CO3 và 0,3 mol NaHCO3. Chất B chứa 0,5 mol HCl. Tính thể tích khí CO2 (đktc) thu được khi cho từ từ đến hết dung dịch B vào dung dịch A? Giả sử các phản ứng là hoàn toàn.
bởi Nguyễn Minh Minh
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho HCl lần lượt vào các K2SO4, AgNO3, Ba(OH)2, NaHCO3, NaAlO2. Số trường hợp có phản ứng xảy ra ?
bởi Lê Minh Trí
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho Be; Na, K, Ba, Fe. Số kim loại tác dụng mạnh với nước ở nhiệt độ thường?
bởi Nguyễn Trà Giang
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho 4,48 lít khí CO2 (đktc) vào 750 ml Ba(OH)2 0,2M, thu được m gam kết tủa. Giá trị của m là?
bởi Thanh Nguyên
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


X là hỗn hợp kim loại Ba và Al. Hoà tan m gam X vào lượng de nước thu được 8,96 lít H2 (đktc). Cũng m gam X vào NaOH dư thì thu được 12,32 lít khí H2 (đktc). Giá trị m là?
bởi Tram Anh
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho a mol CO2 hấp thụ hết chứa b mol NaOH thu được dung dịch X. Cho BaCl2 dư vào dung dịch X thu được m(g) kết tủa. Nếu cho Ba(OH)2 dư vào X thu được m1(g) kết tủa (m khác m1). Tỉ số b/a có giá trị đúng là?
bởi Hữu Trí
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


A. Chất béo, protein và vinyclorua.
B. Etylaxetat, tinh bột và protein.
C. Chất béo, xenlulozo và tinh bột.
D. Chất béo, protein và etylclorua.
Theo dõi (0) 1 Trả lời -


Điều khẳng định dưới đây là đúng?
bởi Nguyễn Hiền
 15/05/2022
15/05/2022
A. Khả năng tan trong nước của các kim loại kiềm tăng dần từ Li đến Cs.
B. Các kim loại kiềm có tính dẫn nhiệt, dẫn điện và có ánh kim.
C. Trong không khí ở điều kiện thường, khả năng oxi hóa các kim loại kiềm giảm dần từ Li đến Cs.
D. Các kim loại kiềm tác dụng được với N2 ngay điều kiện thường.
Theo dõi (0) 1 Trả lời -


Cho phản ứng sau: (1) X + Na2CO3 + H2O → Na2SO4 + Y + Z (2) Y + Na[Al(OH)4] → Z + NaHCO3
bởi Mai Thuy
 16/05/2022
16/05/2022
Biết rằng khi cho X vào dung dịch BaCl2 không thấy phản ứng hóa học xảy ra. Các chất X, Y, Z lần lượt là?
Theo dõi (0) 1 Trả lời -


Cho 11,2 gam CaO vào H2O dư thu được X. Sục từ từ khí CO2 vào dung dịch X, qua quá trình khảo sát người ta lập đồ thị như sau:
bởi Lam Van
 15/05/2022
15/05/2022
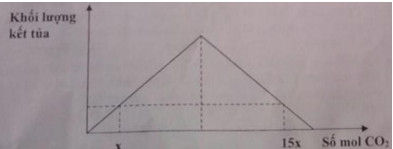
Giá trị của X là?
Theo dõi (0) 1 Trả lời -


A. Giấm ăn.
B. Phèn chua.
C. Muối ăn.
D. Nước vôi.
Theo dõi (0) 1 Trả lời -


Dùng 13,7 gam Ba vào 100ml HCl 1M thu được X. Rồi cho X vào 100ml dung dịch FeSO4 0,7M thu được kết tủa Y. Tính khối lượng kết tủa Y?
bởi Nguyễn Thị Thu Huệ
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho 2 lít KOH có pH = 13 vào 3 lít dung dịch HCl có pH = 2 được dung dịch Y. Giá trị pH của dung dịch Y là?
bởi Ha Ku
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


Khi cho Na vào dung dịch HCl thì điều gì diễn ra?
bởi Vũ Hải Yến
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho NaHCO3, CO, Al(OH)3, HF, SiO2, Cl2, NH4Cl. Số chất tác dụng với NaOH loãng ở nhiệt độ thường là?
bởi Lê Bảo An
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Trong CN, NaOH được sản xuất bằng phương pháp?
bởi Bảo khanh
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


Cho đá vôi có 80% CaCO3, 10,2% Al2O3 và 9,8% Fe2O3 về khối lượng. Nung đá ở nhiệt độ cao ta thu được chất rắn có khối lượng bằng 73,6% khối lượng đá trước khi nung. Hiệu suất của quá trình phân hủy CaCO3 là?
bởi Nguyễn Lê Thảo Trang
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho A chứa cation gồm Mg2+, Ba2+, Ca2+ và các anion gồm Cl– và NO3–. Thêm từ từ Na2CO3 1M vào A cho tới khi lượng kết tủa được lớn nhất thì dừng lại, lúc này người đo được lượng dung dịch Na2CO3 đã dùng là 250ml. Tổng số mol các anion có trong A ?
bởi Tieu Dong
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho 7,84 lít CO2 (đktc) vào 200ml gồm NaOH 1M và KOH xM. Sau phản ứng làm bay hơi nước của dung dịch thu được 37,5 gam chất rắn. Xác định x?
bởi Vương Anh Tú
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho 17,88g hỗn hợp gồm 2 kim loại kiềm A, B và kim loại kiềm thổ M vào nước thu được dd Y và 0,24 mol khí H2. Dung dịch Z gồm H2SO4 và HCl, trong đó số mol HCl gấp 4 lần số mol H2SO4. Để trung hòa \(\frac{1}{2}\) Y cần hết V lít dung dịch Z. Tổng khối lượng muối khan là bao nhiêu?
bởi Nguyễn Trà Giang
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


X là hợp chất C7H8O2. X tác dụng với Na dư cho số mol H2 bay ra bằng số mol NaOH cần dùng để trung hòa cùng lượng X trên. Chỉ ra công thức cấu tạo thu gọn của X.
bởi Thanh Nguyên
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


A. NH3, O2, N2, CH4, H2.
B. NH3, SO2, CO, Cl2.
C. N2, NO2, CO2, CH4, H2.
D. N2, Cl2, O2, CO2, H2.
Theo dõi (0) 1 Trả lời -


Cho NaHCO3, NaHSO4, AlCl3, Na3PO4, AgNO3, HNO3. Chất tác dụng được nhiều chất nhất trong số các chất cho ở trên?
bởi Lê Gia Bảo
 16/05/2022
16/05/2022
A. HCl.
B. BaCl2.
C. H2SO4.
D. NaOH.
Theo dõi (0) 1 Trả lời -

 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Dùng NaOH dư cho vào 100 ml chứa đồng thời Ba(HCO3)2 0,5 M và BaCl2 0,4 M. Khối lượng kết tủa thu được là?
bởi Khánh An
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Dùng m gam X gồm Ba, BaO, Al vào nước dư phản ứng kết thúc được Y; 3,024 lít khí (đktc) và 0,54 gam chất rắn không tan. Rót 110 ml HCl 1M vào dung dịch Y được 5,46 gam kết tủa. Giá trị của m là mấy?
bởi thu hảo
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Cho m gam gồm Na, Na2O, NaOH, Na2CO3 trong dung dịch axit H2SO4 40% (vừa đủ) thu được 8,96 lít hỗn hợp khí có tỉ khối đối với H2 bằng 16,75 và dung dịch Y có nồng độ 51,449%. Cô cạn Y thu được 170,4 gam muối. Giá trị của m là?
bởi Lê Tường Vy
 16/05/2022
Theo dõi (0) 1 Trả lời
16/05/2022
Theo dõi (0) 1 Trả lời -


Trong CN thì người ta điều chế nước giaven bằng cách:
bởi Bao Nhi
 15/05/2022
15/05/2022
A. Cho khí Cl2 đi từ từ qua dung dịch NaOH, Na2CO3.
B. Sục khí Cl2 vào dung dịch KOH.
C. Cho khí Cl2 vào dung dịch Na2CO3.
D. Điện phân dung dịch NaCl không màng ngăn.
Theo dõi (0) 1 Trả lời -


Chất gồm Ca(HCO3)2 , NaOH, Ca(OH)2 có tỉ lệ số mol tương ứng là 2 : 1 : 1. Khuấy kỹ hỗn hợp vào H2O dư. Dung dịch thu được có chứa những gì?
bởi Trần Thị Trang
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


A. Giấm ăn.
B. Muối ăn.
C. Phèn chua.
D. Nước vôi.
Theo dõi (0) 1 Trả lời -


Cho 2,45 gam X gồm 2 kim loại kiềm thổ vào 200 ml HCl 1,25M, thu được Y chứa các chất tan có nồng độ mol bằng nhau. Hai kim loại trong X là?
bởi thu phương
 15/05/2022
Theo dõi (0) 1 Trả lời
15/05/2022
Theo dõi (0) 1 Trả lời -


Kim loại tan hết trong \(H_2O\) dư ở nhiệt độ thường?
bởi Hương Lan
 16/05/2022
16/05/2022
A. Al.
B. Zn.
C. Mg.
D. K.
Theo dõi (0) 1 Trả lời -


Kim loại tan hết trong \(H_2O\) dư ở nhiệt độ thường?
bởi Hương Lan
 16/05/2022
16/05/2022
A. Al.
B. Zn.
C. Mg.
D. K.
Theo dõi (0) 1 Trả lời
Bài tập SGK khác
Bài tập 2 trang 132 SGK Hóa học 12
Bài tập 3 trang 132 SGK Hóa học 12
Bài tập 5 trang 132 SGK Hóa học 12
Bài tập 6 trang 132 SGK Hóa học 12
Bài tập 1 trang 170 SGK Hóa 12 Nâng cao
Bài tập 2 trang 170 SGK Hóa 12 Nâng cao
Bài tập 3 trang 170 SGK Hóa 12 Nâng cao
Bài tập 28.1 trang 65 SBT Hóa học 12
Bài tập 28.2 trang 65 SBT Hóa học 12
Bài tập 28.3 trang 66 SBT Hóa học 12
Bài tập 28.4 trang 66 SBT Hóa học 12
Bài tập 28.5 trang 66 SBT Hóa học 12
Bài tập 28.6 trang 66 SBT Hóa học 12
Bài tập 28.7 trang 66 SBT Hóa học 12
Bài tập 28.8 trang 66 SBT Hóa học 12
Bài tập 28.9 trang 67SBT Hóa học 12
Bài tập 28.10 trang 67 SBT Hóa học 12
Bài tập 28.11 trang 67 SBT Hóa học 12
Bài tập 28.12 trang 67 SBT Hóa học 12
Bài tập 28.13 trang 67 SBT Hóa học 12
Bài tập 28.14 trang 67 SBT Hóa học 12
Bài tập 28.15 trang 67 SBT Hóa học 12




