Hướng dẫn giải bài tập SGK Hoá học 12 Bài 29 Luyện tập Tính chất của nhôm và hợp chất của nhôm giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức môn hoá.
-
Bài tập 1 trang 134 SGK Hóa học 12
Nhôm bền trong môi trường không khí và nước là do:
A. Nhôm là kim loại kém hoạt động.
B. Có màng oxit Al2O3 bền vững bảo vệ.
C. Có màng hiđroxit Al(OH)3 bền vững bảo vệ.
D. Nhôm có tính thụ động với không khí và nước.
-
Bài tập 2 trang 134 SGK Hóa học 12
Nhôm không tan trong dung dịch nào sau đây?
A. HCl
B. H2SO4
C. NaHSO4
D. NH3
-
Bài tập 3 trang 134 SGK Hóa học 12
Cho 31,2 gam hỗn hợp bột Al và Al2O3 tác dụng hết với dung dịch NaOH dư thu được 13,44 lít H2 ở đktc. Khối lượng từng chất trong hỗn hợp ban đầu lần lượt là:
A.16,2 gam và 15 gam.
B. 10,8 gam và 20,4 gam.
C. 6,4 gam và 24,8 gam.
D. 11,2 gam và 20 gam.
-
Bài tập 4 trang 134 SGK Hóa học 12
Chỉ dùng thêm 1 hóa chất, hãy phân biệt các chất trong những dãy sau và viết phương trình hóa học để giải thích?
a) Các kim loại: Al, Ca, Na.
b) Các dung dịch: NaCl, CaCl2, AlCl3.
c) Các chất bột: CaO, MgO, Al2O3
-
Bài tập 5 trang 134 SGK Hóa học 12
Viết phương trình hóa học để giải thích các hiện tượng xảy ra khi chất nào tan là Al2O3; không tan là MgO.
a) Cho dung dịch NH3 dư vào dung dịch AlCl3.
b) Cho từ từ dung dịch NaOH đến dư vào dung dịch AlCl3.
c) Cho từ từ dung dịch Al2(SO4)3 vào dung dịch NaOH và ngược lại.
d) Sục từ từ đến dư khi CO2 vào dung dịch NaAlO2.
e) Cho từ từ đến dư dung dịch HCl vào dung dịch NaAlO2.
-
Bài tập 6 trang 134 SGK Hóa học 12
Hỗn hợp khí X gồm hai kim loại K và Al có khối lượng 10,5 gam. Hòa tan hoàn toàn hỗn hợp X trong nước được dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A: Lúc đầu không có kết tủa, khi thêm được 100 ml dung dịch HCl 1M thì bắt đầu có kết tủa. Tính thành phần % số mol của các kim loại trong X.
-
Bài tập 1 trang 183 SGK Hóa học 12 nâng cao
Biến đổi hóa học nào là do Al(OH)3 có tính axit?
A. Al(OH)3 (r) → Al3+(dd)
B. Al(OH)3 (r) → Al2O3(r)
C. Al(OH)3 (r) → [AL(OH)4]- (dd)
D. Al(OH)3 (r) → Al2O3(r)→ Al(r)
-
Bài tập 2 trang 183 SGK Hóa 12 Nâng cao
Hòa tan hoàn toàn 10g hỗn hợp gồm Al và Al2O3 trong dung dịch NaOH dư thu được 6,72 lit H2 (dktc). Phần trăm khối lượng Al trong hỗn hợp là:
A. 48%
B. 50%
C. 52%
D. 54%
-
Bài tập 3 trang 183 SGK Hóa 12 Nâng cao
Hãy tự chọn hai hóa chất dùng làm thuốc thử nhận biết mỗi kim loại sau: Al, Ag, Mg. Trình bày cách tiến hành thí nghiệm và viết các phương trình hóa học.
-
Bài tập 4 trang 183 SGK Hóa học 12 nâng cao
Hãy cho biết:
a. Cấu hình electron của các nguyên tử Na, Ca, Al và của các ion Na3+, Ca2+, Al3+.
b. Tính chất hóa học chung của các kim loại này.
c. Tính chất hóa học chung của những ion kim loại này.
-
Bài tập 5 trang 183 SGK Hóa 12 Nâng cao
Dùng những thuốc thử nào có thể phân biệt được các chất trong mỗi dãy sau?
a. Các kim loại: Al, Mg, Ca, Na
b. Các dung dịch muối: NaCl, CaCl2, AlCl3
c. Các oxit: CaO, MgO, Al2O3
d. Các hidroxit: NaOH, Ca(OH)2, Al(OH)3
-
Bài tập 6 trang 183 SGK nâng cao Hóa học 12
Tìm công thức hóa học dạng phân tử và dạng chất kép của những chất có thành phần như sau:
a. Hợp chất A: 32,9% Na; 12,9% Al; 54,2% F;
b. Hợp chất B: 14% K; 9,7% Al; 30,5% Si; 45,8% O.
-
Bài tập 7 trang 183 SGK Hóa 12 Nâng cao
Có 4 lọ riêng biệt đựng các dung dịch: NaCl, CuSO4, HCl, NaOH
a. Trình bày cách nhận biết từng chất trogn mỗi lọ trên, với điều kiện không dùng thêm thuốc thử nào khác.
b. Hãy chọn một thuốc thử để sự nhận biết các chất trở nên đơn giản hơn. Trình bày cách nhận biết và viết phương trình phản ứng hóa học.
-
Bài tập 29.1 trang 68 SBT Hóa học 12
Phát biểu nào sau đây đúng khi nói về nhôm oxit ?
A. Al2O3 được sinh ra khi nhiệt phân muối Al(NO3)3.
B. Al2O3 bị khử bởi co ở nhiệt độ cao.
C. Al2O3 tan được trong dung dịch NH3.
D. Al2O3 là oxit không tạo muối.
-
Bài tập 29.2 trang 68 SBT Hóa học 12
Có các dung dịch: KNO3, Cu(NO3)2, FeCl3, AlCl3, NH4Cl. Chỉ dùng hoá chất nào sau đây có thể nhận biết được các dung dịch trên ?
A. Dung dịch NaOH dư.
B. Dung dịch AgNO3.
C. Dung dịch Na2SO4.
D. Dung dịch HCl.
-
Bài tập 29.3 trang 68 SBT Hóa học 12
Cho m gam bột Al tác dụng hết với dung dịch HNO3 dư chỉ thu được 8,96 lít hỗn hợp khí X gồm NO và N2O (đktc) có tỉ lệ mol là 1 : 3. Giá trị của m là
A. 24,3.
B. 42,3.
C. 25,3.
D. 25,7.
-
Bài tập 29.4 trang 68 SBT Hóa học 12
Trộn 24g Fe2O3 với 10,8g Al rồi nung ở nhiệt độ cao (không có không khí). Hỗn hợp thu được sau phản ứng đem hoà tan vào dung dịch NaOH dư thu được 5,376 lít khí (đktc). Hiệu suất của phản ứng nhiệt nhôm là
A. 12,5%.
B. 60%.
C. 80%.
D. 90%.
-
Bài tập 29.5 trang 69 SBT Hóa học 12
Cho nhôm tác dụng với dung dịch chứa NaN03 và NaOH thấy nhôm tan và giải phóng NH3. Trong phương trình hoá học của phản ứng trên hệ số nguyên tối giản của H2O bằng
A. 3.
B. 2.
C. 5.
D. 7.
-
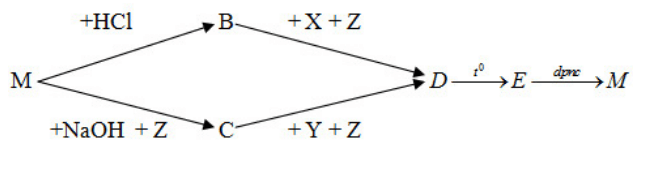
Bài tập 29.6 trang 69 SBT Hóa học 12
Xác định những chất cần lấy cho sơ đồ phản ứng sau :
-
Bài tập 29.7 trang 69 SBT Hóa học 12
Có các chất : NH3, CO2, HCl, KOH, Na2CO3. Có thể dùng những chất nào để kết tủa Al(OH)3 từ dung dịch :
a) Nhôm clorua ?
b) Natri aluminat ?
-
Bài tập 29.8 trang 69 SBT Hóa học 12
Từ Al2O3 và các dung dịch KOH, H2SO4, viết phương trình hoá học của các phản ứng dùng để điều chế phèn chua.
-
Bài tập 29.9 trang 69 SBT Hóa học 12
Dựa trên cơ sở hoá học nào để điéu chế nhôm oxit từ quặng boxit ? Viết phương trình hoá học của các phản ứng xảy ra.
-
Bài tập 29.10 trang 69 SBT Hóa học 12
Criolit được điều chế theo phản ứng sau:
Al2O3 (rắn) + HF (dd) + NaOH (dd) → Na3AlF6 (rắn) + H2O
Tính khối lượng mỗi chất ban đầu để sản xuất 1 kg criolit. Coi hiệu suất phản ứng đạt 100%.
-
Bài tập 29.11 trang 70 SBT Hóa học 12
Cho 2,16 gam Al vào dung dịch HNO3 loãng, lạnh (vừa đủ) thì thu được dung dịch X và không thấy khí thoát ra. Thêm dung dịch NaOH vào dung dịch X đến khi kết tủa tạo ra rồi vừa tan hết. Tính số mol NaOH đã dùng.
-
Bài tập 29.12 trang 70 SBT Hóa học 12
Lấy 26,8 gam hỗn hợp bột X gồm Al và Fe2O3, tiến hành phản ứng nhiệt nhôm cho tới khi phản ứng xảy ra hoàn toàn (giả sử chỉ xảy ra phản ứng khử Fe2O3 thành Fe). Hỗn hợp sản phẩm sau phản ứng cho tác dụng với lượng dư dung dịch HCl được 11,2 lít H2 (đktc). Xác định khối lượng của Al trong hỗn hợp bột X.
-
Bài tập 29.13 trang 70 SBT Hóa học 12
Nung 9,66 gam hỗn hợp bột X gồm Al và một oxit sắt trong điều kiện không có không khí, khi phản ứng nhiệt nhôm xảy ra hoàn toàn (giả sử chí xảy ra phản ứng khử oxit sắt thành sắt) thu được hỗn hợp sản phẩm Y. Chia Y làm 2 phần đều nhau :
- Phần 1 : Cho tác dụng với dung dịch NaOH dư thấy thoát ra 0,336 lít H2 (đktc).
- Phần 2 : Cho tác dụng với dung dịch HCl dư được 1,344 lít H2 (đktc).
Xác định công thức oxit sắt trong hỗn hợp bột X.
-
Bài tập 29.14 trang 70 SBT Hóa học 12
Cho 18 gam hỗn hợp bột Al, Al2O3 và một kim loại R hoá trị II không đổi.
- Nếu cho hỗn hợp tác dụng với dung dịch H2SO4 loãng (dư) thấy thoát ra 8,96 lít H2 (đktc).
- Nếu cho hỗn hợp tác dụng với dung dịch NaOH 2M thấy thoát ra 6,72 lít H2 (đktc) và lượng NaOH tối đa cho phản ứng là 200 ml, ngoài ra còn một phần chất rắn không tan.
Xác định kim loại R và phần trăm khối lượng Al2O3 trong hỗn hợp.