Nß╗Öi dung b├Āi hß╗Źc Amoniac v├Ā muß╗æi amoni t├¼m hiß╗āu vß╗ü cß║źu tß║Īo ph├ón tß╗Ł, t├Łnh chß║źt vß║Łt l├Ł (t├Łnh tan, tß╗ē khß╗æi, m├Āu, m├╣i), ß╗®ng dß╗źng ch├Łnh, amoniac trong ph├▓ng th├Ł nghiß╗ćm v├Ā trong c├┤ng nghiß╗ćp . T├Łnh chß║źt ho├Ī hß╗Źc cß╗¦a amoniac: T├Łnh bazŲĪ yß║┐u (t├Īc dß╗źng vß╗øi nŲ░ß╗øc, dung dß╗ŗch muß╗æi, axit) v├Ā t├Łnh khß╗Ł (t├Īc dß╗źng vß╗øi oxi, clo). C├Īch ─æiß╗üu chß║┐ NH3. T├Łnh chß║źt vß║Łt l├Ł (trß║Īng th├Īi, m├Āu sß║»c, t├Łnh tan). T├Łnh chß║źt ho├Ī hß╗Źc (phß║Żn ß╗®ng vß╗øi dung dß╗ŗch kiß╗üm, phß║Żn ß╗®ng nhiß╗ćt ph├ón) v├Ā ß╗®ng dß╗źng cß╗¦a muß╗æi amoni.
T├│m tß║»t l├Į thuyß║┐t
1.1. AMONIAC
1.1.1. Cß║źu tß║Īo ph├ón tß╗Ł
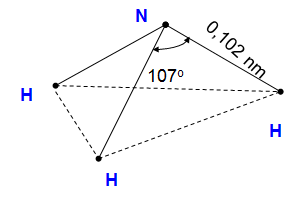
H├¼nh 1: SŲĪ ─æß╗ō cß║źu tß║Īo cß╗¦a ph├ón tß╗Ł NH3
- Nguy├¬n tß╗Ł N li├¬n kß║┐t vß╗øi 3 nguy├¬n tß╗Ł H bß║▒ng 3 li├¬n kß║┐t cß╗Öng h├│a trß╗ŗ c├│ cß╗▒c.
- Nguy├¬n tß╗Ł N c├▓n c├│ 1 cß║Ęp e ho├Ī trß╗ŗ.
- Nguy├¬n tß╗Ł N c├│ sß╗æ oxi h├│a thß║źp nhß║źt -3
- Ph├ón tß╗Ł c├│ cß║źu tß║Īo kh├┤ng ─æß╗æi xß╗®ng n├¬n ph├ón tß╗Ł NH3 ph├ón cß╗▒c.
1.1.2. T├Łnh chß║źt vß║Łt l├Į
- L├Ā chß║źt kh├Ł kh├┤ng m├Āu, m├╣i khai, xß╗æc, nhß║╣ hŲĪn kh├┤ng kh├Ł
- Tan nhiß╗üu trong nŲ░ß╗øc, tß║Īo th├Ānh dd c├│ t├Łnh kiß╗üm
Video 1: Sß╗▒ h├▓a tan cß╗¦a Amoniac trong nŲ░ß╗øc
- Kh├Ł NH3 tan nhiß╗üu trong nŲ░ß╗øc l├Ām giß║Żm P trong b├¼nh v├Ā nŲ░ß╗øc bß╗ŗ h├║t v├Āo b├¼nh. Phenolphtalein chuyß╗ān th├Ānh m├Āu hß╗ōng ŌćÆ NH3 c├│ t├Łnh bazŲĪ.
-
Dung dß╗ŗch NH3 ─æß║Łm ─æß║Ęc trong ph├▓ng th├Ł nghiß╗ćm c├│ nß╗ōng ─æß╗Ö 25% (N = 0,91g/cm3).
1.1.3. T├Łnh chß║źt h├│a hß╗Źc
T├Łnh bazŲĪ yß║┐u
T├Īc dß╗źng vß╗øi nŲ░ß╗øc
- Khi ho├Ā tan kh├Ł NH3 v├Āo nŲ░ß╗øc, 1 phß║¦n c├Īc ph├ón tß╗Ł NH3 phß║Żn ß╗®ng tß║Īo th├Ānh dd bazŲĪ ŌćÆ dd NH3 l├Ā bazŲĪ yß║┐u:
NH3 + H2O \(\rightleftharpoons\) NH4++ OH-
- L├Ām quß╗│ t├Łm chuyß╗ān sang m├Āu xanh
T├Īc dß╗źng vß╗øi dung dß╗ŗch bazŲĪ
- Dung dß╗ŗch NH3 c├│ khß║Ż n─āng l├Ām kß║┐t tß╗¦a nhiß╗üu hidrox├Łt kim loß║Īi
AlCl3 + 3NH3 + 3 H2O ŌåÆ Al(OH)3 \(\downarrow\) + 3 NH4Cl
Al3++3NH3+3H2O ŌåÆ Al(OH)3 \(\downarrow\) + 3NH4+
T├Īc dß╗źng vß╗øi ax├Łt
2NH3 + H2SO4 ŌåÆ (NH4)2SO4
NH3 (k) + HCl (k) ŌåÆ NH4Cl
(kh├┤ng m├Āu) (ko m├Āu) (kh├│i trß║»ng)
Video 2: Amoniac t├Īc dß╗źng vß╗øi axit clohidric
T├Łnh khß╗Ł
Trong ph├ón tß╗Ł NH3, N c├│ sß╗æ oxi h├│a l├Ā -3. NitŲĪ c├│ c├Īc sß╗æ oxi h├│a l├Ā -3,0,+1,+2,+3,+4,+5. NhŲ░ vß║Ły trong c├Īc phß║Żn ß╗®ng h├│a hß╗Źc khi c├│ sß╗▒ thay ─æß╗Ģi sß╗æ oxi h├│a, sß╗æ oxi h├│a cß╗¦a N trong NH3 chß╗ē c├│ thß╗ā t─āng l├¬n ŌåÆ thß╗ā hiß╗ćn t├Łnh khß╗Ł.
T├Īc dß╗źng vß╗øi oxi
Video 3: Th├Ł nghiß╗ćm giß╗»a NH3 v├Ā Oxi
NH3 ─æŲ░ß╗Żc tß║Īo ra tß╗½ phß║Żn ß╗®ng cß╗¦a NH4Cl v├Ā CaO
Kh├Ł O2 ─æŲ░ß╗Żc tß║Īo ra tß╗½ phß║Żn ß╗®ng cß╗¦a KClO3 v├Ā MnO2
- Hiß╗ćn tŲ░ß╗Żng: Que ─æ├│m ─æang ch├Īy bß╗Śng vß╗źt tß║»t
- Giß║Żi th├Łch: Kh├Ł N2 kh├┤ng duy tr├¼ sß╗▒ ch├Īy 4 NH3 + 3O2
2N2 + 6 H2O
T├Īc dß╗źng vß╗øi Clo
2NH3 + 3Cl2 ŌåÆ N2 + 6 HCl
Nß║┐u NH3 dŲ░ : NH3 + HCl ŌåÆ NH4Cl (kh├│i trß║»ng)
* Kß║┐t luß║Łn: Amoniac c├│ c├Īc t├Łnh chß║źt ho├Ī hß╗Źc cŲĪ bß║Żn: T├Łnh bazŲĪ yß║┐u v├Ā T├Łnh khß╗Ł
1.1.4. ß╗©ng dß╗źng
- Sß║Żn xuß║źt HNO3
- Sß║Żn xuß║źt ph├ón ─æß║Īm v├Ā dd NH3 c├│ thß╗ā sß╗Ł dß╗źng trß╗▒c tiß║┐p l├Ām ph├ón b├│n
- ─Éiß╗üu chß║┐ N2H4 l├Ām nhi├¬n liß╗ću cho t├¬n lß╗Ła
- NH3 lß╗Ång d├╣ng l├Ām chß║źt l├Ām lß║Īnh cho thiß║┐t bß╗ŗ lß║Īnh
- Sß╗Ł dß╗źng trong c├┤ng nghiß╗ćp ─æ├┤ng lß║Īnh (sß║Żn xuß║źt nŲ░ß╗øc ─æ├Ī, bß║Żo quß║Żn n├┤ng phß║®m...)
- Sß╗Ł dß╗źng trong c├┤ng nghiß╗ćp m├┤i trŲ░ß╗Øng (loß║Īi bß╗Å mß╗Öt sß╗æ kh├Ł g├óy ├┤ nhiß╗ģm nhŲ░ SO2...)
1.1.5. Điều chế
Trong ph├▓ng th├Ł nghiß╗ćm
- ─Éun n├│ng muß╗æi amoni vß╗øi Ca(OH)2 hay dd kiß╗üm: 2NH4Cl+Ca(OH)2 ŌåÆ CaCl2+2NH3 \(\uparrow\)+2H2O
- ─Éß╗ā l├Ām kh├┤ kh├Ł, ta cho kh├Ł NH3 c├│ lß║½n hŲĪi nŲ░ß╗øc qua b├¼nh v├┤i sß╗æng CaO.
- ─Éiß╗üu chß║┐ nhanh 1 lŲ░ß╗Żng nhß╗Å kh├Ł NH3, ta ─æun n├│ng dung dß╗ŗch NH3 ─æß║Łm ─æß║Ęc.
Trong c├┤ng nghiß╗ćp
N2 + 3H2 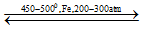
- Nhiß╗ćt ─æß╗Ö: 450 ŌĆō 500OC
- ├üp suß║źt: 200- 300 atm
- Chß║źt x├║c t├Īc: Fe/Al2O3, K2O
1.2. MUỐI AMONI
Muß╗æi amoni l├Ā chß║źt tinh thß╗ā ion gß╗ōm cation amoni NH4+ v├Ā anion gß╗æc ax├Łt. V├Ł dß╗ź: NH4Cl, (NH4)2SO4 , (NH4)2CO3
1.2.1.T├Łnh chß║źt vß║Łt l├Į
- Tinh thß╗ā
- ─Éß╗üu tan trong nŲ░ß╗øc
- Ion NH4+ kh├┤ng m├Āu
1.2.2.T├Łnh chß║źt ho├Ī hß╗Źc
T├Īc dß╗źng vß╗øi bazŲĪ kiß╗üm
(NH4)2SO4 + 2NaOH ŌåÆ Na2SO4 + 2NH3 + 2H2O.
PhŲ░ŲĪng tr├¼nh ion thu gß╗Źn: NH4+ + OH- ŌåÆ NH3 + H2O ŌåÆ ─Éiß╗üu chß║┐ NH3 trong Ph├▓ng th├Ł nghiß╗ćm v├Ā nhß║Łn biß║┐t muß╗æi amoni.
Phß║Żn ß╗®ng nhiß╗ćt ph├ón
- Muß╗æi amoni tß║Īo bß╗¤i ax├Łt kh├┤ng c├│ t├Łnh oxi ho├Ī: (HCl,H2CO3) ŌåÆ NH3
NH4Cl (r) .PNG)
(NH4)2CO3 (r) .PNG)
NH4HCO3(r) .PNG)
- (NH4)2CO3; NH4HCO3 ß╗¤ nhiß╗ćt ─æß╗Ö thŲ░ß╗Øng c┼®ng tß╗▒ ph├ón huß╗Ę; ß╗¤ nhiß╗ćt ─æß╗Ö cao phß║Żn ß╗®ng xß║Ży ra nhanh hŲĪn; D├╣ng NH4HCO3 trong bß╗Öt nß╗¤.
- Muß╗æi amoni tß║Īo bß╗¤i ax├Łt c├│ t├Łnh oxi ho├Ī: (HNO2, HNO3) ŌåÆ N2 , N2O
NH4NO2 .PNG)
NH4NO3 .PNG)
B├Āi tß║Łp minh hß╗Źa
B├Āi 1:
─Éß╗ā nhß║Łn biß║┐t c├Īc dung dß╗ŗch: NH4NO3, (NH4)2SO4, K2SO4 ─æß╗▒ng trong c├Īc lß╗Ź mß║źt nh├Żn ta d├╣ng:
HŲ░ß╗øng dß║½n:
- BŲ░ß╗øc 1: Tr├Łch dß║½n 3 mß║½u thß╗Ł
- BŲ░ß╗øc 2: Bari tan trong nŲ░ß╗øc tß║Īo dung dß╗ŗch Ba(OH)2
- NH4NO3: c├│ kh├Ł m├╣i khai: Ba(OH)2 + 2NH4NO3 ŌåÆ Ba(NO3)2 + 2NH3\(\uparrow\) + 2H2O
- (NH4)2SO4: kh├Ł m├╣i khai v├Ā kß║┐t tß╗¦a trß║»ng: Ba(OH)2 + (NH4)2SO4 ŌåÆ BaSO4\(\downarrow\) + 2NH3\(\uparrow\) + 2H2O
- K2SO4: kß║┐t tß╗¦a trß║»ng: Ba(OH)2 + K2SO4: ŌåÆ BaSO4 \(\downarrow\)+ 2KOH
B├Āi 2:
Hß╗Śn hß╗Żp X gß╗ōm N2 v├Ā H2 c├│ tß╗ē khß╗æi so vß╗øi He bß║▒ng 1,8. ─Éun n├│ng X mß╗Öt thß╗Øi gian trong b├¼nh k├Łn (c├│ bß╗Öt Fe l├Ām x├║c t├Īc) thu ─æŲ░ß╗Żc hß╗Śn hß╗Żp Y c├│ tß╗ē khß╗æi so vß╗øi He bß║▒ng 2. Hiß╗ću suß║źt cß╗¦a phß║Żn ß╗®ng tß╗Ģng hß╗Żp NH3 l├Ā:
HŲ░ß╗øng dß║½n:
MX = 7,2. ├üp dß╗źng quy tß║»c ─æŲ░ß╗Øng ch├®o ta c├│: \(n_{H_2}:n_{N_2}=4:1\)
ŌćÆ Giß║Ż sß╗Ł ban ─æß║¦u c├│ 4 mol H2 v├Ā 1 mol N2 trong X
N2 + 3H2 Ōåö 2NH3
x ŌåÆ x ŌåÆ 2x
ŌćÆ sau phß║Żn ß╗®ng: nY = 2x + (1 - x) + (4 - 3x) = 5 - 2x mol
Bß║Żo to├Ān khß╗æi lŲ░ß╗Żng: mX = mY
ŌćÆ 5 ├Ś 7,2 = (5 - 2x) ├Ś 2 ├Ś 4
ŌćÆ x = 0,25 mol
ŌćÆ H% (t├Łnh theo N2) = 25%
B├Āi 3:
Cho c├Īc phß║Żn ß╗®ng sau:
4NH3 + 5O2 ŌåÆ 4NO + 6H2O (1)
NH3 + H2SO4 ŌåÆ NH4HSO4 (2)
2NH3 + 3CuO ŌåÆ 3Cu + N2\(\uparrow\) + 3H2O (3)
8NH3 + 3Cl2 ŌåÆ N2 + 6NH4Cl (4)
NH3 + H2S ŌåÆ NH4HS (5)
2NH3 + 3O2 ŌåÆ 2N2\(\uparrow\) + 6H2O (6)
NH3 + HCl ŌåÆ NH4Cl (7)
Sß╗æ phß║Żn ß╗®ng trong ─æ├│ NH3 kh├┤ng ─æ├│ng vai tr├▓ l├Ā chß║źt khß╗Ł l├Ā:
HŲ░ß╗øng dß║½n:
C├Īc phß║Żn ß╗®ng m├Ā c├│ sß╗▒ t─āng sß╗æ oxi h├│a cß╗¦a N ŌćÆ NH3 thß╗ā hiß╗ćn t├Łnh khß╗Ł. C├Īc phß║Żn ß╗®ng kh├┤ng c├│ hiß╗ćn tŲ░ß╗Żng tr├¬n l├Ā: 2, 5, 7.
3. Luyß╗ćn tß║Łp B├Āi 8 H├│a hß╗Źc 11
Sau b├Āi hß╗Źc cß║¦n nß║»m:
- Cß║źu tß║Īo ph├ón tß╗Ł, t├Łnh chß║źt vß║Łt l├Ł (t├Łnh tan, tß╗ē khß╗æi, m├Āu, m├╣i), ß╗®ng dß╗źng ch├Łnh, amoniac trong ph├▓ng th├Ł nghiß╗ćm v├Ā trong c├┤ng nghiß╗ćp.
- T├Łnh chß║źt ho├Ī hß╗Źc cß╗¦a amoniac: T├Łnh bazŲĪ yß║┐u (t├Īc dß╗źng vß╗øi nŲ░ß╗øc, dung dß╗ŗch muß╗æi, axit) v├Ā t├Łnh khß╗Ł (t├Īc dß╗źng vß╗øi oxi, clo).
- C├Īch ─æiß╗üu chß║┐ NH3. T├Łnh chß║źt vß║Łt l├Ł (trß║Īng th├Īi, m├Āu sß║»c, t├Łnh tan).
- T├Łnh chß║źt ho├Ī hß╗Źc (phß║Żn ß╗®ng vß╗øi dung dß╗ŗch kiß╗üm, phß║Żn ß╗®ng nhiß╗ćt ph├ón) v├Ā ß╗®ng dß╗źng cß╗¦a muß╗æi amoni.
3.1. Trß║»c nghiß╗ćm
B├Āi kiß╗ām tra Trß║»c nghiß╗ćm H├│a hß╗Źc 11 B├Āi 8 c├│ phŲ░ŲĪng ph├Īp v├Ā lß╗Øi giß║Żi chi tiß║┐t gi├║p c├Īc em luyß╗ćn tß║Łp v├Ā hiß╗āu b├Āi.
-
- A. SO2.
- B. Cl2.
- C. CH4.
- D. NH3.
-
- A. NaNO3.
- B. NH4NO3.
- C. AgNO3.
- D. Cu(NO3)2.
-
- A. NaOH.
- B. Ba(OH)2.
- C. BaCl2.
- D. AgNO3.
C├óu 4-10: Mß╗Øi c├Īc em ─æ─āng nhß║Łp xem tiß║┐p nß╗Öi dung v├Ā thi thß╗Ł Online ─æß╗ā cß╗¦ng cß╗æ kiß║┐n thß╗®c vß╗ü b├Āi hß╗Źc n├Āy nh├®!
3.2. B├Āi tß║Łp SGK v├Ā N├óng cao
C├Īc em c├│ thß╗ā hß╗ć thß╗æng lß║Īi nß╗Öi dung b├Āi hß╗Źc th├┤ng qua phß║¦n hŲ░ß╗øng dß║½n Giß║Żi b├Āi tß║Łp H├│a hß╗Źc 11 B├Āi 8.
B├Āi tß║Łp 1 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 2 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 3 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 4 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 5 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 6 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 7 trang 37 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 8 trang 38 SGK H├│a hß╗Źc 11
B├Āi tß║Łp 8.1 trang 11 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.2 trang 11 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.3 trang 11 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.4 trang 11 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.5 trang 12 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.6 trang 12 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.7 trang 12 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.8 trang 12 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.9 trang 13 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.10 trang 13 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.11 trang 13 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 8.12 trang 13 SBT H├│a hß╗Źc 11
B├Āi tß║Łp 1 trang 47 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 2 trang 47 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 3 trang 47 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 4 trang 47 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 5 trang 47 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 6 trang 47 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 7 trang 48 SGK H├│a hß╗Źc 11 n├óng cao
B├Āi tß║Łp 8 trang 48 SGK H├│a hß╗Źc 11 n├óng cao
4. Hß╗Åi ─æ├Īp vß╗ü B├Āi 8 ChŲ░ŲĪng 2 H├│a hß╗Źc 11
Trong qu├Ī tr├¼nh hß╗Źc tß║Łp nß║┐u c├│ bß║źt k├¼ thß║»c mß║»c g├¼, c├Īc em h├Ży ─æß╗ā lß║Īi lß╗Øi nhß║»n ß╗¤ mß╗źc Hß╗Åi ─æ├Īp ─æß╗ā c├╣ng cß╗Öng ─æß╗ōng H├│a HOC247 thß║Żo luß║Łn v├Ā trß║Ż lß╗Øi nh├®.