Giải bài 6 tr 119 sách GK Hóa lớp 10
Một nguyên tố halogen có cấu hình electron lớp ngoài cùng của nguyên tử là 4s24p5.
a) Viết cấu hình electron nguyên tử đầy đủ của nguyên tố trên.
b) Cho biết tên, kí hiệu và cấu tạo phân tử của nguyên tố hóa này.
c) Nêu tính chất hóa học cơ bản của nguyên tố này và dẫn ra những phản ứng hóa học để minh họa
d) So sánh tính chất hóa học của nguyên tố này với hai nguyên tố halogen khác đứng trên và dưới nó trong nhóm halogen và dẫn ra phản ứng để minh họa.
Gợi ý trả lời bài 6
Câu a:
Halogen có cấu hình electron lớp ngoài cùng của nguyên tử là 4s24p5.
Cấu hình đầy đủ là: 1s2 2s2 2p6 3s2 3p6 3d10 4s24p5
Câu b:
Tên nguyên tố là brom, kí hiệu là Br, công thức phân tử Br2
Câu c:
Tính chất hóa học của nguyên tố này là tính oxi hóa.
Brom phản ứng với nhiều kim loại.
3Br2 + 2Al → Al2Br3
Brom tác dụng với nước tương tự như clo nhưng khó khăn hơn.
Br2 + H2O ⇔ HBr + HbrO
Brom thể hiện tính khử khi tác dụng với chất oxxi hóa mạnh.
Br2 + 5Cl2 + H2O → 2HbrO3 + 10HCl
Brom có thể oxi hóa muối iotua thành iot.
Br2 + NaI → 2NaBr + I2
Câu d:
So sánh tính chất hóa học của brom với clo và iot.
Brom có tính oxi hóa yếu hơn clo nhưng mạnh hơn iot nên:
Cl2 + 2NaBr → 2NaCl + Br2
Br2 + NaI → 2NaBr + I2
-- Mod Hóa Học 10 HỌC247
Video hướng dẫn giải bài 6 SGK
-


Có bao nhiêu phản ứng hóa học nào có thể tạo thành Clo?
bởi Lam Van
 11/05/2022
11/05/2022
(1). Sục khí F2 vào dung dịch NaCl.
(2). Điện phân dung dịch NaCl có màng ngăn.
(3). Điện phân dung dịch HCl.
(4). Cho HCl tác dụng với KMnO4.
(5). Cho HCl tác dụng với K2Cr2O7.
(6). Cho HCl tác dụng với Clorua vôi.
(7). Cho HCl tác dụng với MnO2.
(8). Cho HCl tác dụng với KClO3.
(9). Cho NaCl (rắn) tác dụng H2SO4 đặc.
(10). Điện phân nóng chảy KCl.
Theo dõi (0) 1 Trả lời -


A. Giấm ăn.
B. Clorua vôi.
C. Natri cacbonat.
D. Amoni clorua.
Theo dõi (0) 1 Trả lời -


Điện phân dung dịch NaCl (dùng điện cực trơ và có màng ngăn xốp) thì điều gì sẽ xảy ra?
bởi hà trang
 11/05/2022
11/05/2022
A. Ở cực âm xảy ra quá trình oxi hóa H2O và ở cực dương xảy ra quá trình khử ion Cl–.
B. Ở cực dương xảy ra quá trình oxi hóa ion Na+ và ở cực âm xảy ra quá trình khử ion Cl–.
C. Ở cực âm xảy ra quá trình khử H2O và ở cực dương xảy ra quá trình oxi hóa ion Cl–.
D. Ở cực dương xảy ra quá trình khử ion Na+ và ở cực âm xảy ra quá trình oxi hóa ion Cl-.
Theo dõi (0) 1 Trả lời -


Dùng 6,125 gam KClO3 tác dụng với dung dịch HCl đặc (dư), sau khi phản ứng xảy ra hoàn toàn thì sốmol HCl bị oxi hóa là bao nhiêu?
bởi An Duy
 12/05/2022
Theo dõi (0) 1 Trả lời
12/05/2022
Theo dõi (0) 1 Trả lời -


Cho 37,92 gam KMnO4 một thời gian thu được 35,36 gam chất rắn X. Trộn m gam kaliclo rát với chất rắn X thu được chất rắn Y. Cho toàn bộ chất rắn Y vào HCl đặc dư thu được 15,904 lít khí Cl2 (đktc) giá trị của m là?
bởi Phong Vu
 11/05/2022
Theo dõi (0) 1 Trả lời
11/05/2022
Theo dõi (0) 1 Trả lời -

 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Cho các kim loại nào sau đây tác dụng với Cl2 và dung dịch HCl đều cho cùng một muối.
bởi Nguyễn Lê Tín
 11/05/2022
Theo dõi (0) 1 Trả lời
11/05/2022
Theo dõi (0) 1 Trả lời -


Cho Cl2 trong phòng thí nghiệm từ MnO2 và dung dịch HCl đặc. Nếu không dùng đèn cồn thì có thể thay MnO2 bằng hóa chất nào (các dụng cụ và hóa chất khác không thay đổi) sau đây?
bởi Trịnh Lan Trinh
 11/05/2022
11/05/2022
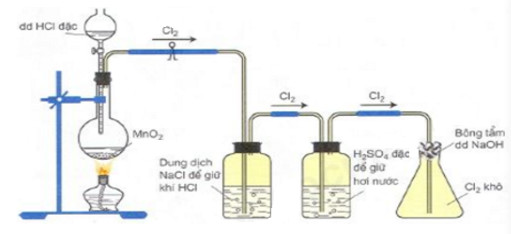 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Số cặp chất xảy ra phản ứng ở nhiệt độ thường là?
bởi hi hi
 12/05/2022
12/05/2022
Cho các cặp chất sau:
(1) Cl2 và H2
(2) H2S và SO2
(3) H2S và dung dịch AgNO3
(4) Cl2 và dung dịch NaOH
(5) NH3 và dung dịch AlCl3
(6) Dung dịch KMnO4 và SO2
(7) Si và dung dịch NaOH loãng
(8) CO2 và dung dịch NaClO
(9) H2S và O2
(10) Cl2 và NH3
Theo dõi (0) 1 Trả lời -


Cho Cl2 + KOH \(\small \xrightarrow{t^0}\) KClO3 + KCl + H2O. Clo đóng vai trò là gì?
bởi Vương Anh Tú
 12/05/2022
Theo dõi (0) 1 Trả lời
12/05/2022
Theo dõi (0) 1 Trả lời -


Dãy xếp đúng thứ tự tính axit và tính khử giảm dần?
bởi Anh Trần
 11/05/2022
11/05/2022
A. HCl, HBr, HI, HF.
B. HI, HBr, HCl, HF.
C. HCl, HI, HBr, HF.
D. HF, HCl, HBr, HI.
Theo dõi (0) 1 Trả lời -


Cho KMnO4 và KClO3 với 1 lượng MnO2 trong bình kín thu được hỗn hợp X. Lấy 52,550g X đem nung nóng sau thời gian thì được hỗn hợp rắn Y và V lít O2. Biết KClO3 bị nhiệt phân hoàn toàn tạo 14,9g KCl chiếm 36,315% khối lượng Y. Sau đó cho toàn bộ Y tác dụng với HCl đặc dư nung nóng, cô cạn thu được 51,275g muối khan. Hiệu suất của quá trình nhiệt phân muối KMnO4 là gì?
bởi Thùy Trang
 11/05/2022
Theo dõi (0) 1 Trả lời
11/05/2022
Theo dõi (0) 1 Trả lời -


Cho X, Y và các muối clorua của chúng tham gia các phản ứng sau X + 2YCl3 \(\rightarrow\) XCl2 + 2YCl2, Y + XCl2 \(\rightarrow\) YCl2 + X Theo các phản ứng trên, nhận xét nào sau đây đúng?
bởi Dương Quá
 12/05/2022
Theo dõi (0) 1 Trả lời
12/05/2022
Theo dõi (0) 1 Trả lời -


Trong các khẳng định sau, có mấy khẳng định đúng? (1) Nhiệt độ sôi và nhiệt độ nóng chảy của các halogen tăng dần theo thứ tự F2, Cl2, Br2, I2.
bởi Trịnh Lan Trinh
 12/05/2022
12/05/2022
(2) Muối iot là muối ăn có trộn lượng nhỏ KI hoặc I2.
(3) Cho khí clo đi qua dung dịch KOH đun nóng, lấy dung dịch thu được trộn với kali clorua và làm lạnh, ta sẽ thu được kali peclorat kết tinh.
(4) Khi cho F2 tác dụng với dung dịch NaOH loãng lạnh, xảy ra phản ứng tự oxi hóa, tự khử.
(5) Dung dịch NaF loãng được dùng làm thuốc chống sâu răng.
Theo dõi (0) 1 Trả lời -


A. O2 và Cl2.
B. NH3 và Cl2.
C. H2S và Cl2.
D. HI và Cl2.
Theo dõi (0) 1 Trả lời -


Tiến hành thí nghiệm như hình vẽ.
bởi Trung Phung
 11/05/2022
11/05/2022
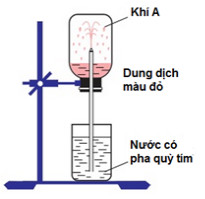
Khí A trong bình có thể là khí nào dưới đây?
Theo dõi (0) 1 Trả lời -


Cho NaX (rắn) + H2SO4 (đặc) \(\overset{t^0}{\rightarrow}\) NaHSO4 + HX (khí). Các hiđro halogenua (HX) có thể điều chế theo phản ứng trên là?
bởi Trần Thị Trang
 11/05/2022
Theo dõi (0) 1 Trả lời
11/05/2022
Theo dõi (0) 1 Trả lời
Bài tập SGK khác
Bài tập 4 trang 118 SGK Hóa học 10
Bài tập 5 trang 118 SGK Hóa học 10
Bài tập 7 trang 119 SGK Hóa học 10
Bài tập 8 trang 119 SGK Hóa học 10
Bài tập 9 trang 119 SGK Hóa học 10
Bài tập 10 trang 119 SGK Hóa học 10
Bài tập 11 trang 119 SGK Hóa học 10
Bài tập 12 trang 119 SGK Hóa học 10
Bài tập 13 trang 119 SGK Hóa học 10
Bài tập 14 trang 119 SGK Hóa học 10
Bài tập 26.1 trang 60 SBT Hóa học 10
Bài tập 26.2 trang 60 SBT Hóa học 10
Bài tập 26.3 trang 60 SBT Hóa học 10
Bài tập 26.4 trang 61 SBT Hóa học 10
Bài tập 26.5 trang 61 SBT Hóa học 10
Bài tập 26.6 trang 61 SBT Hóa học 10
Bài tập 26.7 trang 61 SBT Hóa học 10
Bài tập 26.8 trang 61 SBT Hóa học 10
Bài tập 26.9 trang 61 SBT Hóa học 10
Bài tập 26.10 trang 61 SBT Hóa học 10
Bài tập 26.11 trang 61 SBT Hóa học 10
Bài tập 26.12 trang 62 SBT Hóa học 10
Bài tập 26.13 trang 62 SBT Hóa học 10
Bài tập 26.14 trang 62 SBT Hóa học 10
Bài tập 26.15 trang 62 SBT Hóa học 10
Bài tập 26.16 trang 62 SBT Hóa học 10
Bài tập 1 trang 149 SGK Hóa học 10 nâng cao
Bài tập 2 trang 149 SGK Hóa học 10 nâng cao
Bài tập 3 trang 149 SGK Hóa học 10 nâng cao
Bài tập 4 trang 149 SGK Hóa học 10 nâng cao
Bài tập 5 trang 150 SGK Hóa học 10 nâng cao
Bài tập 6 trang 150 SGK Hóa học 10 nâng cao
Bài tập 7 trang 150 SGK Hóa học 10 nâng cao
Bài tập 8 trang 150 SGK Hóa học 10 nâng cao





