Bài tập 13.5 trang 20 SBT Hóa học 11
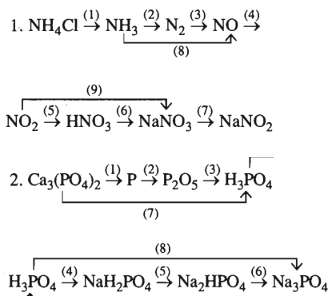
Viết các phương trình hóa học thực hiện các dãy chuyển hóa sau:
Hướng dẫn giải chi tiết bài 13.5
1.
(1) NH4Cl + NaOH → NH3 + H2O + NaCl
(2) 4NH3 + 3O2 → 2N2 + 6H2O
(3) N2 + O2 ⇔ 2NO
(4) 2NO + O2 → 2NO2
(5) 4NO2 + O2 + 2H2O → 4HNO3
(6) HNO3 + NaOH → NaNO3 + H2O
(7) 2NaNO3 → 2NaNO2 + O2
(8) 4NH3 + 5O2 → 4NO + 6H2O (đk: 850 - 900oC)
(9) 2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O
2.
(1) Ca3(PO4)2 + 3SiO2 + 5C (1200oC)→ 2P + 3CaSiO3 + 5CO
(2) 4P + 5O2 to→ 2P2O5
(3) P2O5 + 3H2O → 2H3PO4
(4) H3PO4 + NaOH → NaH2PO4 + H2O
(5) NaH2PO4 + NaOH → Na2HPO4 + H2O
(6) Na2HPO4 + NaOH → Na3PO4 + H2O
(7) Ca3(PO4)2 + 3H2SO4 → 2H3PO4 + 3CaSO4
(8) H3PO4 + 3NaOH → Na3PO4 + 3H2O
-- Mod Hóa Học 11 HỌC247
-


Cho 5 lọ mất nhãn đựng các dung dịch : \(KNO_3, Cu(NO_3)_2, FeCl_3\) và \(NH_4Cl\). Chỉ sử dụng duy nhất một thuốc thử, hãy nhận biết các dung dịch trên
bởi Ban Mai
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Có 5 dung dịch mất nhãn gồm \(CuCl_2, NaNO_3, Mg(NO_3)_2; NH_4NO_3\) và \(Fe(NO_3)_3\). Có thể dùng kim loại nào sau đây để phân biệt cả 5 dung dịch?
bởi Bo Bo
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Trong nước tự nhiên thường có lẫn những lượng nhỏ các muối \(Ca(NO_3)_2, Mg(NO_3)_2, Ca(HCO_3)_2\) và \(Mg(HCO_3)_2\). Có thể dùng một hóa chất nào sau đây để loại được tất cả các muối trên?
bởi Trần Phương Khanh
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Cho năm lọ mất nhãn đựng các dung dịch: \(KNO_3, Cu(NO_3)_2, FeCl_3\) và \(NH_4Cl\). Có thể dùng hóa chất nào sau đây để nhận biết chúng?
bởi Lê Minh
 22/02/2021
Theo dõi (0) 1 Trả lời
22/02/2021
Theo dõi (0) 1 Trả lời -


Cho ba hợp kim: Cu-Ag, Cu-Al, Cu-Zn. Thuốc thử nào sau đây có thể được dùng để phân biệt ba hợp kim trên?
bởi Nguyễn Thị Trang
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dug dịch hỗn hợp HCl 0,1M và \(H_2SO_4\) 0,05M để thu được dung dịch có pH = 2 ?
bởi hi hi
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Để xác định nồng đội dung dịch NaOH người ta tiến hành như sau: cân 1,26 gam axit oxalic ngậm nước (\(H_2C_2O_4.2H_2O\)) hòa tan hoàn toàn vào nước, định mức thành 100 ml. lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng.
bởi Nguyễn Minh Hải
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Chuẩn độ 20 ml dung dịch hỗn hợp HCl 0,1M + \(HNO_3\) a mol/l cần dùng hết 16,5 ml dung dịch hỗn hợp KOH 0,1M và \(Ba(OH)_2\) 0,05M. Giá trị của a là:
bởi Lê Nguyễn Hạ Anh
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời -


Để xác định nồng độ dung dịch \(H_2O_2\), người ta hòa tan 0,5 gam nước oxi già vào nước, thêm \(H_2SO_4\) tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch \(KMnO_4\) 0,1M. Xác định hàm lượng \(H_2O_2\) trong nước oxi già.
bởi Thùy Nguyễn
 22/02/2021
Theo dõi (0) 1 Trả lời
22/02/2021
Theo dõi (0) 1 Trả lời -


Chuẩn độ 20 ml dung dịch HCl chưa biết nồng độ đã dùng hết 17 ml dung dịch NaOH 0,12M. Xác định nồng độ mol của dung dịch HCl.
bởi Nguyễn Tiểu Ly
 22/02/2021
Theo dõi (0) 1 Trả lời
22/02/2021
Theo dõi (0) 1 Trả lời -


Xà phòng hóa 8,8 gam etyl axetat bằng 200ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được chất rắn có khối lượng là:
bởi Nguyễn Thị Thúy
 23/02/2021
Theo dõi (0) 1 Trả lời
23/02/2021
Theo dõi (0) 1 Trả lời
Bài tập SGK khác
Bài tập 13.3 trang 20 SBT Hóa học 11
Bài tập 13.4 trang 20 SBT Hóa học 11
Bài tập 13.6 trang 21 SBT Hóa học 11
Bài tập 13.7 trang 21 SBT Hóa học 11
Bài tập 13.8 trang 21 SBT Hóa học 11
Bài tập 13.9 trang 21 SBT Hóa học 11
Bài tập 1 trang 57 SGK Hóa học 11 nâng cao
Bài tập 2 trang 58 SGK Hóa học 11 nâng cao
Bài tập 3 trang 58 SGK Hóa học 11 nâng cao
Bài tập 4 trang 58 SGK Hóa học 11 nâng cao
Bài tập 5 trang 58 SGK Hóa học 11 nâng cao
Bài tập 1 trang 72 SGK Hóa học 11 nâng cao
Bài tập 2 trang 72 SGK Hóa học 11 nâng cao
Bài tập 3 trang 72 SGK Hóa học 11 nâng cao