Các em đã nghiên cứu các tính chất hóa học của Axit, Bazơ; Ngoài những tính chất đã tìm hiểu ra. Thì hai hợp chất này còn có thêm một tính chất nữa là tác dụng với muối, vậy Muối tác dụng với Axit, Bazơ tạo ra sản phẩm gì? Và còn có tính chất nào khác nữa không? Ta vào bài học mới ngày hôm nay.
Tóm tắt lý thuyết
1.1. Tính chất hoá học của muối
1.1.1. Muối tác dụng với kim loại (tạo muối mới + kim loại mới)
- Các em chú ý quan sát thao tác tiến hành thí nghiệm và hiện tượng của phản ứng:
Video 1: Phản ứng giữa AgNO3 và kim loại Cu
- Hiện tượng: Có kim loại màu xám bạc bám bên ngoài dây đồng. Dung dịch ban đầu không màu dần chuyển qua màu xanh
- Giải thích: Do xảy ra phản ứng Cu+ AgNO3 → Cu(NO3)2 + 2Ag. Kim loại Ag sinh ra, bám vào dây đồng và dung dịch có màu xanh của Cu(NO3)2
1.1.2. Muối tác dụng với Axit (tạo muối mới, axit mới)
Lưu ý: Với sản phẩm sinh ra là axit yếu sẽ không tồn tại mà chuyển hóa thành chất bền hơn.
- Các em chú ý quan sát thao tác thí nghiệm và hiện tượng phản ứng diễn ra:
Video 2: Thí nghiệm giữa dung dịch BaCl2 và H2SO4
- Hiện tượng: Có kết tủa trắng xuất hiện
- Giải thích:
+ Gốc =SO4 trong phân tử H2SO4 kết hợp với nguyên tố Bari trong phân tử BaCl2 tạo thành kết tủa BaSO4
+ Phương trình hóa học: H2SO4 + BaCl2 → BaSO4 + 2HCl
1.1.3. Muối tác dụng với Muối (tạo muối mới 1 + muối mới 2)
- Các em chú ý quan sát thao tác thí nghiệm và hiện tượng phản ứng diễn ra:
Video 3: Phản ứng giữa dung dịch NaCl và AgNO3
- Hiện tượng: Xuất hiện kết tủa trắng
- Giải thích: Do xảy ra phản ứng AgNO3+NaCl → AgCl+ NaNO3. Kết tủa trắng chính là AgCl sỉnh ra.
1.1.4. Muối tác dụng với Bazơ (tạo Muối mới + bazơ mới)
- Các em chú ý quan sát thao tác thí nghiệm và hiện tượng phản ứng diễn ra:
Video 2: Phản ứng giữa dung dịch Cu(OH)2 và H2SO4
- Hiện tượng: Cu(OH)2 tan dần và tạo dung dịch màu xanh
- Giải thích: Do xảy ra phản ứng H2SO4l+Cu(OH)2 → CuSO4 + 2H2O
Ví dụ khác:
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
Ba(OH)2+ 2HNO3→ Ba(NO3)2 + 2H2O
1.1.5. Phản ứng phân huỷ muối
Một số muối ở nhiệt độ cao sẽ bị phân huỷ.
2KClO3 (xúc tác MnO2) → 2KCl + 3O2
Video 3: Phản ứng nhiệt phân muối KClO3 với xúc tác MnO2
1.2. Phản ứng trao đổi trong dung dịch
1.2.1. Nhận xét về các phản ứng hóa học của muối
Các phản ứng trong dung dịch của muối với Axit, Bazơ và Muối xảy ra có sự trao đổi các thành phần với nhau tạo ra những hợp chất mới.
1.2.2. Phản ứng trao đổi
Là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới.
1.2.3. Điều kiện xảy ra phản ứng trao đổi:
Phản ứng trao đổi trong dung dịch của các chất chỉ xảy ra nếu sản phẩm tạo thành có chất không tan hoặc chất khí.
Bài tập minh họa
Bài 1:
Hoàn thành sơ đồ phản ứng sau đây:
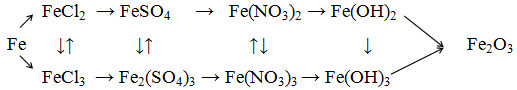
Hướng dẫn:
Fe + 2HCl → FeCl2 + H2
FeCl2 + Ag2SO4 → FeSO4 + 2AgCl↓
FeSO4 + Ba(NO3)2 → Fe(NO3)2 + BaSO4↓
Fe(NO3)2 + 2KOH → Fe(OH)2 + 2KNO3
Fe(OH)2 + O2 (t0) → Fe2O3 + H2O
2Fe + 3Cl2 → 2FeCl3
2FeCl3 + 3Ag2SO4 → Fe2(SO4)3 + 6AgCl↓
Fe2(SO4)3 + 3Ba(NO3)2 → 2Fe(NO3)3 + 3BaSO4↓
Fe(NO3)3 + 3KOH → Fe(OH)3 + 3KNO3
2Fe(OH)3 (t0) → Fe2O3 + H2O
2FeCl2 (lục nhạt)+ Cl2 → 2FeCl3(vàng nâu)
2FeCl3 + Fe → 3FeCl2
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Fe2(SO4)3 + Fe → 3FeSO4
4Fe(NO3)2 + O2 + 4HNO3 → 4Fe(NO3)3 + 2H2O
2Fe(NO3)3 + Cu → 2Fe(NO3)2 + Cu(NO3)2
4Fe(OH)2(trắng xanh) + O2 + 2H2O → 4Fe(OH)3(nâu đỏ)
Bài 2:
Cho H2SO4 loãng, dư tác dụng với hỗn hợp gồm Mg và Fe thu được 2,016 lít khí ở đktc. Nếu hỗn hợp kim loại này tác dụng với dd FeSO4 dư thì khối lượng hỗn hợp trên tăng lên 1,68 gam.
a. Viết phương trình phản ứng hóa học
b. Tìm khối lượng mỗi kim loại trong hỗn hợp trên
Hướng dẫn:
a. Ta có PTHH:
Mg + H2SO4 → MgSO4 + H2↑ (1)
x mol x mol x mol
Fe + H2SO4 → FeSO4 + H2↑ (2)
y mol y mol y mol
Cho hỗn hợp kim loại trên vào dd FeSO4 dư thì Mg tác dụng hết (Fe không tác dụng) theo phương trình sau:
Mg + FeSO4 → MgSO4 + Fe (3)
x mol x mol
khối lượng hỗn hợp tăng lên 1,68 gam là khối lượng chênh lệch giữa Fe mới tạo ra và Mg đã phản ứng.
b. Ta có số mol của khí H2 là 0,09 mol
theo phương trình (1) và (2) ta có hệ phương trình :
x + y = 0,09
56y – 24x = 1,68
Giải hệ phương trình trên ta được nghiệm : x = 0,0525; y = 0,0375
Vậy khối lượng của 2 kim loại trên là :
mFe = 0,0375. 56 = 2,1 (gam)
mMg = 0,0525. 24 = 1,26 (gam)
3. Luyện tập Bài 9 Hóa học 9
Sau bài học cần nắm: tính chất hóa học của muối
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 9 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
Câu 1:
Cho dung dịch axit sunfuric loãng tác dụng với muối natrisunfit ( Na2SO3). Chất khí nào sinh ra?
- A. Khí hiđro
- B. Khí oxi
- C. Khí lưu huỳnhđioxit
- D. Khí hiđro sunfua
-
- A. CO
- B. CO2
- C. H2
- D. Cl2
-
- A. Dung dịch NaOH
- B. Dung dịch HCl
- C. Dung dịch AgNO3
- D. Dung dịch BaCl2
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 9.
Bài tập 1 trang 33 SGK Hóa học 9
Bài tập 2 trang 33 SGK Hóa học 9
Bài tập 3 trang 33 SGK Hóa học 9
Bài tập 4 trang 33 SGK Hóa học 9
Bài tập 5 trang 33 SGK Hóa học 9
Bài tập 6 trang 33 SGK Hóa học 9
Bài tập 9.1 trang 11 SBT Hóa học 9
Bài tập 9.2 trang 11 SBT Hóa học 9
Bài tập 9.3 trang 11 SBT Hóa học 9
Bài tập 9.4 trang 11 SBT Hóa học 9
Bài tập 9.5 trang 12 SBT Hóa học 9
Bài tập 9.6 trang 12 SBT Hóa học 9
Bài tập 9.7 trang 12 SBT Hóa học 9
Bài tập 9.8 trang 12 SBT Hóa học 9
4. Hỏi đáp về Bài 9 chương 1 Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.












