HOC247 xin giới thiệu đến quý thầy cô giáo và các em học sinh Bộ 5 đề thi giữa HK2 môn Hóa học 12 năm 2021-2022 Trường THPT Lương Văn Can, đề thi gồm có các câu trắc nghiệm với đáp án đi kèm sẽ giúp các em luyện tập, làm quen các dạng đề đồng thời đối chiếu kết quả, đánh giá năng lực bản thân từ đó có kế hoạch học tập phù hợp. Mời các em cùng tham khảo!
|
TRƯỜNG THPT LƯƠNG VĂN CAN |
ĐỀ THI GIỮA HỌC KÌ 2 MÔN HÓA HỌC 12 NĂM HỌC 2021-2022 Thời gian làm bài 45 phút |
ĐỀ THI SỐ 1
Câu 1: Các chất đều tác dụng với dung dịch Ca(OH)2 gồm
A CO2, HNO3, NaNO3.
B NaHCO3, CO2, CH3NH2
C NH4NO3, Ca(HCO3)2, Na2CO3.
D CO2, NaCl, Na2CO3.
Câu 2: Có 4 dung dịch: Na2CO3, NaOH, NaCl, HCl. Nếu chỉ dùng thêm quỳ tím thì có thể nhận biết được
A 3dung dịch. B 4 dung dịch. C 1dung dịch. D 2 dung dịch.
Câu 3: Cho 14,4gam hỗn hợp Fe, Cu tác dụng với dung dịch HCl dư, sau phản ứng thu được 4,48 lít khí (đktc). Khối lượng của Cu trong hỗn hợp là
A 3,2 gam B 64,0 gam C 6,4 gam D 0,64 gam
Câu 4: Cho hỗn hợp CaO, MgO, Na2CO3, Fe3O4 tan vào nước ta thu được chất rắn gồm
A CaCO3, MgO, Fe3O4 B Na2CO3, Fe3O4. C MgO, Fe3O4. D CaO, MgO, Fe3O4.
Câu 5: Có 3 cốc nước : nước cất, nước cứng tạm thời (chứa Ca(HCO3)2), nước cứng vĩnh cửu (chứa CaSO4). Phương pháp nhận biết 3 cốc nước trên là
A đun nóng và dùng dung dịch Na2CO3.
B đun nóng, sau đó dùng dung dịch nước vôi.
C dùng quỳ tím, dùng dung dịch HCl.
D dùng dung dịch HCl, sau đó đun nhẹ.
Câu 6: Cho hỗn hợp Al, Fe vào dung dịch chứa hỗn hợp Cu(NO3)2 và AgNO3, sau phản ứng thu được hỗn hợp rắn gồm 3 kim loại. Ba kim loại đó là
A Al, Fe, Ag B Al, Fe, Cu C Ag, Cu, Fe D Ag, Cu, Al
Câu 7: .Mô tả nào dưới đây không phù hợp với nhôm?
A mức oxi hóa đặc trưng trong hợp chất là +3
B nhôm ở ô thứ 13, chu kì 2, nhóm IIIA
C tinh thể cấu tạo lập phương tâm diện
D cấu hình e rút gọn: [Ne] 3s2 3p1
Câu 8: Dung dịch FeSO4 có lẫn CuSO4. Để loại bỏ tạp chất có thể dùng một lượng dư
A Al B Cu C Ag D Fe
Câu 9: Sục khí CO2 dư vào dung dịch muối X thu được kết tủa trắng. Nhỏ từ từ dung dịch HCl vào dung dịch muối X đặc dư, thấy xuất hiện kết tủa trắng sau đó kết tủa tan dần. Muối X là
A C6H5ONa B BaCl2 C NaAlO2 D AlCl3
Câu 10: Cho Na vào 300ml dung dịch AlCl3. Khi phản ứng kết thúc thu được 5,6 lít khí H2 (đktc), dung dịch A và kết tủa B. Lọc lấy kết tủa đem nung đến khối lượng không đổi thu được 5,1 gam chất rắn D. Nồng độ mol của dung dịch AlCl3 là
A 0,8 M B 0.5 M C 0,4 M D 0,6 M
Câu 11: Cho 6 gam kim loại kiềm thổ tác dụng hết với nước thu được 12,22 lít khí (ở 250C; 0,5atm). Kim loại kiềm thổ đã dùng là
A Mg B Sr C Ba D Ca
Câu 12: Phát biểu sai là: Fe có khả năng tan trong dung dịch
A FeCl3 B AgNO3 C FeCl2 D CuSO4
Câu 13: Phương trình hóa học viết sai là
A Fe + Cl2 → FeCl2
B 3Fe + 2O2 → Fe3O4
C Fe (dư) + 2AgNO3 → Fe(NO3)2 + 2Ag
D Fe + 2HCl → FeCl2 + H2
Câu 14: Cho a mol NaAlO2 tác dụng với dung dịch có chứa b mol HCl. Điều kiện của a và b để xuất hiện kết tủa là
A b 4a B b> 4a C b = 4a D b < 4a
Câu 15: Cho 7.8gam kim loại kiềm M tác dụng với lượng nước (dư) sinh ra 2,24 lít H2 (đktc). Kim loại M là
A Ba B Na C Ca D K
Câu 16: Phản ứng giữa Al(OH)3 với dung dịch xút thuộc loại phản ứng
A phân hủy B oxi hóa - khử C axit - bazơ D thế
Câu 17: Để bảo quản dung dịch Fe2(SO4)3, tránh hiện tượng thủy phân người ta thường nhỏ vào ít giọt dung dịch
A NH3.
B H2SO4.
C BaCl2.
D NaOH.
Câu 18: Cho sơ đồ chuyển hóaH2 (A) KAlO2 (B) (C) (A). Các chất A, B, C lần lượt là
A K, Al(OH)3, Al2O3
B Al, KHCO3, Al2O3
C Al2O3, Al(OH)3, Al
D Al, Al(OH)3, Al2O3
Câu 19: Cho 33.9 gam hỗn hợp bột nhôm oxit và nhôm tác dụng vừa đủ với 675 ml dung dịch HCl 4M. Khối lượng nhôm trong hỗn hợp ban đầu là
A 6,75 gam B 10,20 gam. C 11,85 gam. D 13,5gam
Câu 20: Dẫn 8,96 lít khí CO2 (đktc) vào 350 ml dung dịch Ca(OH)2 1M. Khối lượng kết tủa thu được là
A 15 gam. B 30 gam. C 20 gam. D 25 gam.
Câu 21: Cho phản ứng Fe + Cu2+ → Fe2+ + Cu. Nhận xét không đúng là
A ion Fe2+ oxi hóa được kim loại Cu.
B kim loại Fe khử được ion Cu2+
C tính oxi hóa của ion Fe2+ yếu hơn ion Cu2+
D kim loại Fe có tính khử mạnh hơn kim loại Cu.
Câu 22: Cho hỗn hợp kim loại gồm Na và Al vào nước, thu được dung dịch và 4,48 lít khí (đktc), 2.7 gam chất rắn. Khối lượng của Na và Al tương ứng là
A 7,8 gam và 5,4 gam B 2.3 gam và 5,4 gam C 3,9 gam và 8,1 gam D 15,6 gam và 5,4 gam
Câu 23: Chất nào sau đây không có tính lưỡng tính?
A NaHCO3 B Al(OH)3 C ZnSO4 D Al2O3
Câu 24: Oxi hóa 11,2 gam Fe bằng oxi được m gam hỗn hợp Y gồm Fe, FeO, Fe3O4, Fe2O3. Y tan hết trong HNO3 dư, sinh ra 0,06 mol NO (sản phẩm khử duy nhất). Giá trị của m là
A 7,56 B 6,56 C 5,66 D 14,56
Câu 25: Khử hoàn toàn m gam hỗn hợp X gồm FeO và Fe2O3 bằng H2 (t0), kết thúc thí nghiệm thu được 12,6 gam nước và 28 gam Fe. Phần trăm khối lượng FeO có trong X là
A 47,4%. B 18,4% C 27,8%. D 52,6%.
Câu 26: Để bảo quản kim loại kiềm, người ta
A ngâm chìm trong dầu hoả. B ngâm chìm vào dung dịch NaOH C cho vào lọ đậy kín. D ngâm chìm trong dung dịch muối ăn.
Câu 27: Cho Na vào dung dịch CuSO4 dư, dung dịch thu được sau phản ứng chứa các chất tan là
A Na2SO4, CuSO4, Cu(OH)2
B Na2SO4, Cu(OH)2
C Na2SO4, CuSO4.
D Na2SO4, CuSO4, NaOH
Câu 28: Cho luồng khí CO dư đi qua ống sứ chứa hỗn hợp các chất sau: CaO, Al2O3, Fe2O3, CuO, nung nóng. Chất rắn còn lại trong ống sứ gồm
A Al, CaCO3, Fe, Cu. B Al2O3, Fe, Cu, CaO. C CaCO3, Al2O3, Fe, Cu. D Al2O3, Cu, Fe2O3, CaO.
Câu 29: Khi điện phân dung dịch NaCl, ở anot xảy ra
A sự khử Cl- B sự oxi hoá H2O C sự khử H2O D sự oxi hóa Cl-
Câu 30: X là hỗn hợp Al(OH)3, Ag2O, Cu(OH)2 và Zn(OH)2. Để tách Al(OH)3 ra khỏi hỗn hợp X, người ta cho X vào dung dịch
A HCl dư, sau đó cho dung dịch NaOH dư vào thì Al(OH)3 tách ra.
B NaOH dư, sau đó cho dung dịch NH3 vừa đủ vào thì Al(OH)3 tách ra
C NH3 dư, Al(OH)3 không tan tách ra
D HCl dư, sau đó trung hòa axit dư băng dung dịch kiềm thì Al(OH)3 tách ra.
ĐÁP ÁN ĐỀ THI SỐ 1
1. C 2. B 3. A 4. A 5. A 6. C 7. B 8. D 9. C 10. B
11. A 12. C 13. A 14. D 15. D 16. C 17. B 18. D 19. D 20. B
21. A 22. B 23. C 24. D 25. B 26. A 27. C 28. C 29. D 30. A
ĐỀ THI SỐ 2
ĐỀ THI GIỮA HK2 MÔN HÓA HỌC 12 NĂM 2022 TRƯỜNG THPT LƯƠNG VĂN CAN - ĐỀ SỐ 2
I. Phần trắc nghiệm
Câu 1: Phản ứng hóa học nào không xảy ra khi thực hiện quá trình luyện gang trong lò cao?
A. C + O2 → CO2.
B. C + 2O2 → 2CO.
C. 2C + O2 → 2CO.
D. Cả A và C.
Câu 2: Phát biểu nào dưới đây là đúng?
A. Nhôm là một kim loại lưỡng tính.
B. Al2O3 là một oxit trung tính.
C. Al(OH)3 là một bazơ lưỡng tính.
D. Al(OH)3 là một hiđroxit lưỡng tính.
Câu 3: Tính chất nào sau đây là tính chất chung của các hợp chất: FeO, Fe2O3, Fe(OH)2, Fe(OH)3?
A. Tính khử.
B. Tính oxi hoá.
C. Tính bazơ
D. Tính axit.
Câu 4: Cho 32,04 gam AlCl3 vào 500 ml dung dịch NaOH 1,6M sau khi phản ứng xong thu được thu được bao nhiêu gam kết tủa?
A. 12,48 gam.
B. 4,68 gam.
C. 18,72gam.
D. 6,24 gam.
Câu 5: Nhôm không tan trong dung dịch nào dưới đây?
A. HCl.
B. H2SO4.
C. KHSO4.
D. NH3.
Câu 6: Quặng manđehit chứa
A. Fe2O2.
B. Fe2O3.nH2O.
C. Fe3O4.
D. FeCO3.
Câu 7: Crom không tan được trong dung dịch
A. H2SO4 đặc, nguội.
B. HBr đặc, nguội.
C. HCl đặc.
D. HNO3 đặc, nóng.
Câu 8: Biết cấu hình của Fe là: 1s22s22p63s23p63d64s2. Vị trí của Fe trong bảng tuần hoàn là
A. Ô: 26, chu kì: 4, nhóm VIIIB.
B. Ô: 25, chu kì: 3, nhóm IIB.
C. Ô: 26, chu kì: 4, nhóm IIA.
D. Ô: 20, chu kì: 3, nhóm VIIIA.
Câu 9: Các số oxi hoá đặc trưng của Crom trong hợp chất là
A. +1, +2, +4, +6.
B. +3, +4, +6.
C. +2, +4, +6.
D. +2, + 3, +6.
Câu 10: Khử hoàn toàn 16g bột oxit sắt nguyên chất bằng CO ở nhiệt độ cao. Sau khi phản ứng kết thúc, khối lượng chất rắn giảm 4,8g. Oxit sắt đã dùng là
A. Fe2O
B. Fe2O3
C. FeO
D. Fe3O4
II. Phần tự luận
Câu 1 (3 điểm): Hoàn thiện các PTHH xảy ra trong sơ đồ sau:
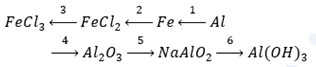
Câu 2 (2 điểm): Cho 1,56 gam hỗn hợp gồm Al và Al2O3 phản ứng hết với dung dịch HCl (dư), thu được V lít khí H2 (đktc) và dung dịch X. Nhỏ từ từ dung dịch NH3 đến dư vào dung dịch X thu được kết tủa, lọc hết lượng kết tủa, nung đến khối lượng không đổi thu được 2,04 gam chất rắn. Viết các PTHH xảy ra và tính giá trị của V.
Câu 3 (2 điểm): Nung nóng m gam hỗn hợp Al và Fe2O3 (trong môi trường không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau:
- Phần 1 tác dụng với dung dịch H2SO4 loãng (dư), sinh ra 3,08 lít khí H2 (ở đktc);
- Phần 2 tác dụng với dung dịch NaOH (dư), sinh ra 0,84 lít khí H2 (ở đktc).
Tính giá trị của m.
ĐÁP ÁN ĐỀ THI SỐ 2
1. Phần trắc nghiệm
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
C |
D |
C |
A |
D |
C |
A |
A |
D |
B |
---(Để xem tiếp nội dung phần còn lại của đề thi số 2 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐỀ THI SỐ 3
ĐỀ THI GIỮA HK2 MÔN HÓA HỌC 12 NĂM 2022 TRƯỜNG THPT LƯƠNG VĂN CAN - ĐỀ SỐ 3
Câu 1: Cho 4,291 gam hỗn hợp A gồm Fe3O4 , Al2O3 và CuO tác dụng vừa đủ với 179 ml dung dịch HCl 1M. Cô cạn dung dịch thu được khối lượng muối khan là
A. 9,2135 gam B. 9,1415 gam C. 9,5125 gam D. 9,3545 gam
Câu 2: Kim loại nào sau đây có độ cứng lớn nhất trong tất cả các kim loại?
A. Đồng. B. Crom. C. Vonfam. D. Sắt.
Câu 3: Một dung dịch hỗn hợp chứa a mol NaAlO2 và a mol NaOH tác dụng với một dung dịch chứa b mol HCl. Điều kiện để thu được kết tủa sau phản ứng là
A. a < b < 5a. B. a = b. C. b = 5a. D. a = 2b.
Câu 4: Khi dẫn từ từ khí CO2 đến dư vào dung dịch Ca(OH)2 thấy có
A. bọt khí và kết tủa trắng.
B. kết tủa trắng, sau đó kết tủa tan dần.
C. bọt khí bay ra.
D. kết tủa trắng xuất hiện.
Câu 5: Những kim loại nào sau đây có thể điều chế bằng phương pháp nhiệt luyện.
A. Na, Ca, Mg. B. Zn, Fe, Sn. C. Hg, Ag, Na. D. Al, Fe, Zn.
Câu 6: Hỗn hợp X gồm CuO, Fe, Al, Zn, Mg. Cho m gam hỗn hợp X tác dụng với oxi nung nóng, sau một thời gian thu được (m + 0,96) gam hỗn hợp rắn Y. Cho Y phản ứng với dung dịch HNO3 loãng (dư) thu được 7,168 lít NO (sản phẩm khử duy nhất, ở đktc) và dung dịch Z. Cô cạn Z được (m +73,44) gam chất rắn khan. Số mol HNO3 đã phản ứng là
A. 1,52. B. 1,64. C. 1,48. D. 1,4.
Câu 7: Cho các hydroxit: NaOH, Mg(OH)2, Fe(OH)3, Al(OH)3. Hidroxit có tính bazơ mạnh nhất là
A. Fe(OH)3. B. NaOH. C. Mg(OH)2. D. Al(OH)3.
Câu 8: Hoà tan m gam Fe trong dung dịch HCl dư, sau khi phản ứng kết thúc thu được 4,48 lít khí H2 (ở đktc). Giá trị của m là
A. 11,2. B. . 5,6. C. 2,8. D. 1,4.
Câu 9: Một muối khi tan vào nước tạo thành dung dịch có môi trường kiềm, muối đó là
A. MgCl2. B. KHSO4. C. Na2CO3. D. NaCl.
Câu 10: Cho phản ứng: a Fe + b H2SO4 (đặc) → c Fe2(SO4)3 + d SO2 + e H2O
Các hệ số a, b, c, d, e là những số nguyên, tối giản thì tổng (a + b) bằng
A. 4. B. 10. C. 8. D. 6.
---(Để xem tiếp nội dung từ câu 11 đến câu 30 của đề thi số 3 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ THI SỐ 3
|
1 |
A |
6 |
A |
11 |
B |
16 |
C |
21 |
D |
26 |
A |
|
2 |
B |
7 |
B |
12 |
B |
17 |
D |
22 |
D |
27 |
A |
|
3 |
A |
8 |
A |
13 |
A |
18 |
D |
23 |
C |
28 |
B |
|
4 |
B |
9 |
C |
14 |
C |
19 |
D |
24 |
A |
29 |
A |
|
5 |
B |
10 |
C |
15 |
C |
20 |
C |
25 |
C |
30 |
B |
ĐỀ THI SỐ 4
ĐỀ THI GIỮA HK2 MÔN HÓA HỌC 12 NĂM 2022 TRƯỜNG THPT LƯƠNG VĂN CAN - ĐỀ SỐ 4
Câu 1: Chất X là một bazơ mạnh, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất amoniac, clorua vôi, vật liệu xây dựng…. Công thức của X là
A. NaOH. B. KOH. C. Ca(OH)2. D. Ba(OH)2.
Câu 2: Nước cứng gây ra nhiều tác hại trong đời sống cũng như trong sản xuất. Để làm mềm một loại nước cứng có tính cứng toàn phần, ta có thể dùng
A. Ca(OH)2. B. NaOH. C. HCl. D. Na2CO3.
Câu 3: Cho các kim loại: Ca, Fe, Cu, Ag, Cr, Zn. Số kim loại tác dụng được với dung dịch HCl là
A. 2. B. 3. C. 5. D. 4.
Câu 4: Phèn chua là một chất có nhiều ứng dụng quan trọng trong ngành thuộc da, công nghiệp giấy, chất cầm màu trong ngành nhuộm vải, chất làm trong nước…. Công thức hóa học của phèn chua là
A. K2SO4.Al2(SO4)3.24H2O.
B. (NH4)2SO4.Al2(SO4)3.24H2O.
C. Na2SO4.Al2(SO4)3.24H2O.
D. Li2SO4.Al2(SO4)3.24H2O.
Câu 5: Sục từ từ cho đến dư khí CO2 vào dung dịch Ca(OH)2. Hiện tượng hóa học xảy ra là
A. Xuất hiện kết tủa trắng sau đó tan khi CO2 dư.
B. Xuất hiện kết tủa màu trắng xanh, sau đó chuyển sang nâu đỏ.
C. Xuất hiện kết tủa trắng không tan khi CO2 dư.
D. Không hiện tượng do không có phản ứng xảy ra.
Câu 6: Trong số các cation kim loại: Fe2+, Fe3+, Cu2+, Ag+. Ion có tính oxi hóa mạnh nhất là
A. Fe2+. B. Cu2+. C. Fe3+. D. Ag+.
Câu 7: Nhiệt phân hoàn toàn 16,2 gam Ca(HCO3)2 thu được chất rắn có khối lượng là
A. 5,6 gam. B. 5 gam. C. 11,2 gam. D. 10 gam.
Câu 8: Cho 8,4 gam sắt tác dụng với dung dịch HNO3 đặc nóng dư, thể tích khí NO2 (sản phẩm khử duy nhất, ở đktc) thu được sau phản ứng là
A. 3,36 lít. B. 10,08 lít. C. 5,04 lít. D. 6,72 lít.
Câu 9: Cấu hình electron lớp ngoài cùng của các kim loại kiềm có dạng
A. ns2np1. B. ns1. C. ns2np5. D. ns2.
Câu 10: Kim loại cứng nhất là
A. Cr. B. W. C. Ag. D. Fe.
---(Để xem tiếp nội dung từ câu 11 đến câu 30 của đề thi số 4 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ THI SỐ 4
|
1 |
C |
11 |
C |
21 |
D |
|
2 |
D |
12 |
D |
22 |
B |
|
3 |
D |
13 |
B |
23 |
B |
|
4 |
A |
14 |
C |
24 |
D |
|
5 |
A |
15 |
B |
25 |
A |
|
6 |
D |
16 |
C |
26 |
C |
|
7 |
A |
17 |
D |
27 |
C |
|
8 |
B |
18 |
A |
28 |
A |
|
9 |
B |
19 |
B |
29 |
B |
|
10 |
A |
20 |
C |
30 |
A |
ĐỀ THI SỐ 5
ĐỀ THI GIỮA HK2 MÔN HÓA HỌC 12 NĂM 2022 TRƯỜNG THPT LƯƠNG VĂN CAN - ĐỀ SỐ 5
Câu 1: Cho hỗn hợp gồm 8,4 gam sắt và 3,6 gam Mg tác dụng với dung dịch H2SO4 loãng dư, thể tích khí (ở đktc) thu được sau phản ứng là
A. 6,72 lít. B. 10,08 lít. C. 8,96 lít. D. 8,4 lít.
Câu 2: Điện phân dung dịch CuSO4 nồng độ 0,5M với điện cực trơ trong thì thu được 1gam Cu. Nếu dùng dòng điện một chiều có cường độ 1A, thì thời gian điện phân tối thiểu có giá trị gần nhất là
A. 40 phút 45 giây. B. 40 phút 15 giây. C. 50 phút 15 giây. D. 50 phút 45 giây.
Câu 3: Cho 25 gam hỗn hợp bột gồm 5 oxit kim loại ZnO, FeO, Fe3O4, MgO, Fe2O3 tác dụng vừa đủ với 200 ml dung dịch HCl 2M. Kết thúc phản ứng, khối lượng muối có trong dung dịch X là
A. 36,0 gam. B. 39,6 gam. C. 38,0 gam. D. 39,2 gam.
Câu 4: Tiến hành bốn thí nghiệm sau:
- Thí nghiệm 1: Nhúng thanh Fe vào dung dịch FeCl3;
- Thí nghiệm 2: Nhúng thanh Fe vào dung dịch CuSO4;
- Thí nghiệm 3: Nhúng thanh Cu vào dung dịch FeCl3;
- Thí nghiệm 4: Cho thanh Fe tiếp xúc với thanh Cu rồi nhúng vào dung dịch HCl.
Số trường hợp xuất hiện ăn mòn điện hoá là
A. 1. B. 4. C. 2. D. 3.
Câu 5: Cho các chất: Al, AlCl3, Al2O3, Al(OH)3. Số chất có tính lưỡng tính là
A. 3. B. 2. C. 4. D. 1.
Câu 6: Có các kim loại Cu, Ag, Fe, Al, Au. Độ dẫn điện của chúng giảm dần theo thứ tự
A. Ag, Cu, Au, Al, Fe. B. Au, Ag, Cu, Al, Fe.
C. Ag, Au, Cu, Fe, Al. D. Ag, Cu, Fe, Al, Au.
Câu 7: Hiện tượng nào dưới đây được mô tả không đúng?
A. Cho bột Cu vào dung dịch FeCl3 màu vàng nâu, màu của dung dịch chuyển dần sang màu xanh.
B. Thêm NaOH vào dung dịch FeCl3 màu vàng nâu thấy xuất hiện kết tủa trắng xanh.
C. Cho bột sắt vào dung dịch FeCl3 thấy màu vàng nâu của dung dịch bị nhạt dần.
D. Cho CO2 đến vào dung dịch Ca(OH)2 thấy có kết tủa sau đó tan khi CO2 dư.
Câu 8: Dãy các ion xếp theo chiều giảm dần tính oxi hoá là
A. Ag+, Cu2+, Fe3+, Fe2+. B. Fe3+, Cu2+, Ag+, Fe2+.
C. Ag+, Fe3+, Cu2+, Fe2+. D. Fe3+, Ag+, Cu2+, Fe2+.
Câu 9: Sắt (Fe) ở ô số 26 của bảng tuần hoàn các nguyên tố hóa học. Cấu hình electron của ion Fe2+ là
A. [Ar] 3d54s1. B. [Ar]3d6. C. [Ar]3d64s2. D. [Ar] 3d44s2.
Câu 10: Cho các chất và ion sau: Fe; FeSO4; FeO; Fe3O4; Fe(NO3)3; FeCl2; Fe2+; Fe3+. Số lượng chất và ion có khả năng vừa đóng vai trò chất khử, vừa đóng vai trò chất oxi hóa là
A. 5. B. 4. C. 6. D. 3.
---(Để xem tiếp nội dung từ câu 11 đến câu 30 của đề thi số 5 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ THI SỐ 5
|
1 |
A |
6 |
A |
11 |
B |
16 |
A |
21 |
C |
26 |
B |
|
2 |
C |
7 |
B |
12 |
B |
17 |
A |
22 |
C |
27 |
D |
|
3 |
A |
8 |
C |
13 |
B |
18 |
B |
23 |
C |
28 |
B |
|
4 |
C |
9 |
B |
14 |
C |
19 |
C |
24 |
D |
29 |
C |
|
5 |
B |
10 |
C |
15 |
B |
20 |
D |
25 |
C |
30 |
C |
Trên đây là trích dẫn một phần nội dung Bộ 5 đề thi giữa HK2 môn Hóa học 12 năm 2021-2022 có đáp án Trường THPT Lương Văn Can. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Ngoài ra các em có thể tham khảo thêm một số tư liệu cùng chuyên mục tại đây:
Thi Online:
Chúc các em học tốt!













