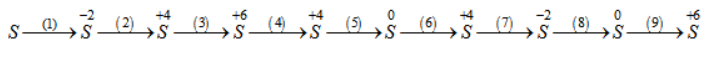Bài tập 30.7 trang 67 SBT Hóa học 10
Viết phương trình hoá học của các phản ứng hoàn thành chuỗi phản ứng sau :
Hướng dẫn giải chi tiết bài 30.7
(1) S + H2 to → H2S
(2) 2H2S + 3O2 to → 2SO2 + 2H2O
(3) SO2 + Br2 + 2H2O to → H2SO4 + 2HBr
(4) Cu + H2SO4 đặc nóng → CuSO4 + SO2 + 2H2O
(5) SO2 + 2Mg → S + 2MgO
(6) S + O2 to → SO2
(7) SO2 + 6HI → H2S + 3I2 + 2H2O
(8) H2S + Cl2 → S + 2HCl
(9) S + 6HNO3 đặc nóng → H2SO4 + 6NO2 + 2H2O
-- Mod Hóa Học 10 HỌC247
-


Lí do nước ở ao hồ thường bị đen?
bởi Aser Aser
 01/02/2021
Theo dõi (0) 1 Trả lời
01/02/2021
Theo dõi (0) 1 Trả lời -


Lí do nào S dùng để thu hồi thủy ngân?
bởi can tu
 01/02/2021
Theo dõi (0) 1 Trả lời
01/02/2021
Theo dõi (0) 1 Trả lời -


Cho các oxit: \(S{O_2};{\text{ }}N{O_2};{\text{ }}Cr{O_3};{\text{ }}C{O_2};\,\,CO;\,\,NO;{\text{ }}{P_2}{O_5};{\text{ }}{N_2}{O_5};{\text{ }}S{O_3}\).Số oxit trong dãy tác dụng được với nước ở điều kiện thường là:
bởi Đan Nguyên
 29/01/2021
29/01/2021
A. 6
B. 4
C. 7
D. 5
Theo dõi (0) 1 Trả lời -


Hòa tan hoàn toàn 9,75 gam Zn trong lượng dư dung dịch \(HNO_3\) đặc, nóng. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và V lít \(NO_2\) (sản phẩm khử duy nhất, đktc). Giá trị của V là
bởi bach hao
 28/01/2021
28/01/2021
A.4,48.
B. 2,24.
C. 3,36.
D. 6,72.
Theo dõi (0) 1 Trả lời -


Trong số các dung dịch \(Cu{(N{O_3})_2};{\text{ }}Fe{(N{O_3})_3};{\text{ }}AgN{O_3};{\text{ }}Pb{(N{O_3})_2};Zn{\left( {N{O_3}} \right)_2};{\text{ }}FeC{l_2}\). Số dung dịch phản ứng được với \(H_2S\) là:
bởi Phạm Hoàng Thị Trà Giang
 29/01/2021
29/01/2021
A.6
B.5
C.3
D.4
Theo dõi (0) 1 Trả lời -


Hơi thủy ngân rất độc , vì vậy khí vỡ nhiệt kế , chất bột được rắc lên thủy ngân và sau đó gom lại là:
bởi Huong Duong
 29/01/2021
29/01/2021
A.Cát
B.Lưu huỳnh
C. muối ăn
D.Vôi sống
Theo dõi (0) 1 Trả lời -


Nhận định nào sau đây đúng khi so sánh tính chất cơ bản của lưu huỳnh và oxi:
bởi Tram Anh
 21/01/2021
21/01/2021
A. tính oxi hóa của lưu huỳnh < oxi
B. tính oxi hóa của lưu huỳnh > oxi
C. tính oxi hóa của lưu huỳnh và oxi bằng nhau
D. tính khử của oxi và lưu huỳnh bằng nhau
Theo dõi (0) 1 Trả lời -


Tính chất vật lí nào sau đây không phải là tính chất vật lí đặc trưng của lưu huỳnh?
bởi Phạm Hoàng Thị Trà Giang
 22/01/2021
22/01/2021
A. chất rắn màu vàng.
B. không tan trong nước.
C. có nhiệt độ nóng chảy thấp hơn nhiệt độ sôi của nước.
D. tan nhiều trong benzen.
Theo dõi (0) 1 Trả lời -


S + 2H2SO4 đặc → 3SO2 + 2H2O
Tỉ lệ số nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hoá là:
A. 1 : 2.
B. 1 : 1.
C. 3 : 2.
D. 2 : 1.
Theo dõi (0) 1 Trả lời
Bài tập SGK khác
Bài tập 30.5 trang 67 SBT Hóa học 10
Bài tập 30.6 trang 67 SBT Hóa học 10
Bài tập 30.8 trang 67 SBT Hóa học 10
Bài tập 30.9 trang 67 SBT Hóa học 10
Bài tập 30.10 trang 68 SBT Hóa học 10
Bài tập 30.11 trang 68 SBT Hóa học 10
Bài tập 1 trang 172 SGK Hóa học 10 nâng cao
Bài tập 2 trang 172 SGK Hóa học 10 nâng cao