Mời quý thầy cô cùng các em học sinh tham khảo tài liệu Bộ 5 đề thi thử THPT QG môn Hóa học năm 2021-2022 Trường THPT Tam Dương. Đề thi gồm các câu trắc nghiệm có đáp án hướng dẫn giải chi tiết hy vọng sẽ giúp các em học sinh ôn tập hiệu quả và đạt điểm số cao trong các kì thi sắp tới.
|
TRƯỜNG THPT TAM DƯƠNG |
ĐỀ THI THỬ THPT QUỐC GIA MÔN HÓA HỌC NĂM HỌC 2021-2022 Thời gian làm bài 50 phút |
ĐỀ THI SỐ 1
Câu 1: Hai chất hữu cơ X, Y là đồng phân của nhau và có công thức phân tử là C3H7O2N. X tác dụng với NaOH thu được muối X1 có công thức phân tử là C2H4O2NNa; Y tác dụng với NaOH thu được muối Y1 có công thức phân tử là C3H3O2Na. Công thức cấu tạo của X, Y là:
A. X là CH3-COOH3N-CH3 và Y là CH2=CH-COONH4.
B. X là H2N-CH2-COOCH3 và Y là CH2=CH-COONH4.
C. X là H2N-CH2-COOCH3 và Y là CH3-CH2COONH4.
D. X là CH3-CH(NH2)-COOH và Y là CH2=CH-COONH4.
Câu 2: Nhỏ từ từ dung dịch H2SO4 loãng vào dung dịch K2CrO4 thì màu của dung dịch chuyển từ
A. màu da cam sang màu vàng.
B. không màu sang màu da cam.
C. không màu sang màu vàng.
D. màu vàng sang màu da cam.
Câu 3: Cho dung dịch AgNO3 tác dụng với dung dịch chứa chất X thấy tạo kết tủa T màu vàng. Cho kết tủa T tác dụng với dung dịch HNO3 dư thấy kết tủa tan. Chất X là
A. K3PO4. B. KBr. C. KI. D. KCl.
Câu 4: Nguyên tắc chung để điều chế kim loại là
A. Oxi hóa các cation kim loại.
B. Oxi hóa các kim loại.
C. Khử các cation kim loại.
D. Khử các kim loại.
Câu 5: Este X khi tác dụng với dung dịch NaOH thu được 2 muối là natri phenolat và natri propionat. X có công thức là
A. C6H5OOCCH3.
B. C6H5COOCH2CH3.
C. CH3COOC6H5.
D. CH3CH2COOC6H5.
Câu 6: Cho dãy các chất: glucozơ, xenlulozơ, etyl fomat, metylamin. Số chất trong dãy có thể tham gia phản ứng tráng gương là
A. 2. B. 1. C. 3. D. 4.
Câu 7: Bảng dưới đây ghi lại hiện tượng khi làm thí nghiệm với các chất sau ở dạng dung dịch nước: X, Y, Z, T và Q
|
|
X |
Y |
Z |
T |
Q |
|
Quỳ tím |
không đổi màu |
không đổi màu |
không đổi màu |
không đổi màu |
không đổi màu |
|
Dung dịch AgNO3/NH3, đun nhẹ |
không có kết tủa |
Ag |
không có kết tủa |
không có kết tủa |
Ag |
|
Cu(OH)2, lắc nhẹ |
Cu(OH)2 không tan |
dung dịch xanh lam |
dung dịch xanh lam |
Cu(OH)2 không tan |
Cu(OH)2 không tan |
|
Nước brom |
Kết tủa trắng |
không có kết tủa |
không có kết tủa |
không có kết tủa |
không có kết tủa |
Các chất X, Y, Z, T và Q lần lượt là
A. Glixerol, glucozơ, etylen glicol, metanol, axetanđehit.
B. Phenol, glucozơ, glixerol, etanol, anđehit fomic.
C. Anilin, glucozơ, glixerol, anđehit fomic, metanol.
D. Fructozơ, glucozơ, axetanđehit, etanol, anđehit fomic.
Câu 8: Cho dãy các chất: glucozơ, saccarozơ, xenlulozơ, tinh bột. Số chất trong dãy không tham gia phản ứng thủy phân là
A. 2. B. 1. C. 3. D. 4.
Câu 9: Phương trình hóa học nào sau đây là sai?
A. 2NaOH + Cl2 \(\to \) NaCl + NaClO + H2O.
B. Fe3O4 + 8HCl \(\to \) FeCl2 + 2FeCl3 + 4H2O.
C. Cu + H2SO4 \(\xrightarrow{{}}\)CuSO4 + H2.
D. 4FeCO3 + O2 \(\xrightarrow{{{t}^{0}}}\)2Fe2O3 + 4CO2.
Câu 10: Hòa tan m gam hỗn hợp gồm Al, Fe vào dung dịch H2SO4 loãng (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X. Cho dung dịch Ba(OH)2 (dư) vào dung dịch X, thu được kết tủa Y. Nung Y trong không khí đến khối lượng không đổi, thu được chất rắn Z là
A. hỗn hợp gồm Al2O3 và Fe2O3.
B. Fe2O3.
C. hỗn hợp gồm BaSO4 và FeO.
D. hỗn hợp gồm BaSO4 và Fe2O3.
Câu 11: Cách bảo quản thực phẩm (thịt, cá…) bằng cách nào sau đây được coi là an toàn?
A. Dùng nước đá và nước đá khô.
B. Dùng nước đá khô, fomon.
C. Dùng fomon, nước đá.
D. Dùng phân đạm, nước đá.
Câu 12: Cho dãy các oxit: MgO, FeO, CrO3, Cr2O3. Số oxit lưỡng tính trong dãy là
A. 4. B. 1. C. 3. D. 2.
Câu 13: Cho các dung dịch: HCl, NaOH, HNO3 loãng, CuSO4. Fe không tác dụng được với dung dịch nào?
A. HNO3 loãng. B. NaOH. C. CuSO4. D. HCl.
Câu 14: Dung dịch AlCl3 không tác dụng với
A. dung dịch NH3. B. dung dịch AgNO3. C. dung dịch HNO3. D. dung dịch KOH.
Câu 15: Tính chất vật lý nào sau đây của kim loại không phải do các electron tự do gây ra?
A. Ánh kim. B. Tính dẫn điện và nhiệt.
C. Tính dẻo. D. Tính cứng.
Câu 16: Dung dịch của hợp chất nào sau đây không làm đổi màu giấy quì ẩm?
A. H2NCH2COOH. B. C2H5NH2.
C. CH3NH2. D. H2N-CH2-CH(NH2)COOH.
Câu 17: Nước cứng vĩnh cửu có chứa các ion
A. K+; Na+; \(C{{O}_{3}}^{2-}\); \(HC{{O}_{3}}^{-}\).
B. Mg2+; Na+; \(HC{{O}_{3}}^{-}\) .
C. Mg2+; Ca2+; \(HC{{O}_{3}}^{-}\) .
D. Mg2+; Ca2+; \(S{{O}_{4}}^{2-}\).
Câu 18: Một loại polime rất bền với nhiệt và axit, được tráng lên "chảo chống dính" là polime có tên gọi nào sau đây?
A. Plexiglas – poli(metyl metacrylat).
B. Poli(phenol – fomanđehit) (PPF).
C. Teflon – poli(tetrafloetilen).
D. Poli(vinyl clorua) (nhựa PVC).
Câu 19: Dãy ion được sắp xếp theo chiều giảm dần tính oxi hóa là
A. Ag+, Fe3+, H+, Cu2+, Fe2+, Zn2+.
B. Zn2+, Fe2+, H+, Cu2+, Fe3+, Ag+.
C. Fe3+, Ag+, Fe2+, H+, Cu2+, Zn2+.
D. Ag+, Fe3+, Cu2+, H+, Fe2+, Zn2+ .
Câu 20: Chọn nhận xét đúng:
A. Xenlulozơ có cấu trúc mạch phân nhánh.
B. Tất cả các peptit và protein đều có phản ứng màu biure với Cu(OH)2.
C. Xà phòng là muối của natri hoặc kali với axit béo.
D. Este chỉ được tạo ra khi cho axit cacboxylic phản ứng với ancol.
Câu 21: Phát biểu nào sau đây là đúng?
A. Ở điều kiện thường, tất cả các kim loại đều ở trạng thái rắn.
B. Tính chất hóa học đặc trưng của kim loại là tính khử.
C. Ở điều kiện thường, các kim loại đều có khối lượng riêng lớn hơn khối lượng riêng của nước.
D. Các kim loại đều chỉ có một số oxi hoá duy nhất trong các hợp chất.
Câu 22: Có bốn thanh sắt được đặt tiếp xúc với những kim loại khác nhau và nhúng trong các dung dịch HCl như hình vẽ dưới đây:
.jpg?enablejsapi=1)
Thanh sắt bị hòa tan nhanh nhất sẽ là thanh được đặt tiếp xúc với
A. Cu. B. Zn. C. Sn. D. Ni.
Câu 23: Để điều chế 26,73 kg xenlulozơ trinitrat (hiệu suất 60%) cần dùng ít nhất V lít axit nitric 65% (d = 1,5 g/ml) phản ứng với xenlulozơ dư. V gần nhất với giá trị nào sau đây?
A. 20. B. 29. C. 18. D. 30.
Câu 24: Hợp chất X có công thức phân tử C5H8O2. Cho 5 gam X tác dụng vừa đủ với dung dịch NaOH, thu được dung dịch Y. Lấy toàn bộ Y tác dụng hoàn toàn với dung dịch AgNO3/NH3 đun nóng, thu được 10,8 gam Ag. Số đồng phân cấu tạo của X là
A. 7. B. 8. C. 6. D. 2.
Câu 25: Dẫn V lít khí CO (đktc) qua ống sứ nung nóng đựng lượng dư CuO. Sau khi phản ứng hoàn toàn, khối lượng chất rắn giảm 3,2 gam. Giá trị của V là
A. 2,24. B. 3,36. C. 5,60. D. 4,48.
Câu 26: Thuỷ phân hoàn toàn glixerol trifomiat trong 200 gam dung dịch NaOH cô cạn dung dịch hỗn hợp sau phản ứng thu được 28,4 gam chất rắn khan và 9,2 gam ancol. Xác định nồng độ phần trăm của dung dịch NaOH?
A. 10%. B. 8%. C. 12%. D. 14%.
Câu 27: Amino axit X có công thức (H2N)2C3H5COOH. Cho 0,02 mol X tác dụng với 200 ml dung dịch hỗn hợp H2SO4 0,1M và HCl 0,3M, thu được dung dịch Y. Cho Y phản ứng vừa đủ với 400 ml dung dịch NaOH 0,1M và KOH 0,2M, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 6,38. B. 8,09. C. 10,43. D. 10,45.
Câu 28: Thổi khí CO2 vào dung dịch chứa 0,02 mol Ba(OH)2, thu được m gam kết tủa. Biết số \(0,005\le {{n}_{C{{O}_{2}}}}\le 0,024.\) Giá trị của m là
A. \(0
B. \(0
Câu 29: Đốt cháy hoàn toàn hỗn hợp amin no, đơn chức, mạch hở, thu được CO2, H2O và N2. Với \(T=\frac{{{n}_{C{{O}_{2}}}}}{{{n}_{{{H}_{2}}O}}}\) thì T nằm trong khoảng nào sau đây ?
A. \(0,4\le T\le 1.\)
B. \(0,5\le T<1.\)
C. \(0,5\le T\le 1.\)
D. 0,4
Câu 30: Hoà tan hoàn toàn một lượng hỗn hợp X gồm Fe3O4 và FeS2 trong 63 gam dung dịch HNO3, thu được 1,568 lít NO2 (đktc). Dung dịch thu được (Y) cho tác dụng vừa đủ với 200 ml dung dịch NaOH 2M, lọc kết tủa đem nung đến khối lượng không đổi thu được 9,76 gam chất rắn. Nồng độ phần trăm của dung dịch HNO3 có giá trị là
A. 46,2%. B. 47,2%. C. 46,6%. D. 44,2%.
Câu 31: Cho sơ đồ phản ứng:
(a) X + H2O → Y
(b) Y + AgNO3 + NH3 + H2O → amoni gluconat + Ag + NH4NO3
(c) Y → E + Z
(d) Z + H2O → X + G
X, Y, Z lần lượt là:
A. Xenlulozơ, saccarozơ, cacbon đioxit.
B. Tinh bột, glucozơ, etanol.
C. Xenlulozơ, fructozơ, cacbon đioxit.
D. Tinh bột, glucozơ, cacbon đioxit.
Câu 32: Hòa tan 32,8 gam hỗn hợp X gồm Fe và Fe2O3 (có tỉ lệ mol là 3 : 1) vào V lít dung dịch HCl 1M. Sau khi kết thúc các phản ứng thấy còn lại 2,8 gam kim loại không tan. Giá trị của V là
A. 0,6. B. 1,2. C. 0,9. D. 1,1.
Câu 33: Khi nhỏ từ từ đến dư dung dịch NaOH vào dung dịch AlCl3, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
.jpg)
Tỉ lệ x : y là :
A. 7 : 8. B. 6 : 7. C. 5 : 4. D. 4 : 5.
Câu 34: Đốt cháy 3,2 gam este E đơn chức tạo bởi axit X và ancol Y, mạch hở được 3,584 lít CO2 (đktc) và 2,304 gam H2O. Nếu cho 15 gam E tác dụng với 200 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được 14,3 gam chất rắn khan. Vậy công thức của ancol Y là
A. CH2=CH-OH.
B. CH2=CH-CH2OH.
C. CH3CH2OH.
D. CH3OH.
Câu 35: Hợp chất X có công thức phân tử C6H8O6. X phản ứng với NaOH theo tỉ lệ mol 1 : 3 và phản ứng với AgNO3/NH3 theo tỉ lệ mol 1 : 6. X không phản ứng với NaHCO3. Có các kết luận sau:
(1) X có chứa liên kết ba đầu mạch.
(2) X có chứa nhóm chức axit cacboxylic.
(3) X có chứa nhóm chức este.
(4) X có nhóm chức anđehit.
(5) X là hợp chất đa chức.
Số kết luận đúng về X là
A. 1. B. 4. C. 2. D. 3.
Câu 36: Nung 15,6 gam Al(OH)3 ở nhiệt độ cao đến khối lượng không đổi, thu được m gam một oxit. Giá trị của m là
A. 10,2. B. 15,3. C. 20,4. D. 5,1.
Câu 37: Đốt cháy hoàn toàn 0,1 mol peptit X (X được tạo thành các amino axit chỉ chứa 1 nhóm –NH2 và 1 nhóm –COOH) cần 58,8 lít O2 (đktc) thu được 2,2 mol CO2 và 1,85 mol H2O. Nếu cho 0,1 mol X thủy phân hoàn toàn trong 500 ml dung dịch NaOH 2M thu được dung dịch Y, cô cạn Y thu được m gam chất rắn. Công thức chung của peptit và giá trị của m lần lượt là
A. CxHyO8N7 và 96,9 gam. B. CxHyO10N9 và 96,9 gam.
C. CxHyO10N9 và 92,9 gam. D. CxHyO9N8 và 92,9 gam.
Câu 38: Cho 0,5 mol hỗn hợp E chứa 2 este đều đơn chức, mạch hở tác dụng với dung dịch AgNO3/NH3 đun nóng, thu được 64,8 gam Ag. Mặt khác, đun nóng 37,92 gam hỗn hợp E trên với 320 ml dung dịch NaOH 2M rồi cô cạn dung dịch sau phản ứng thu được phần rắn Y và 20,64 gam hỗn hợp chứa 2 ancol no trong đó oxi chiếm 31,0% về khối lượng. Đốt cháy hết chất rắn Y thu được Na2CO3; x mol CO2; y mol H2O. Tỉ lệ x : y là
A. 4 : 3. B. 7 : 6. C. 14 : 9. D. 17 : 9.
Câu 39: Đốt cháy 16,96 gam hỗn hợp gồm Fe và Mg trong oxi một thời gian, thu được hỗn hợp rắn X. Hòa tan hết X trong 242 gam dung dịch HNO3 31,5%, thu được dung dịch Y chỉ chứa các muối có khối lượng 82,2 gam và 1,792 lít (đktc) hỗn hợp khí Z gồm N2O và NO có tỉ khối so với He bằng 10,125. Cho NaOH dư vào dung dịch Y, lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được 25,6 gam chất rắn khan. Nồng độ C% của Fe(NO3)3 trong Y có giá trị gần nhất với
A. 14%. B. 15%. C. 12%. D. 13%.
Câu 40: Cho 0,5 mol Mg và 0,2 mol Mg(NO3)2 vào bình kín không có oxi rồi nung ở nhiệt độ cao đến phản ứng hoàn toàn, thu được hỗn hợp chất rắn X. Hỗn hợp chất rắn X tác dụng với nhiều nhất 500 ml dung dịch Fe(NO3)3 có nồng độ aM. Giá trị của a là
A. 1,2. B. 0,4. C. 2. D. 0,667.
ĐỀ THI SỐ 2
ĐỀ THI THỬ THPT QG MÔN HÓA HỌC NĂM 2022 TRƯỜNG THPT TAM DƯƠNG - ĐỀ 02
Câu 1: Thứ tự một số cặp oxi hoá - khử trong dãy điện hoá như sau: Mg2+/Mg; Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+; Ag+/Ag. Dãy chỉ gồm các chất, ion tác dụng được với ion Fe3+ trong dung dịch là:
A. Mg, Cu, Cu2+. B. Mg, Fe2+, Ag. C. Mg, Fe, Cu. D. Fe, Cu, Ag+.
Câu 2: Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư;
(b) Sục khí Cl2 vào dung dịch FeCl2;
(c) Dẫn khí H2 dư qua bột CuO nung nóng;
(d) Cho Na vào dung dịch CuSO4 dư;
(e) Nhiệt phân AgNO3;
(g) Đốt FeS2 trong không khí;
(h) Điện phân dung dịch CuSO4 với điện cực trơ;
Sau khi kết thúc phản ứng, số thí nghiệm thu được kim loại là
A. 4. B. 3. C. 2. D. 5.
Câu 3: Nhận định nào sau đây là sai?
A. Thép có hàm lượng Fe cao hơn gang. B. Crom còn được dùng để mạ thép.
C. Gang và thép đều là hợp kim. D. Sắt là nguyên tố phổ biến nhất trong vỏ trái đất.
Câu 4: Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch nào sau đây?
A. Muối ăn. B. Cồn. C. Xút. D. Giấm ăn.
Câu 5: Phát biểu nào sau đây không đúng?
A. Cr2O3 là oxit lưỡng tính, không tan trong dung dịch axit loãng, kiềm loãng.
B. CrO3 tan dễ trong nước, tác dụng dễ dàng với dung dịch kiềm loãng.
C. Do Cr(OH)3 là hiđroxit lưỡng tính nên Cr tác dụng được với dung dịch NaOH đặc.
D. CrO là oxit bazơ, tan dễ dàng trong dung dịch axit.
Câu 6: Cho sơ đồ phản ứng sau: Al → X → Y → AlCl3. X, Y có thể lần lượt là cặp chất nào sau đây?
A. Al2(SO4)3, Al2O3.
B. Al(OH)3, Al(NO3)3.
C. Al2(SO4)3, Al(OH)3.
D. Al(OH)3, Al2O3.
Câu 7: Điện trở đặc trưng cho khả năng cản trở dòng điện. Điện trở càng lớn thì khả năng dẫn điện của kim loại càng giảm. Cho 4 kim loại X, Y, Z, T ngẫu nhiên tương ứng với Ag, Al, Fe, Cu. Cho bảng giá trị điện trở của các kim loại như sau:
|
Kim loại |
X |
Y |
Z |
T |
|
Điện trở (Ωm) |
2,82.10-8 |
1,72.10-8 |
1,00.10-7 |
1,59.10-8 |
Y là kim loại nào trong các kim loại dưới đây?
A. Fe. B. Cu. C. Ag. D. Al.
Câu 8: Tính bazơ của các hiđroxit được xếp theo thứ tự giảm dần từ trái sang phải là
A. NaOH, Al(OH)3, Mg(OH)2.
B. NaOH, Mg(OH)2, Al(OH)3.
C. Mg(OH)2, NaOH, Al(OH)3.
D. Mg(OH)2, Al(OH)3, NaOH.
Câu 9: Dung dịch saccarozơ tinh khiết không có tính khử, nhưng khi đun nóng với H2SO4 loãng lại có phản ứng tráng gương, đó là do
A. đã có sự thủy phân saccarozơ tạo ra glucozơ và fructozơ chúng đều tráng gương được trong môi trường bazơ.
B. đã có sự tạo thành anđehit sau phản ứng.
C. Saccarozơ tráng gương được trong môi trường axit.
D. đã có sự thủy phân tạo chỉ tạo ra glucozơ.
Câu 10: Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Dung dịch I2 |
Có màu xanh tím |
|
Y |
Cu(OH)2 trong môi trường kiềm |
Có màu tím |
|
Z |
Dung dịch AgNO3 trong NH3, đun nóng dư, đun nóng |
Kết tủa Ag trắng sáng |
|
T |
Nước Br2 |
Kết tủa trắng |
Dung dịch X, Y, Z, T lần lượt là:
A. Hồ tinh bột, lòng trắng trứng, glucozơ, anilin.
B. Hồ tinh bột, anilin, lòng trắng trứng, glucozơ.
C. Hồ tinh bột, lòng trắng trứng, anilin, glucozơ.
D. Lòng trắng trứng, hồ tinh bột, glucozơ, anilin.
---(Để xem tiếp nội dung từ câu 11 đến câu 40 của đề thi số 2 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐỀ THI SỐ 3
ĐỀ THI THỬ THPT QG MÔN HÓA HỌC NĂM 2022 TRƯỜNG THPT TAM DƯƠNG - ĐỀ 03
Câu 1: Este nào sau đây có mùi dứa chín?
A. etyl isovalerat. B. etyl butirat. C. benzyl axetat. D. isoamyl axetat.
Câu 2: Cấu hình electron của ion X2+ là 1s²2s²2p63s²3p63d6. Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X thuộc
A. chu kì 4, nhóm VIIIB. B. chu kì 3, nhóm VIB.
C. chu kì 4, nhóm VIIIA. D. chu kì 4, nhóm IIA.
Câu 3: Kim loại M có các tính chất: nhẹ, bền trong không khí ở nhiệt độ thường; tan được trong dung dịch NaOH nhưng không tan trong dung dịch HNO3 đặc nguội và H2SO4 đặc nguội. Kim loại M là
A. Cr. B. Fe. C. Al. D. Zn.
Câu 4: Cho luồng khí H2 (dư) qua hỗn hợp các oxit CuO, Fe2O3, ZnO, MgO nung ở nhiệt độ cao. Sau phản ứng hỗn hợp rắn còn lại là:
A. Cu, Fe, Zn, Mg. B. Cu, Fe, ZnO, MgO.
C. Cu, FeO, ZnO, MgO. D. Cu, Fe, Zn, MgO.
Câu 5: Cho lòng trắng trứng vào Cu(OH)2 thấy xuất hiện màu
A. đen. B. tím. C. đỏ. D. vàng.
Câu 6: Dãy gồm các chất đều tác dụng với dung dịch NaOH là:
A. metyl axetat, glucozơ, etanol. B. metyl axetat, alanin, axit axetic.
C. etanol, fructozơ, metylamin. D. glixerol, glyxin, anilin.
Câu 7: Thực hiện một số thí nghiệm với 4 kim loại, thu được kết quả như sau:
|
|
X |
Y |
Z |
T |
|
Dung dịch NaOH |
có xảy ra phản ứng |
không xảy ra phản ứng |
không xảy ra phản ứng |
không xảy ra phản ứng |
|
Dung dịch HCl |
có xảy ra phản ứng |
không xảy ra phản ứng |
có xảy ra phản ứng |
không xảy ra phản ứng |
|
Dung dịch muối Fe(III) |
có xảy ra phản ứng |
có xảy ra phản ứng |
có xảy ra phản ứng |
không xảy ra phản ứng |
X, Y, Z, T lần lượt là:
A. Al, Fe, Cu, Ag. B. Al, Cu, Fe, Ag. C. Al, Ag, Fe, Cu. D. Al, Fe, Ag, Cu.
Câu 8: Chất tác dụng với H2 tạo thành sobitol là
A. xenlulozơ. B. tinh bột. C. glucozơ. D. saccarozơ.
Câu 9: Cho các dung dịch sau : NaHCO3, Na2S, Na2SO4, Fe(NO3)2, FeSO4, Fe(NO3)3 lần lượt vào dung dịch HCl. Số trường hợp có khí thoát ra là
A. 3. B. 2. C. 5. D. 4.
Câu 10: Điện phân dung dịch chứa HCl, NaCl, FeCl3 (điện cực trơ, có màng ngăn). Đồ thị nào sau đây biểu diễn đúng sự biến thiên pH của dung dịch theo thời gian (bỏ qua sự thuỷ phân của muối)?
A. .jpg)
B. .jpg)
C. 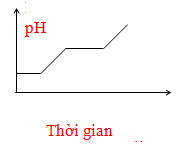
D. .jpg)
---(Để xem tiếp nội dung từ câu 11 đến câu 40 của đề thi số 3 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐỀ THI SỐ 4
ĐỀ THI THỬ THPT QG MÔN HÓA HỌC NĂM 2022 TRƯỜNG THPT TAM DƯƠNG - ĐỀ 04
Câu 1: Phương trình hóa học nào sau đây sai?
A. Cu + 2FeCl3 (dung dịch) \(\xrightarrow{{}}\) CuCl2 + 2FeCl2.
B. 2Na + 2H2O \(\xrightarrow{{}}\) 2NaOH + H2.
C. Fe + ZnSO4 (dung dịch) \(\xrightarrow{{}}\) FeSO4 + Zn.
D. H2 + CuO \(\xrightarrow{{{\text{t}}^{\text{o}}}}\) Cu + H2O.
Câu 2: Cho mô hình thí nghiệm điều chế và thu khí như hình vẽ sau:
.jpg)
Phương trình hóa học nào sau đây không phù hợp với hình vẽ trên?
A. NH4Cl + NaNO2 → NaCl + N2 + H2O.
B. CaCO3 + HCl → CaCl2 + CO2 + H2O.
C. Al4C3 + 12H2O→ 4Al(OH)3 + 3CH4.
D. CaC2 + H2O → Ca(OH)2 + C2H2.
Câu 3: Cho vào ống nghiệm một vài tinh thể K2Cr2O7, sau đó thêm tiếp khoảng 1 ml nước và lắc đều để K2Cr2O7 tan hết, thu được dung dịch X. Thêm vài giọt dung dịch KOH vào dung dịch X, thu được dung dịch Y. Màu sắc của dung dịch X và Y lần lượt là:
A. màu vàng chanh và màu da cam.
B. màu da cam và màu vàng chanh.
C. màu vàng chanh và màu nâu đỏ.
D. màu nâu đỏ và màu vàng chanh.
Câu 4: Cho sơ đồ chuyển hóa: Fe \(\xrightarrow{X}\) FeCl3 \(\xrightarrow{Y}\) Fe(OH)3
(mỗi mũi tên ứng với một phản ứng). Hai chất X, Y lần lượt là:
A. NaCl, Cu(OH)2.
B. HCl, Al(OH)3.
C. Cl2, NaOH.
D. HCl, NaOH.
Câu 5: Amino axit X no, mạch hở, có công thức CnHmO2N. Biểu thức liên hệ giữa m và n là
A. m = 2n + 3.
B. m = 2n + 1.
C. m = 2n + 2.
D. m = 2n.
Câu 6: Khi nhỏ từ từ dung dịch AlCl3 cho tới dư vào dung dịch NaOH và lắc đều thì
A. đầu tiên xuất hiện kết tủa trắng keo, sau đó kết tủa không tan lại.
B. đầu tiên không xuất hiện kết tủa, sau đó có kết tủa trắng keo.
C. đầu tiên xuất hiện kết tủa trắng keo, sau đó kết tủa tan lại.
D. không thấy kết tủa trắng keo xuất hiện.
Câu 7: Cho các dãy chuyển hóa: \(Glyxin\xrightarrow{NaOH}{{X}_{1}}\xrightarrow{HCl\,\,d\ddot{o}}{{X}_{2}}\)
X2 là :
A. H2NCH2COONa.
B. H2NCH2COOH.
C. ClH3NCH2COOH.
D. ClH3NCH2COONa
Câu 8: Phát biểu nào sau đây là đúng?
A. Saccarozơ có khả năng tham gia phản ứng tráng bạc.
B. Xenlulozơ tan tốt trong nước và etanol.
C. Hiđro hóa hoàn toàn glucozơ (xúc tác Ni, đun nóng) tạo ra sobitol.
D. Thủy phân hoàn toàn tinh bột trong dung dịch H2SO4 đun nóng, tạo ra fructozơ.
Câu 9: Dãy gồm các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3 đặc, nguội là:
A. Cu, Pb, Ag. B. Fe, Mg, Al. C. Cu, Fe, Al. D. Fe, Al, Cr.
---(Để xem tiếp nội dung từ câu 11 đến câu 40 của đề thi số 4 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐỀ THI SỐ 5
ĐỀ THI THỬ THPT QG MÔN HÓA HỌC NĂM 2022 TRƯỜNG THPT TAM DƯƠNG - ĐỀ 05
Câu 1: Cho các hợp kim sau: Cu – Fe (1); Zn – Fe (2); Fe – C (3); Sn – Fe (4). Khi tiếp xúc với dung dịch chất điện li thì các hợp kim mà trong đó Fe đều bị ăn mòn trước là:
A. (1), (2) và (3). B. (2), (3) và (4). C. (1), (3) và (4). D. 1, 2 và 4.
Câu 2: Nhỏ từ từ đến dư dung dịch NaOH loãng vào mỗi dung dịch sau: FeCl3, Ca(HCO3)2, CrCl3, AlCl3, MgSO4. Sau khi các phản ứng xảy ra hoàn toàn, số trường hợp thu được kết tủa là
A. 2. B. 4. C. 1. D. 3.
Câu 3: Cho hỗn hợp Fe, Cu phản ứng với dung dịch HNO3 loãng. Sau khi phản ứng hoàn toàn, thu được dung dịch chỉ chứa một chất tan và kim loại dư. Chất tan đó là
A. Fe(NO3)3. B. Cu(NO3)2. C. HNO3. D. Fe(NO3)2.
Câu 4: Một trong những nguyên nhân chính gây ra sự suy giảm tầng ozon là do
A. mưa axit.
B. quá trình sản xuất gang thép.
C. hợp chất CFC (freon).
D. sự tăng nồng độ khí CO2.
Câu 5: Phát biểu nào sau đây không đúng?
A. Cr2O3 là oxit lưỡng tính.
B. CrO3 tan dễ trong nước, tác dụng dễ dàng với dung dịch kiềm loãng.
C. Do Cr(OH)3 là hiđroxit lưỡng tính nên Cr tác dụng được với dung dịch NaOH đặc.
D. CrO là oxit bazơ, tan dễ dàng trong dung dịch axit.
Câu 6: Cho bột Al và dung dịch KOH dư thấy hiện tượng:
A. Sủi bọt khí, bột Al không tan hết và thu được dung dịch không màu.
B. Sủi bọt khí, Al không tan hết và dung dịch màu xanh lam.
C. Sủi bọt khí, bột Al tan dần đến hết và thu được dung dịch màu xanh lam.
D. Sủi bọt khí, Al tan dần đến hết và thu được dung dịch không màu.
Câu 7: Những tính chất vật lí chung của kim loại (tính dẫn điện, tính dẫn nhiệt, tính dẻo, ánh kim) được gây nên chủ yếu bởi
A. các electron tự do trong mạng tinh thể kim loại.
B. khối lượng riêng của kim loại.
C. tính chất của kim loại.
D. cấu tạo mạng tinh thể của kim loại.
Câu 8: Nguyên tử X có cấu hình electron 1s22s22p63s1. Vị trí của X trong bảng tuần hoàn các nguyên tố hóa học là:
A. Chu kỳ 3, nhóm IA là nguyên tố phi kim.
B. Chu kỳ 4, nhóm VIIA là nguyên tố phi kim.
C. Chu kỳ 4, nhóm IA là nguyên tố kim loại.
D. Chu kỳ 3, nhóm IA là nguyên tố kim loại.
Câu 9: Thuỷ phân hoàn toàn tinh bột trong dung dịch axit vô cơ loãng, thu được chất hữu cơ X. Cho X phản ứng với khí H2 (xúc tác Ni, to), thu được chất hữu cơ Y. Các chất X, Y lần lượt là:
A. glucozơ, fructozơ.
B. glucozơ, sobitol.
C. glucozơ, saccarozơ.
D. glucozơ, etanol.
Câu 10: Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: CH3COOC2H5, CH3CH2OH, CH3COOH, HCOOCH3 và các tính chất được ghi trong bảng sau:
|
Chất |
X |
Y |
Z |
T |
|
Nhiệt độ sôi |
31,8oC |
78,3oC |
118,1oC |
77,1oC |
Nhận xét nào sau đây đúng ?
A. X là CH3CH2OH.
B. Z là CH3COOH.
C. Y là CH3COOC2H5.
D. T là HCOOCH3.
---(Để xem tiếp nội dung từ câu 11 đến câu 40 của đề thi số 5 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
Trên đây là trích dẫn một phần nội dung Bộ 5 đề thi thử THPT QG môn Hóa học năm 2021-2022 có đáp án Trường THPT Tam Dương. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Ngoài ra các em có thể tham khảo thêm một số tư liệu cùng chuyên mục tại đây:
- Bộ 5 đề thi thử THPT QG môn Hóa học năm 2021-2022 có đáp án Trường THPT Lý Tự Trọng
- Bộ 5 đề thi thử THPT QG môn Hóa học năm 2021-2022 có đáp án Trường THPT Hà Huy Tập
Thi Online:
Chúc các em học tốt!












