Bộ 5 đề thi HK2 môn Hóa học 12 năm 2021-2022 Trường THPT Lê Viết Thuật gồm các câu hỏi có đáp án cụ thể và ma trận đề đánh giá. Có như vậy thế hệ giúp học trò lập cập làm quen với cấu trúc đề thi, ôn luyện để đạt kết quả cao hơn trong các kì thi sau này.
|
TRƯỜNG THPT LÊ VIẾT THUẬT |
ĐỀ THI HỌC KÌ 2 MÔN HÓA HỌC 12 NĂM HỌC 2021-2022 Thời gian làm bài 45 phút |
ĐỀ THI SỐ 1
Câu 1: Số nguyên tử cacbon trong phân tử etan là
A. 1. B. 2. C. 3. D. 4.
Câu 2: Tính chất hóa học đặc trưng của anken là dễ tham gia
A. phản ứng thế.
B. phản ứng cộng.
C. phản ứng thủy phân.
D. phản ứng trùng ngưng.
Câu 3: Số liên kết đôi C=C trong phân tử buta-1,3-đien là
A. 2. B. 3. C. 4. D. 1.
Câu 4: Công thức phân tử của benzen là
A. C6H6. B. C5H8. C. C7H8. D. CH4.
Câu 5: Khi đun nóng, toluen không tác dụng được với chất nào sau đây?
A. H2 (xúc tác). B. KMnO4. C. Br2 (xúc tác). D. NaOH.
Câu 6: Ở điều kiện thường chất nào sau đây là chất lỏng?
A. Metan. B. Benzen. C. Etilen. D. Axetilen.
Câu 7: Ancol etylic tác dụng với Na, thu được hiđro và chất nào sau đây?
A. C2H5OH. B. C2H5ONa. C. CH3OH. D. CH3ONa.
Câu 8: Tên thay thế của C2H5OH là
A. etanol. B. metanol. C. propanol. D. phenol.
Câu 9: Ancol nào sau đây là ancol bậc II?
A. CH3OH.
B. CH3CH2OH.
C. CH3CH(OH)CH3.
D. CH3CH2CH2OH.
Câu 10: Chất nào sau đây là chất rắn ở điều kiện thường?
A. Ancol etylic. B. Etan. C. Propan. D. Phenol.
Câu 11: Phenol rất độc, do đó khi sử dụng phenol phải hết sức cẩn thận. Công thức phân tử của phenol là
A. C2H6O. B. C6H6O. C. C3H8O. D. C2H4O2.
Câu 12: Chất nào sau đây tham gia phản ứng tráng bạc?
A. HCHO. B. CH3OH. C. C6H5OH. D. CH3COOH.
Câu 13: Chất X có công thức cấu tạo là CH3CH2CHO. Tên gọi của X là
A. metanal. B. etanal. C. propanal. D. butanal.
Câu 14: Chất nào sau đây là anđehit?
A. metanal. B. propanol. C. axit propanoic. D. phenol.
Câu 15: Dung dịch chất nào sau đây làm quì tím hóa đỏ?
A. Ancol etylic. B. Etanal. C. Axit axetic. D. Phenol.
Câu 16: Chất nào sau đây có nhiệt độ sôi cao nhất?
A. Axit fomic. B. Etanol. C. Etanal. D. Etan.
Câu 17: Benzen tác dụng với Br2 (Fe, t0) theo tỉ lệ mol 1:1, thu được chất hữu cơ X. Tên gọi của X là.
A. o-bromtoluen. B. toluen. C. Hexan. D. brombenzen.
Câu 18: Đun propan-1-ol với H2SO4 đặc ở 1800C, thu được chất nào sau đây?
A. Propen. B. Eten. C. Propan. D. Propin.
Câu 19: Chất nào sau đây tác dụng với dung dịch HNO3 tạo axit picric?
A. Benzen. B. Etanol. C. Axit axetic. D. Phenol.
Câu 20: Hiđro hóa hoàn toàn anđehit axetic (xúc tác Ni,to), thu được sản phẩm là
A. axit axetic. B. ancol etylic. C. Etilen. D. propilen.
Câu 21: Phát biểu nào sau đây sai?
A. Tính chất hóa học đặc trưng của anken là dễ tham gia phản ứng cộng.
B. Trùng hợp buta-1,3-đien ở điều kiện thích hợp thu được cao su buna.
C. Các ankin đều tham gia phản ứng với AgNO3 trong dung dịch NH3.
D. Isopren thuộc loại hiđrocacbon không no.
Câu 22: Phát biểu nào sau đây đúng?
A. Ở điều kiện thường, các hiđrocacbon thơm đều là chất lỏng.
B. Công thức phân tử của benzen là C8H8.
C. Toluen làm mất màu dung dịch KMnO4 khi đun nóng.
D. Công thức phân tử chung dãy đồng đẳng của benzen là CnH2n-2 (n ).
Câu 23: Đốt cháy hoàn toàn 0,015 mol C3H8, thu được CO2 và m gam H2O. Giá trị của m là
A. 0,54. B. 0,81. C. 2,16. D. 1,08.
Câu 24: Cho m gam ancol X (C2H5OH) tác dụng hoàn toàn với kim loại Na dư, thu được 0,448 lít khí H2 (ở đktc). Giá trị của m
A. 2,40. B. 0,60. C. 1,84. D. 0,92.
Câu 25: Phát biểu nào sau đây đúng?
A. Dung dịch phenol làm quì tím chuyển sang màu hồng.
B. Phenol tác dụng với NaOH tạo khí H2.
C. Phenol tác dụng với NaHCO3 tạo khí CO2.
D. Phenol tác dụng với Na tạo khí H2.
Câu 26: Chất nào sau đây tác dụng được với NaHCO3 tạo khí CO2?
A. Axit axetic. B. Phenol. C. Metanol. D. Propanal.
Câu 27: Cho 0,66 gam CH3CHO tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được m gam Ag. Giá trị của m là
A. 1,62. B. 0,81. C. 3,24. D. 4,75.
Câu 28: Cho 0,5 ml dung dịch chất X vào ống nghiệm, sau đó nhỏ tiếp từng giọt nước brom, đồng thời lắc nhẹ ống nghiệm, thấy có kết tủa trắng xuất hiện. Chất X là
A. Etanol. B. Phenol. C. Benzen. D. axit axetic.
Câu 29: Tỷ khối hơi của hỗn hợp X gồm propan, etan, butan so với không khí là 1,372. Để đốt cháy hết 0,3 mol X cần lượng oxi là
A. 2,275 mol. B. 1,365 mol. C. 4,25 mol. D. 2,15 mol.
Câu 30: Dẫn 4,032 lít (đktc) hỗn hợp hơi A gồm C2H2, HCHO (anđehit fomic) vào dung dịch AgNO3 trong NH3 dư. Sau khi phản ứng hoàn toàn thu được a gam kết tủa. Biết tỉ khối hơi của A so với H2 bằng 13,665. Giá trị của a là
A. 54,72. B. 41,76. C. 35,28. D. 70,56.
Câu 31: Thực hiện thí nghiệm như hình vẽ bên. Kết thúc thí nghiệm, trong bình đựng dung dịch AgNO3 trong NH3 xuất hiện kết tủa màu vàng nhạt. Chất X là
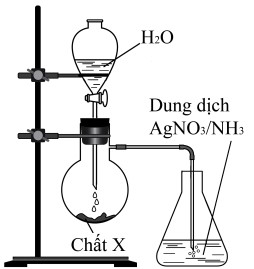
A. CaO. B. Al4C3.
C. CaC2. D. NaCl.
Câu 32: Oxi hoá 1,2 gam CH3OH bằng CuO nung nóng, sau một thời gian thu được hỗn hợp sản phẩm X (gồm HCHO, H2O và CH3OH dư). Cho toàn bộ X tác dụng với lượng dư Ag2O (hoặc AgNO3) trong dung dịch NH3, được 12,96 gam Ag. Hiệu suất của phản ứng oxi hoá CH3OH là
A. 70,4% B. 65,5% C. 76,6% D. 80,0%.
Câu 33: Đốt cháy hoàn toàn a mol axit hữu cơ Y được 2a mol CO2. Mặt khác, để trung hoà a mol Y cần vừa đủ 2a mol NaOH. Công thức cấu tạo thu gọn của Y là
A. HOOC-CH2-CH2-COOH B. C2H5-COOH
C. HOOC-COOH D. CH3-COOH
Câu 34: Cho các phát biểu sau:
(a) Axit fomic có phản ứng tráng bạc.
(b) Đun ancol etylic với H2SO4 đặc ở 1400C thu được đietyl ete.
(c) Anđehit fomic là chất khí ở điều kiện thường.
(d) Propen tác dụng với HBr thu được 2 dẫn xuất monobrom.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
Câu 35: Khi tách nước từ ancol 3-metylbutan-2-ol, sản phẩm chính thu được là
A. 3-metylbut-1-en.
B. 2-metylbut-2-en.
C. 2-metylbut-3-en.
D. 3-metylbut-2-en.
Câu 36: Cho 14 gam hỗn hợp X gồm CH4, C2H2, C3H6, C4H6 và H2 qua dung dịch brom dư đến phản ứng hoàn toàn thấy có 0,4 mol Br2 tham gia phản ứng. Mặt khác, đốt cháy hoàn toàn 0,6 mol hỗn hợp X thu được 1,5 mol CO2 và m gam H2O. Giá trị của m là
A. 36,0. B. 25,2. C. 27,0. D. 28,8.
Câu 37: Trung hòa 3,88 gam hỗn hợp X gồm hai axit cacboxylic no, đơn chức, mạch hở bằng dung dịch NaOH, cô cạn toàn bộ dung dịch sau phản ứng thu được 5,2 gam muối khan. Nếu đốt cháy hoàn toàn 3,88 gam X thì thể tích oxi (đktc) cần dùng là
A. 4,48 lít. B. 3,36 lít. C. 2,24 lít. D. 1,12 lít.
Câu 38: A là ancol no, đơn chức mạch hở. Cho 2,4 gam A tác dụng với Na dư thu được 0,448 lít H2 (ở đktc). Công thức phân tử của A là
A. CH4O. B. C2H6O. C. C3H6O. D. C3H8O.
Câu 39: Cho các phát biểu sau:
(a) Từ metanol có thể điều chế trực tiếp axit axetic.
(b) Hidrat hóa etilen (H2SO4, 3000C) thu được ancol etylic.
(c) Nung natri axetat với vôi tôi xút thu được metan.
(d) Oxi hóa etilen là phương pháp hiện đại sản xuất anđehit axetic.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
Câu 40: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào hai ống nghiệm, mỗi ống 3 – 4 giọt dung dịch CuSO4 2%.
Bước 2: Cho tiếp vào hai ống nghiệm, mỗi ống 2-3 ml dung dịch NaOH 10%, lắc nhẹ.
Bước 3: Tiếp tục nhỏ vào ống thứ nhất 3 – 4 giọt etanol, vào ống thứ hai 3 – 4 giọt glixerol. Lắc nhẹ cả hai ống nghiệm.
Cho các phát biểu sau:
(a) Kết thúc bước 2, trong cả hai ống nghiệm đều có kết tủa xanh của Cu(OH)2.
(b) Ở bước 2, có thể thay dung dịch NaOH bằng dung dịch KOH.
(c) Ở bước 3, trong ống nghiệm thứ nhất và thứ hai đều có hiện tượng: kết tủa bị tan ra cho dung dịch màu xanh lam.
(d) Ở bước 3, trong ống nghiệm thứ 2 tạo ra chất [C3H5(OH)2O]2Cu (đồng (II) glixerat).
Số phát biểu đúng là
A. 2. B. 4. C. 3. D. 1.
ĐỀ THI SỐ 2
ĐỀ THI HỌC KÌ 2 MÔN HÓA HỌC 12 TRƯỜNG THPT LÊ VIẾT THUẬT- ĐỀ 02
Câu 41: Quặng giàu sắt nhất là ?
A. Hematit. B. Xiđerit C. Pirit D. Mandehit.
Câu 42: Nước có tính cứng tạm thời có chứa anion nào sau đây?
A. HCO3-. B. HCO3-, SO42-, Cl-. C. SO42-, Cl-. D. Cl-, NO3-.
Câu 43: Kim loại nào sau đây có thể điều chế được bằng phản ứng nhiệt nhôm?
A. Na. B. Al. C. Ca. D. Fe.
Câu 44: Thành phần chính của quặng nào sau đây có chứa hợp chất của nguyên tố Canxi, Magie (MgCO3.CaCO3)
A. Manhetit. B. Boxit. C. Xinvinit. D. Đolomit.
Câu 45: Kim loại nhôm không tan trong dung dịch nào sau đây?
A. KNO3. B. HNO3 loãng. C. HCl. D. H2SO4 đặc nóng.
Câu 46: Phương trình hóa học nào sau đây đúng?
A. Na + AgNO3 → NaNO3 + Ag. B. Na2O + CO → 2Na + CO2.
C. Na2CO3 → Na2O + CO2. D. Na2O + H2O → 2NaOH.
Câu 47: Kim loại Fe phản ứng với dung dịch X (loãng, dư), tạo muối Fe(III). Chất X là
A. HNO3. B. H2SO4. C. HCl. D. CuSO4.
Câu 48: Số electron lớp ngoài cùng của các nguyên tử kim loại thuộc nhóm IIA là
A. 4. B. 1. C. 3. D. 2.
Câu 49: Dung dịch chất nào sau đây không phản ứng với FeO ?
A. NaOH. B. HCl. C. H2SO4. D. HNO3.
Câu 50: Dung dịch nào sau đây hòa tan được Al2O3?
A. HCl. B. KNO3. C. MgCl2. D. NaCl.
---(Để xem nội dung chi tiết từ câu 51 đến câu 80 của Đề thi số 02, các em vui lòng xem online hoặc đăng nhập HOC247.NET tải về máy)---
ĐỀ THI SỐ 3
ĐỀ THI HỌC KÌ 2 MÔN HÓA HỌC 12 TRƯỜNG THPT LÊ VIẾT THUẬT- ĐỀ 03
Câu 1: Cho Fe tác dụng với hơi nước ở nhiệt độ cao hơn 5700C thì thu được sản phẩm là
A. Fe2O3 và Fe3O4. B. Fe2O3 và H2. C. Fe3O4 và H2. D. FeO và H2.
Câu 2: Hai chất chỉ có tính oxi hóa là
A. Fe2O3, FeCl3. B. FeO, Fe2O3. C. Fe2O3, FeCl2. D. FeO, FeCl3.
Câu 3: Để tạo men màu lục cho đồ sứ, đồ thủy tinh người ta dùng
A. K2CrO4. B. CrO3. C. Cr2O3. D. Cr(OH)3.
Câu 4: Chất nào dưới đây là chất khử các sắt oxit trong lò cao?
A. CO. B. CO2. C. Al. D. H2.
Câu 5: Trong công nghiệp, nhôm được sản xuất bằng phương pháp điện phân Al2O3 nóng chảy. Nhiệt độ nóng chảy của Al2O3 rất cao (20500C), vì vậy để hạ nhiệt độ nóng chảy xuống, phải hòa tan Al2O3 trong:
A. criolit nóng chảy. B. đất sét nóng chảy. C. boxit nóng chảy. D. mica nóng chảy.
Câu 6: Có các dung dịch: AlCl3, FeCl3, CuCl2, FeCl2. Nếu chỉ dùng dung dịch NaOH làm thuốc thử thì có thể phân biệt được
A. 2 dung dịch. B. 4 dung dịch. C. 1 dung dịch. D. 3 dung dịch.
Câu 7: Hòa tan 16,8 gam sắt bằng dung dịch H2SO4 loãng dư thu được dung dịch X. Dung dịch X phản ứng vừa đủ với V ml dung dịch K2Cr2O7 0,5M. Giá trị của V là
A. 150 ml. B. 50 ml. C. 100 ml. D. 200 ml
Câu 8: Cho dung dịch chứa FeCl2 và AlCl3 tác dụng với dung dịch NaOH dư, sau đó lấy kết tủa nung trong không khí đến khối lượng không đổi thu được chất rắn gồm
A. Fe2O3. B. FeO. C. FeO, ZnO. D. Fe2O3, ZnO.
Câu 9: Hòa tan hết 1,08 gam hỗn hợp Cr và Fe trong dung dịch HCl loãng, nóng thu được 448ml khí (đktc). Lượng crom có trong hỗn hợp là
A. 0,26 gam. B. 1,04 gam. C. 0,056 gam D. 0,52 gam.
Câu 10: Để chế tạo thép không gỉ, người ta thêm vào thành phần của thép thường kim loại
A. Mn. B. W, Cr. C. Cr, Ni. D. Si.
---(Để xem nội dung chi tiết từ câu 11 đến câu 40 của Đề thi số 03, các em vui lòng xem online hoặc đăng nhập HOC247.NET tải về máy)---
ĐÁP ÁN ĐỀ THI SỐ 3
|
1 |
D |
11 |
D |
21 |
D |
31 |
B |
|
2 |
A |
12 |
B |
22 |
B |
32 |
C |
|
3 |
C |
13 |
C |
23 |
C |
33 |
D |
|
4 |
A |
14 |
C |
24 |
D |
34 |
A |
|
5 |
A |
15 |
B |
25 |
A |
35 |
D |
|
6 |
B |
16 |
D |
26 |
A |
36 |
D |
|
7 |
C |
17 |
A |
27 |
D |
37 |
C |
|
8 |
A |
18 |
B |
28 |
B |
38 |
A |
|
9 |
D |
19 |
B |
29 |
B |
39 |
C |
|
10 |
C |
20 |
B |
30 |
D |
40 |
C |
ĐỀ THI SỐ 4
ĐỀ THI HỌC KÌ 2 MÔN HÓA HỌC 12 TRƯỜNG THPT LÊ VIẾT THUẬT- ĐỀ 04
Câu 1. Điện phân dung dịch hỗn hợp chứa 0,04 mol AgNO3 và 0,05 mol Cu(NO3)2, điện cực trơ, dòng điện 5A, trong 32 phút 10 giây. Khối lượng kim loại bám vào catot là:
A. 6,24 gam. B. 3,12 gam. C. 6,5 gam. D. 7,24 gam.
Câu 2. Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3, MgO (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm:
A. Cu, Al, Mg.
B. Cu, Al, MgO.
C. Cu, Al2O3, MgO.
D. Cu, Al2O3, Mg.
Câu 3. Dẫn V lít (đktc) khí CO2 qua 100ml dung dịch Ca(OH)2 1M thu được 6gam kết tủa. Lọc bỏ kết tủa, lấy dung dịch nước lọc đun nóng lại thu được kết tủa nữa. Giá trị của V là:
A. 1,344lit. B. 2,24 lit.
C. 3,136lit. D. 3,136lit hoặc 1,344 lit.
Câu 4. Để khử hoàn toàn 30 gam hỗn hợp CuO, FeO, Fe2O3, Fe3O4, MgO cần dùng 5,6 lít khí CO (ở đktc). Khối lượng chất rắn sau phản ứng là:
A. 28 gam. B. 26 gam. C. 22 gam. D. 24 gam.
Câu 5. Để làm sạch loại thủy ngân có lẫn tạp chất là Zn,Sn,Pb cần khuấy loại thủy ngân này trong:
A. Dung dịch Sn(NO3)2. B. Dung dịch HgNO3)2.
C. Dung dịch Zn(NO3)2. D. Dung dịch Pb(NO3)2.
Câu 6. Al2O3, Al(OH)3 bền trong:
A. Dung dịch HCl. B. Dung dịch Ca(OH)2.
C. H2O. D. Dung dịch Ba(OH)2.
Câu 7. Chất nào dưới đây góp phần nhiều nhất vào sự hình thành mưa axit ?
A. Ozon. B. Dẫn xuất flo của hidrocacbon.
C. Cacbon dioxit. D. Lưu huỳnh dioxit.
Câu 8. Để phân biệt các khí CO CO2 O2 và SO2 có thể dùng
A. tàn đóm cháy dở và nước brom.
B. dung dịch Na2CO3 và nước brom.
C. tàn đóm cháy dở nước vôi trong và dung dịch K2CO3.
D. tàn đóm cháy dở nước vôi trong và nước brom.
Câu 9. Hòa tan hết 9,6 gam hỗn hợp hai kim loại kiềm thuộc 2 chu kì liên tiếp vào nước được 3,36 lít khí (đktc). Hai kim loại kiềm đó là:
A. K, Rb. B. Rb, Cs. C. Li, Na. D. Na, K.
Câu 10. Cho 50 gam hỗn hợp X gồm bột Fe3O4 và Cu vào dung dịch HCl dư. Kết thúc phản ứng còn lại 20,4 gam chất rắn không tan. Phần trăm về khối lượng của Cu trong hỗn hợp X là:
A. 53,6%. B. 40,8%. C. 20,4%. D. 40,0 %.
---(Để xem nội dung chi tiết từ câu 11 đến câu 40 của Đề thi số 04, các em vui lòng xem online hoặc đăng nhập HOC247.NET tải về máy)---
ĐÁP ÁN ĐỀ THI SỐ 4
|
1. A |
11. C |
21. A |
31. C |
|
2. C |
12. B |
22. D |
32. B |
|
3. C |
13. D |
23. C |
33. A |
|
4. B |
14. A |
24. C |
34. D |
|
5. B |
15. A |
25. C |
35. A |
|
6. C |
16. D |
26. B |
36. A |
|
7. D |
17. B |
27. D |
37. D |
|
8. D |
18. D |
28. C |
38. B |
|
9. D |
19. B |
29. B |
39. B |
|
10. A |
20. A |
30. C |
40. A |
ĐỀ THI SỐ 5
ĐỀ THI HỌC KÌ 2 MÔN HÓA HỌC 12 TRƯỜNG THPT LÊ VIẾT THUẬT- ĐỀ 05
Câu 1. Khi điều chế kim loại, các ion kim loại đóng vai trò là chất
A. nhận proton B. bị khử C. khử D. cho proton
Câu 2. Trộn 200 ml dung dịch H2SO4 0,05M với 300 ml dung dịch NaOH 0,06M. pH của dung dịch tạo thành là
A. 2,7 B. 1,6 C. 2,4 D. 1,9
Câu 3. Nhỏ từ từ dung dịch H2SO4 loãng vào dung dịch K2CrO4 thì màu của dung dịch chuyển từ
A. màu vàng sang màu da cam B. không màu sang màu vàng
C. không màu sang màu da cam D. màu da cam sang màu vàng
Câu 4. Có các kim loại: Cu, Ag, Fe, Al, Au. Độ dẫn điện của chúng giảm dần theo thứ tự
A. Ag, Cu, Au, Al, Fe
B. Ag, Cu, Fe, Al, Au
C. Al, Fe, Cu, Ag, Cu
D. Au, Ag, Cu, Fe, Al
Câu 5. Hòa tan hết m gam hỗn hợp Al và Fe trong lượng dư dung dịch H2SO4 loãng thoát ra 0,4 mol khí, còn trong lượng dư dung dịch NaOH thì thu được 0,3 mol khí. Giá trị của m là
A. 11,00 B. 13,70 C. 12,28 D. 19,50
Câu 6. Dùng m gam Al để khử hết 1,6 gam Fe2O3 (phản ứng nhiệt nhôm). Cho sản phẩm sau phản ứng tác dụng với lượng dư dung dịch NaOH thu được 0,672 lít khí (đktc). Giá trị của m là
A. 0,540 B. 1,755 C. 1,080 D. 0,810
Câu 7. Hòa tan hoàn toàn a gam hỗn hợp X gồm Fe, FeS, FeS2 và S vào dung dịch HNO3 loãng dư, giải phóng 8,064 lít NO ( là sản phẩm khử duy nhất ở đtkc ) và dung dịch Y. Cho dung dịch Ba(OH)2 dư vào dung dịch Y thu được kết tủa Z. Hòa tan lượng kết tủa Z bằng dung dịch HCl dư, sau phản ứng còn lại 30,29 gam chất rắn không tan. Giá trị của a gam là
A. 8,64 B. 9,76 C. 7,92 D. 9,52
Câu 8. Điện phân dung dịch CuCl2 bằng điện cực trơ trong 1 giờ với cường độ dòng điện 5 ampe. Khối lượng đồng giải phóng ở catot là
A. 5,9 gam B. 7,9 gam C. 5,5 gam D. 7,5 gam
Câu 9. Hoà tan 1,84 gam hỗn hợp Fe và Mg trong lượng dư dung dịch HNO3 thấy thoát ra 0,04 mol khí NO duy nhất (đktc). Số mol Fe và Mg trong hỗn hợp lần lượt bằng
A. 0,03 và 0,03 B. 0,02 và 0,03 C. 0,03 và 0,02 D. 0,01 và 0,01
Câu 10. 100 ml dung dịch A chứa NaOH 0,1M và NaAlO2 0,3M .Thêm từ từ HCl 0,1M vào dung dịch A cho đến khi kết tủa tan trở lại một phần,lọc kết tủa ,nung ở nhiệt độ cao đến khối lượng không đổi thu được 1,02g chất rắn .Thể tích dung dịch HCl đã dùng là
A. 0,8 lít B. 0,6 lít C. 0,7 lít D. 0,5 lít
---(Để xem nội dung chi tiết từ câu 11 đến câu 30 của Đề thi số 05, các em vui lòng xem online hoặc đăng nhập HOC247.NET tải về máy)---
ĐÁP ÁN ĐỀ THI SỐ 5
01. B; 02. A; 03. A; 04. A; 05. A; 06. C; 07. B; 08. A; 09. B; 10. C
11. C; 12. A; 13. C; 14. A; 15. D; 16. A; 17. C; 18. A; 19. B; 20. B
21. D; 22. D; 23. D; 24. B; 25. A; 26. D; 27. C; 28. B; 29. A; 30. B
Trên đây là một phần trích dẫn nội dung Bộ 5 đề thi HK2 môn Hóa học 12 năm 2021-2022 có đáp án Trường THPT Lê Viết Thuật. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Ngoài ra các em có thể tham khảo thêm một số tư liệu cùng chuyên mục:
- Đề cương ôn tập HK2 môn Hóa học 12 năm 2021-2022
- Bộ 5 đề thi HK2 môn Hóa học 12 năm 2021-2022 có đáp án Trường THPT Hà Huy Tập
Thi Online:
Chúc các em học tốt!












