Mời quý thầy cô cùng các em học sinh tham khảo tài liệu Bản sắc tư duy NAP 4.0 trong giải toán Hóa học vô cơ năm 2021. Tài liệu bao gồm phần tóm tắt lý thuyết, các hỏi minh họa có đáp án và phần tự luyện tập. Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập hiệu quả và đạt điểm số cao trong kì thi sắp tới.
1. TÓM TẮT LÝ THUYẾT
1.1. Tư duy NAP 4.0 về tính bất biến của kim loại
Trong hóa học vô cơ những bài toán liên quan tới tính chất của kim loại chính là những bài toán nền tảng rất quan trọng. Tuy nhiên, đại đa số các em vẫn có tư duy tự luận để áp dụng vào giải trắc nghiệm. Phần này tôi sẽ trình bày cho bạn thấy bản chất tổng quát hay quy luật bất biến của kim loại khi nó tham gia phản ứng hóa học.
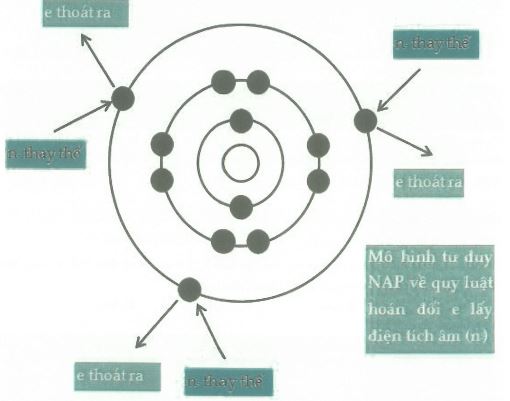
Quy luật ở đây là: khi kim loại tham gia vào bất kì một phản ứng nào đó thì electron trong kim loại sẽ bị bật ra và để đảm bảo tính trung hòa về điện thì phải có một điện tích âm khác thay thế phần e bị bật ra đó (các bạn xem mô hình dưới đây). Đương nhiên là nếu không có phản ứng hóa học thì cũng sẽ không có e nào bay ra nên không có sự đổi trác gì hết.
1.2. Một số trường hợp điển hình:
|
Kim loại |
Tác nhân phản ứng |
Điện tích âm thay thế e |
Hợp chất tạo thành |
|
Trước Pb (trong dãy điện hóa) |
HCl |
Cl |
Muối |
|
Trước Pb (trong dãy điện hóa) |
H2SO4 |
|
Muối |
|
Trừ (Au, Pt) |
HNO3 |
|
Muối |
|
Trừ (Au, Ag, Pt) |
O2 |
|
Oxit |
|
Kiềm, Ba, Ca, Sr |
H2O |
OH- |
Hidroxit |
|
|
… |
… |
… |
1.3. Những sản phẩm khử quan trọng để nhận ra số e bị bật ra từ kim loại
|
Sản phẩm khử |
Số e bật ra |
Sản phẩm khử |
Số e bật ra |
|
H2 |
2 |
N2 |
10 |
|
NO2 |
1 |
O2- |
2 |
|
NO |
3 |
SO2 |
2 |
|
N2O |
8 |
S |
6 |
|
|
8 |
H2S |
8 |
2. VÍ DỤ MINH HỌA
Ví dụ 1: Hỗn hợp X chứa 0,03 mol Cu; 0,03 mol Zn; 0,03 mol Mg và 0,02 mol Al. Đốt nóng X trong O2 dư để các phản ứng xảy ra hoàn toàn thì thu được tối đa bao nhiêu gam oxit?
A. 7,05 gam B. 8,06 gam C. 6,78 gam D. 7,62 gam
Định hướng tư duy giải:
Ta có:
\({n_e} = 0,03.2 + 0,03.2 + 0,03.2 + 0,02.3 = 0,24\) → \({n_O} = 0,12\)
Ví dụ 2: Hòa tan hoàn toàn m gam hỗn hợp X chứa Ca, Ba, Na, K, Li vào trong nước dư thu được dung dịch Y và 3,36 lít khí (đktc). Trung hòa dung dịch Y cần dùng vừa đủ 300 ml dung dịch HCl aM. Giá trị của a là?
A. 1,0 B. 0,8 C. 1,2 D. 1,5
Định hướng tư duy giải:
Ta có:
\({n_{{H_2}}} = 0,15\) → \({n_e} = 0,3\) → \({n_{O{H^ - }}} = 0,3\) \({→n_{{H^ + }}} = 0,3 = 0,3a\) → a = 1
Ví dụ 3: Hòa tan hết 1,360 gam hỗn hợp hai kim loại X, Y trong dung dịch H2SO4 loãng, thu được 0,672 lít khí (đktc) và m gam muối. Giá trị của m là:
A. 2,44 B. 4,42 C. 24,4 D. 4,24
Định hướng tư duy giải:
Ta có:
\({n_{{H_2}}} = 0,03\) → \(n_e^ \uparrow = 0,06\) → \({n_{SO_4^{2 - }}} = 0,03\) → \(m = 1,36 + 0,03.96 = 4,24\)
Ví dụ 4: Hòa tan 9,14 gam hợp kim Cu, Mg, Al bằng một lượng vừa đủ dung dịch HCl thu được 7,84 lít khí X (đktc) và 2,54 gam chất rắn Y và dung dịch Z. Lọc bỏ chất rắn Y, cô cạn cẩn thận dung dịch Z thu được lượng muối khan là
A. 31,45 gam B. 33,99 gam C. 19,025 gam D. 56,3 gam
Định hướng tư duy giải:
Chú ý: Cu không tan trong HCl (không có sự đổi e lấy Cl-)
Ta có:
\({n_{{H_2}}} = 0,35\) → \({n_e} = 0,7\) → \({n_{C{l^ - }}} = 0,7\) → \(m = 9,24 - 2,54 + 0,7.35,5 = 31,45\)
Ví dụ 5: Cho 24 gam Mg tác dụng vừa đủ với dung dịch chứa a mol HNO3. Sau phản ứng thu được hỗn hợp khí X gồm các khí N2; N2O có số mol bằng nhau và bằng 0,l mol. Tìm giá trị a.
A. 2,8 B. 1,6 C. 2,54 D. 2,45
Định hướng tư duy giải:
Ta có ngay:
\({n_{Mg}} = 1\,\,\left( {mol} \right)\) → \({n_e} = 2\) → \({n_{Mg{{\left( {N{O_3}} \right)}_2}}} = 1\,\,\left( {mol} \right)\)
\(\left\{ \begin{array}{l}
{n_{{N_2}}} = 0,1\\
{n_{{N_2}O}} = 0,1
\end{array} \right.\) → \({n_{N{H_4}N{O_3}}} = \frac{{2 - 0,1.10 - 0,1.8}}{8} = 0,025\)
Ví dụ 6: Hòa tan hết 20,5 gam hỗn hợp Mg, Al, Zn trong dung dịch HNO3 thu được 4,48 lít hỗn hợp khí X gồm NO2, NO, N2O, N2 ở đktc, không còn sản phẩm khử nào khác, trong đó NO2 và N2 có cùng số mol. Tỷ khối hơi của X so với H2 là 18,5. Khối lượng muối thu được khi cô cạn dung dịch sau phản ứng là:
A. 88,7 gam B. 119,7 gam C. 144,5 gam D. 55,7 gam
Định hướng tư duy giải:
Vì \({n_{N{O_2}}} = {n_{{N_2}}}\) ta tưởng tượng như nhấc 1 O trong NO2 rồi lắp vào N2 như vậy X sẽ chỉ có hai khí là NO và N2O (số mol hỗn hợp X vẫn không đổi).
Khi đó: \({n_X} = 0,2\left\{ \begin{array}{l}
NO:0,1\,\,\left( {mol} \right)\\
{N_2}O:0,1\,\,\left( {mol} \right)
\end{array} \right.\) → \({n_e} = n_{NO_3^ - }^{{\rm{trong muoi}}} = 0,1.3 + 0,1.8 = 1,1\) (mol)
\(m = 20,5 + 1,1.62 = 88,7\) (gam)
Ví dụ 7: Cho m gam hỗn hợp X gồm Mg và Al (có tỷ lệ mol 3:4) vào dung dịch chứa HNO3 loãng dư, sau phản ứng hoàn toàn thu được dung dịch chứa 8,2m gam muối. Biết rằng có 0,3 mol N+5 trong HNO3 đã bị khử. Số mol HNO3 đã phản ứng là:
A. 2,1 B. 3,0 C. 2,4 D. 4,0
Định hướng tư duy giải:
Có \(\left\{ \begin{array}{l}
Mg:3a\\
Al:4a
\end{array} \right.\). → \({n_e} = 18a\) → \(m = 24.3a + 27.4a = 180a\)
Vậy
\(8,2m\left\{ \begin{array}{l}
Mg,Al\\
NO_3^ - :18a\\
N{H_4}N{O_3}:0,3
\end{array} \right.\)
\(7,2.180a = 18a.62 + 80.0,3\) → \(a = \frac{2}{{15}}\) → \({n_{HN{O_3}}} = \frac{2}{{15}}.18 + 0,3.2 = 3\)
3. LUYỆN TẬP
Câu 1: Hòa tan 30 gam hỗn hợp một số kim loại vào dung dịch H2SO4 đặc nóng dư thu được dung dịch X và 0,15 mol SO2, 0,l mol S và 0,005 mol H2S. Khối lượng muối tạo thành sau phản ứng là :
A. 78g B. 120,24g C. 44,4g D. 75,12g
Câu 2: Hoà tan 6,0 gam hỗn hợp X gồm Mg, Al, Zn trong dung dịch HNO3 vừa đủ, sau phản ứng hoàn toàn thu được dung dịch Y và hỗn hợp gồm 0,02 mol NO và 0,02 mol N2O. Làm bay hơi dung dịch Y thu được 25,4 gam muối khan. Số mol HNO3 bị khử trong phản ứng trên là:
A. 0,08 mol B. 0,06 mol C. 0,09 mol D. 0,07 mol
Câu 3: Hoà m gam hỗn hợp Fe, Cu (Fe chiếm 40%) vào 380 ml dung dịch HNO3 1M. Sau phản ứng thu được dung dịch Y và 0,7m gam chất rắn và 1,12 lít hỗn hợp gồm NO, N2O (ở đktc) (là hai sản phẩm khử duy nhất). Khối lượng muối khan thu được khi cô cạn Y là
A. 32,4 gam B. 45 gam C. 21,6 gam D. 27 gam
Câu 4: Hỗn hợp X gồm Fe, Cu có khối lượng 6 gam. Tỉ lệ khối lượng giữa Fe và Cu là 7:8. Cho lượng X nói trên vào một lượng dung dịch HNO3, khuấy đều cho phản ứng xảy ra hoàn toàn thì thu được một phần chất rắn Y nặng 4,32 gam, dung dịch muối sắt và NO. Khối lượng muối Fe tạo thành trong dung dịch là
A. 4,5 gam B. 5,4 gam C. 7,4 gam D. 6,4 gam
Câu 5: Cho 4,8g Mg tác dụng với HNO3 dư. Phản ứng xảy ra hoàn toàn thu được 2,24 lít NO (đktc) và dd X. Khối lượng muối thu được trong X:
A. 29,6g B. 30,6g C. 34,5g D. 22,2g
Câu 6: Cho 6,675g hỗn hợp Mg và kim loại M (hóa trị duy nhất n, đứng sau Mg, tác dụng được với H+ giải phóng H2) có tỷ lệ mol là 1:1 vào dung dịch AgNO3 dư khi kết thúc phản ứng thu được 32,4g chất rắn. Ở một thí nghiệm khác nếu cho 6,675g hỗn hợp kim loại trên vào dung dịch HNO3 dư sau phản ứng thu được V lít NO đktc (sản phẩm khử duy nhất), giá trị của V là:
A. 4,48 B. 1,12 C. 3,36 D. 2,24
Câu 7: Cho 25,24 gam hỗn hợp X chứa Al, Zn, Mg, Fe phản ứng vừa đủ với 787,5 gam dung dịch HNO3 20% thu được dung dịch chứa m gam muối và 0,2 mol hỗn hợp khí Y (gồm N2O và N2) có tỉ khối so với H2 là 18. Giá trị của m là
A. 163,60. B. 153,13. C. 184,12. D. 154,12.
Câu 8: Hòa tan hết hỗn hợp X gồm Fe, Cu và Ag trong V ml dung dịch HNO3 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y và 0,2 mol NO (sản phẩm khử duy nhất). Giá trị tối thiểu của V là
A. 800. B. 400. C. 600. D. 200.
Câu 9: Cho 2,8 gam hỗn hợp X gồm Cu và Ag phản ứng hoàn toàn với dung dịch HNO3 dư, thu được 0,04 mol NO2 (sản phẩm khử duy nhất của N+5 và dung dịch chứa m gam muối. Giá trị của m là
A. 4,08. B. 5,28. C. 2,62. D. 3,42.
Câu 10: Hoà tan hoàn toàn 8,4 gam Fe cần V ml dung dịch HNO3 0,5M thu được khí NO (sản phẩm khử duy nhất). Giá trị nhỏ nhất của V là
A. 400. B. 1200. C. 800. D. 600.
Câu 11: Hòa tan hoàn toàn 42,9 gam Zn trong lượng vừa đủ V ml dung dịch HNO3 10% sau phản ứng thu được dung dịch A chứa 129,54 gam hai muối tan và 4,032 lít (đktc) hỗn hợp hai khí NO và N2O . Giá trị của V là:
A. 840 ml B. 540 ml C. 857 ml D. 1336 ml
Câu 12: Cho 12,9g hỗn hợp gồm Mg và Al phản ứng vừa đủ với V(lít) dung dịch HNO3 0.5M thu được dung dịch B và hỗn hợp C gồm 2 khí N2 và N2O có thể tích bằng 2.24 lít (đktc).Tỉ khối của C so với H2 là 18. Cho dung dịch NaOH dư vào dung dịch B thu được 1.12 lít khí(đktc) và mg kết tủa. Giá trị của m và V lần lượt là:
A. 35g và 3,2lít B. 35g và 2,6lít C. 11,6g và 3,2lít D. 11,6g và 2,6lít
Câu 13: Cho 14,4 gam hỗn hợp gồm Fe, Mg và Cu (số mol mỗi kim loại bằng nhau) tác dụng hết với dung dịch HNO3, thu được dung dịch X và 2,688 lít (đktc) hỗn hợp gồm 4 khí N2, N2O, NO và NO2 trong đó hai khí N2 và NO2 có số mol bằng nhau. Cô cạn cẩn thận toàn bộ X thu được 58,8 gam muối khan. Số mol HNO3 đã tham gia phản ứng là
A. 0,945. B. 0,725. C. 0,923. D. 0,893.
Câu 14: Biết hai kim loại A,B đều có hóa trị II (MA < MB). Nếu cho 10,4 gam hỗn hợp A và B (có số mol bằng nhau) tác dụng với dd HNO3 đặc, dư thu được 8,96 lít khí NO2 là sản phẩm khử duy nhất.(đktc). Nếu cho 12,8 gam hỗn hợp A và B (có khối lượng bằng nhau) tác dụng với dung dịch HNO3 đặc ,dư thu được 11,6 lít NO2 (đktc), A và B lần lượt là:
A. Mg và Cu B. Cu và Zn C. Mg và Zn D. Ca và Cu
Câu 15: Cho 6,175 gam Zn tác dụng vừa đủ với dung dịch chứa a mol HNO3. Sau phản ứng thu được dung dịch X và 0,448 lít hỗn hợp khí Y gồm NO, N2O. Tỉ khối hơi của Y so với hh là 18,5. Cô cạn dung dịch X thu được b gam muối. Giá trị của a và b lần lượt là:
A. 0,24 và 18,735. B. 0,14 và 17,955. C. 0,24 và 18,755. D. 0,14 và 18,755.
Trên đây là một phần trích dẫn nội dung Bản sắc tư duy NAP 4.0 trong giải toán Hóa học vô cơ năm 2021. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Chúc các em học tốt!












