Nhß║▒m gi├║p c├Īc em hß╗Źc sinh c├│ th├¬m nhiß╗üu t├Āi liß╗ću tham khß║Żo hoc247 xin giß╗øi thiß╗ću t├Āi liß╗ću 11 PhŲ░ŲĪng ph├Īp giß║Żi nhanh b├Āi tß║Łp H├│a hß╗Źc hß╗»u cŲĪ, v├┤ cŲĪ ─æŲ░ß╗Żc bi├¬n soß║Īn v├Ā tß╗Ģng hß╗Żp dŲ░ß╗øi ─æ├óy. T├Āi liß╗ću gß╗ōm 11 phŲ░ŲĪng ph├Īp giß║Żi sß║Į gi├║p c├Īc em ├┤n tß║Łp thß║Łt tß╗æt, cß╗¦ng cß╗æ kiß║┐n thß╗®c bß╗Ö m├┤n H├│a. Hy vß╗Źng ─æ├óy sß║Į l├Ā t├Āi liß╗ću tham khß║Żo hß╗»u ├Łch cho c├Īc em hß╗Źc sinh!
11 PhŲ░ŲĪng ph├Īp giß║Żi nhanh b├Āi tß║Łp H├│a hß╗Źc hß╗»u cŲĪ, v├┤ cŲĪ
PhŲ░ŲĪng ph├Īp 1. PhŲ░ŲĪng ph├Īp bß║Żo to├Ān ─æiß╗ćn t├Łch trong h├│a hß╗Źc
1. Nội dung
+ Nguy├¬n tß╗Ł, ph├ón tß╗Ł, dung dß╗ŗch lu├┤n trung h├▓a vß╗ü ─æiß╗ćn
+ Trong nguy├¬n tß╗Ł: Sß╗æ proton = sß╗æ electron
+ Trong dung dß╗ŗch: sß╗æ mol x ─æiß╗ćn t├Łch ├óm = sß╗æ mol x ─æiß╗ćn t├Łch dŲ░ŲĪng
2. Phß║Īm vi sß╗Ł dß╗źng
+ ─Éß╗æi vß╗øi b├Āi to├Īn dung dß╗ŗch
+ Trong b├Āi to├Īn c├│ xuß║źt hiß╗ćn c├Īc chß║źt ─æiß╗ćn li mß║Īnh: muß╗æi, axit, bazŲĪ
Ch├║ ├Į: Vß╗øi phŲ░ŲĪng ph├Īp n├Āy thŲ░ß╗Øng sß╗Ł dß╗źng kß║┐t hß╗Żp vß╗øi c├Īc phŲ░ŲĪng ph├Īp sau:
+ Bß║Żo to├Ān khß╗æi lŲ░ß╗Żng
+ Bß║Żo to├Ān nguy├¬n tß╗æ
+ Viß║┐t phŲ░ŲĪng tr├¼nh ion r├║t gß╗Źn
`PhŲ░ŲĪng ph├Īp n├Āy thŲ░ß╗Øng chß╗ē sß╗Ł dß╗źng vß╗øi b├Āi to├Ān v├┤ cŲĪ
PhŲ░ŲĪng ph├Īp 2: PhŲ░ŲĪng ph├Īp bß║Żo to├Ān electron trong h├│a hß╗Źc
1. Nội dung
Trong phß║Żn ß╗®ng oxi h├│a khß╗Ł:
Sß╗æ electron nhŲ░ß╗Øng = Sß╗æ electron nhß║Łn
Sß╗æ mol electron nhŲ░ß╗Øng = Sß╗æ mol electron nhß║Łn
2. Phß║Īm vi sß╗Ł dß╗źng
+ Chß╗¦ yß║┐u ├Īp dß╗źng cho b├Āi to├Īn oxi h├│a khß╗Ł c├Īc chß║źt v├┤ cŲĪ
+ Khi gß║Ęp b├Āi to├Īn c├│ sß╗Ł dß╗źng HNO3, H2SO4 ─æß║Ęc n├│ng
Ch├║ ├Į:
+ X├Īc ─æß╗ŗnh ch├Łnh x├Īc chß║źt khß╗Ł, chß║źt oxi h├│a ( dß╗▒a v├Āo sß╗▒ thay ─æß╗Ģi sß╗æ oxi h├│a cß╗¦a c├Īc nguy├¬n tß╗Ł trong c├Īc chß║źt)
+ C├│ thß╗ā ├Īp dß╗źng bß║Żo to├Ān e cho mß╗Öt sß╗æ phŲ░ŲĪng tr├¼nh, nhiß╗üu phŲ░ŲĪng tr├¼nh hoß║Ęc to├Ān bß╗Ö qu├Ī tr├¼nh
+ X├Īc ─æß╗ŗnh c├Īc chß║źt nhŲ░ß╗Øng v├Ā nhß║Łn e. Nß║┐u x├®t cho mß╗Öt qu├Ī tr├¼nh, chß╗ē cß║¦n x├Īc ─æß╗ŗnh trß║Īng th├Īi ─æß║¦u v├Ā trß║Īng th├Īi cuß╗æi sß╗æ oxi h├│a cß╗¦a nguy├¬n tß╗æ, thŲ░ß╗Øng kh├┤ng quan t├óm ─æß║┐n trß║Īng th├Īi trung gian sß╗æ oxi h├│a cß╗¦a nguy├¬n tß╗æ
+ Khi ├Īp dß╗źng phŲ░ŲĪng ph├Īp bß║Żo to├Ān e thŲ░ß╗Øng sß╗Ł dß╗źng k├©m c├Īc phŲ░ŲĪng ph├Īp bß║Żo to├Ān kh├Īc ( khß╗æi lŲ░ß╗Żng, nguy├¬n tß╗æ)
PhŲ░ŲĪng ph├Īp 3: PhŲ░ŲĪng ph├Īp bß║Żo to├Ān khß╗æi lŲ░ß╗Żng trong h├│a hß╗Źc
1. Nội dung
mtham gia = msß║Żn phß║®m
─Éß╗æi vß╗øi b├Āi to├Īn sß╗Ł dß╗źng c├Īc chß║źt dŲ░ sau phß║Żn ß╗®ng ta c├│:
mtrŲ░ß╗øc pŲ░ = msau pŲ░
Ch├║ ├Į: ─Éß╗æi vß╗øi c├Īc phß║Żn ß╗®ng tß║Īo th├Ānh chß║źt kß║┐t tß╗¦a, bay hŲĪi, khß╗æi lŲ░ß╗Żng dung dß╗ŗch sß║Į thay ─æß╗Ģi sau phß║Żn ß╗®ng:
mdd sau phß║Żn ß╗®ng = mdd trŲ░ß╗øc phß║Żn ß╗®ng + mchß║źt tan ŌĆō mkß║┐t tß╗¦a ŌĆō mbay hŲĪi
2. Phß║Īm vi sß╗Ł dß╗źng
ThŲ░ß╗Øng sß╗Ł dß╗źng phŲ░ŲĪng ph├Īp bß║Żo to├Ān khß╗æi lŲ░ß╗Żng trong c├Īc b├Āi to├Īn sau:
+ Biß║┐t tß╗Ģng khß╗æi lŲ░ß╗Żng chß║źt ban ─æß║¦u ( tham gia) t├Łnh khß╗æi lŲ░ß╗Żng chß║źt tß║Īo th├Ānh sß║Żn phß║®m hoß║Ęc ngŲ░ß╗Żc lß║Īi
+ Trong b├Āi to├Īn c├│ n chß║źt m├Ā ch├║ng ta biß║┐t khß╗æi lŲ░ß╗Żng cß╗¦a (n-1) chß║źt ta sß║Į t├Łnh ─æŲ░ß╗Żc khß╗æi lŲ░ß╗Żng chß║źt c├▓n lß║Īi
+ Nhß╗»ng b├Āi to├Īn ta kh├┤ng thß╗ā x├Īc ─æß╗ŗnh ─æŲ░ß╗Żc sß╗æ mol do kh├┤ng biß║┐t ─æŲ░ß╗Żc ph├ón tß╗Ł khß╗æi cß╗¦a c├Īc chß║źt
PhŲ░ŲĪng ph├Īp 4: PhŲ░ŲĪng ph├Īp bß║Żo to├Ān nguy├¬n tß╗æ trong h├│a hß╗Źc
1. Nội dung
Tß╗Ģng sß╗æ mol nguy├¬n tß╗Ł cß╗¦a mß╗Öt nguy├¬n tß╗æ X bß║źt kß╗│ trŲ░ß╗øc v├Ā sau phß║Żn ß╗®ng l├Ā lu├┤n bß║▒ng nhau
2. Phß║Īm vi sß╗Ł dß╗źng
Trong c├Īc phß║Żn ß╗®ng h├│a hß╗Źc c├Īc nguy├¬n tß╗æ lu├┤n ─æŲ░ß╗Żc bß║Żo to├Ān
ŌćÆ Sß╗æ mol nguy├¬n tß╗Ł cß╗¦a mß╗Öt nguy├¬n tß╗æ X bß║źt k├¼ trŲ░ß╗øc v├Ā sau phß║Żn ß╗®ng bß║▒ng nhau
Hß║¦u hß║┐t tß║źt cß║Ż c├Īc dß║Īng b├Āi tß║Łp ─æß╗üu c├│ thß╗ā sß╗Ł dß╗źng phŲ░ŲĪng ph├Īp bß║Żo to├Ān nguy├¬n tß╗æ, ─æß║Ęc biß╗ćt l├Ā c├Īc dß║Īng b├Āi hß╗Śn hß╗Żp nhiß╗üu chß║źt, xß║Ży ra biß║┐n ─æß╗Ģi phß╗®c tß║Īp. ThŲ░ß╗Øng sß╗Ł dß╗źng trong c├Īc trŲ░ß╗Øng hß╗Żp sau:
+ Tß╗½ nhiß╗üu chß║źt ban ─æß║¦u tß║Īo th├Ānh sß║Żn phß║®m
Tß╗½ dß╗» kiß╗ćn ─æß╗ü b├Āi ŌćÆ sß╗æ mol cß╗¦a nguy├¬n tß╗æ X trong c├Īc chß║źt ban ─æß║¦u ŌćÆ tß╗Ģng sß╗æ mol trong sß║Żn phß║®m ŌćÆ sß╗æ mol sß║Żn phß║®m
+ Tß╗½ mß╗Öt chß║źt ban ─æß║¦u tß║Īo th├Ānh hß╗Śn hß╗Żp nhiß╗üu sß║Żn phß║®m
Tß╗½ dß╗» kiß╗ćn ─æß╗ü b├Āi ŌćÆ Tß╗Ģng sß╗æ mol ban ─æß║¦u, sß╗æ mol cß╗¦a c├Īc hß╗Żp phß║¦n ─æ├Ż cho ŌćÆ sß╗æ mol chß║źt cß║¦n x├Īc ─æß╗ŗnh
+ Tß╗½ nhiß╗üu chß║źt ban ─æß║¦u tß║Īo th├Ānh nhiß╗üu sß║Żn phß║®m
─Éß╗æi vß╗øi dß║Īng b├Āi n├Āy kh├┤ng cß║¦n thiß║┐t phß║Żi t├¼m ch├Łnh x├Īc sß╗æ mol cß╗¦a tß╗½ng chß║źt, chß╗ē quan t├óm: \(\sum\limits_{}^{} {{n_X}(tr) = \sum\limits_{}^{} {{n_X}(sau)} } \) ( chß╗ē quan t├óm ─æß║┐n tß╗Ģng sß╗æ mol cß╗¦a c├Īc nguy├¬n tß╗æ trŲ░ß╗øc v├Ā sau phß║Żn ß╗®ng)
+ ─Éß╗æt ch├Īy ─æß╗ā ph├ón t├Łch th├Ānh phß║¦n nguy├¬n tß╗æ cß╗¦a hß╗Żp chß║źt
Ch├║ ├Į:
+ Hß║Īn chß║┐ viß║┐t phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng m├Ā viß║┐t sŲĪ ─æß╗ō phß║Żn ß╗®ng biß╗āu diß╗ģn sß╗▒ biß║┐n ─æß╗Ģi cß╗¦a nguy├¬n tß╗æ ─æang cß║¦n quan t├óm
+ Tß╗½ sß╗æ mol cß╗¦a nguy├¬n tß╗æ ch├║ng ta quan t├óm sß║Į t├Łnh ra ─æŲ░ß╗Żc sß╗æ mol cß╗¦a c├Īc chß║źt
+ Sß╗æ mol nguy├¬n tß╗æ trong hß╗Żp chß║źt bß║▒ng sß╗æ nguy├¬n tß╗Ł cß╗¦a nguy├¬n tß╗æ ─æ├│ trong hß╗Żp chß║źt nh├ón vß╗øi sß╗æ mol hß╗Żp chß║źt chß╗®a nguy├¬n tß╗æ ─æ├│
Giß║Ż sß╗Ł ta c├│ hß╗Żp chß║źt AxBy c├│ sß╗æ mol l├Ā a (mol).
Khi ─æ├│ sß╗æ mol nguy├¬n tß╗æ A v├Ā B trong hß╗Żp chß║źt l├Ā: nA = ax (mol) v├Ā nB = ay (mol)
PhŲ░ŲĪng ph├Īp 5: PhŲ░ŲĪng ph├Īp chß╗Źn ─æß║Īi lŲ░ß╗Żng th├Łch hß╗Żp trong h├│a hß╗Źc
1. Nội dung
C├│ mß╗Öt sß╗æ b├Āi to├Īn tŲ░ß╗¤ng nhŲ░ thiß║┐u dß╗» kiß╗ćn g├óy bß║┐ tß║»c cho viß╗ćc t├Łnh to├Īn v├¼ vß║Ły ta phß║Żi tß╗▒ chß╗Źn mß╗Öt ─æß║Īi lŲ░ß╗Żng ph├╣ hß╗Żp ─æß╗ā phß╗źc vß╗ź cho viß╗ćc giß║Żi to├Īn
2. Phß║Īm vi sß╗Ł dß╗źng
Khi ch├║ng ta gß║Ęp b├Āi to├Īn c├│ dß║Īng: ─Éß╗ü b├Āi cho dŲ░ß╗øi dß║Īng tß╗Ģng qu├Īt ( kh├┤ng c├│ gi├Ī trß╗ŗ x├Īc ─æß╗ŗnh) hoß║Ęc cho tß╗ē lß╗ć thß╗ā t├Łch tß╗ē lß╗ć sß╗æ mol c├Īc chß║źt
+ Chß╗Źn mol nguy├¬n tß╗Ł hoß║Ęc ph├ón tß╗Ł chß║źt tham gia
+ Chß╗Źn mß╗Öt mol hß╗Śn hß╗Żp c├Īc chß║źt tham gia phß║Żn ß╗®ng
+ Chß╗Źn ─æ├║ng tß╗ē lß╗ć lŲ░ß╗Żng chß║źt trong ─æß║¦u b├Āi ─æ├Ż cho
+ Chß╗Źn cho th├┤ng sß╗æ mß╗Öt gi├Ī trß╗ŗ ph├╣ hß╗Żp ─æß╗ā ─æŲĪn giß║Żn ph├®p t├Łnh
PhŲ░ŲĪng ph├Īp 6: PhŲ░ŲĪng ph├Īp ─æß╗ō thß╗ŗ trong h├│a hß╗Źc
C├Īc dß║Īng b├Āi sß╗Ł dß╗źng khß║Żo s├Īt ─æß╗ō thß╗ŗ:
+ B├Āi to├Īn cho CO2 (SO2) t├Īc dß╗źng vß╗øi dung dß╗ŗch Ca(OH)2 hoß║Ęc Ba(OH)2
PhŲ░ŲĪng tr├¼nh:
CO2 + 2OH- ŌåÆ CO32- + H2O
Khi CO2 dŲ░ tiß║┐p tß╗źc xß║Ży ra phß║Żn ß╗®ng
CO2 + CO32- ŌåÆ HCO3-
.png?enablejsapi=1)
- Hiß╗ćn tŲ░ß╗Żng: Xuß║źt hiß╗ćn kß║┐t tß╗¦a t─āng dß║¦n ─æß║┐n cß╗▒c ─æß║Īi, sau ─æ├│ tan dß║¦n ─æß║┐n hß║┐t
- nŌåō cß╗▒c ─æß║Īi = a = nCO2
- Nß║┐u 0 < nŌåō < a ŌćÆ C├│ 2 gi├Ī trß╗ŗ cß╗¦a CO2
TH1: CO2 thiß║┐u tß║Īo kß║┐t tß╗¦a chŲ░a cß╗▒c ─æß║Īi: nCO2 = a
TH2: CO2 dŲ░ tß║Īo kß║┐t tß╗¦a cß╗▒c ─æß║Īi sau ─æ├│ h├▓a tan kß║┐t tß╗¦a:
nCO2 = 2a ŌĆō n Ōåō= nOH- - n Ōåō
+ B├Āi to├Īn li├¬n quan tß╗øi muß╗æi Al3+ t├Īc dß╗źng vß╗øi OH-
PhŲ░ŲĪng tr├¼nh:
Al3+ + 3OH- ŌåÆ Al(OH)3
Nß║┐u OH- dŲ░ tiß║┐p tß╗źc xß║Ży ra phß║Żn ß╗®ng:
Al(OH)3 + OH- ŌåÆ AlO2- + 2H2O
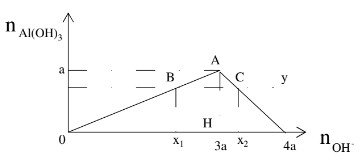
- Hiß╗ćn tŲ░ß╗Żng: Xuß║źt hiß╗ćn kß║┐t tß╗¦a t─āng dß║¦n ─æß║┐n cß╗▒c ─æß║Īi sau ─æ├│ tan dß║¦n ─æß║┐n hß║┐t
- nŌåōcß╗▒c ─æß║Īi = a khi ─æ├│ nOH- = 3a
- Nß║┐u 0 < nŌåō < a th├¼ c├│ 2 trŲ░ß╗Øng hß╗Żp cß╗¦a OH-
TH1: nŌåō tß║Īo ra chŲ░a cß╗▒c ─æß║Īi nOH- = 3nŌåō;
TH2: nŌåō ─æß║Īt cß╗▒c ─æß║Īi sau ─æ├│ lß║Īi tan khi ─æ├│ nOH- = 4a ŌĆō nŌåō
+ Muß╗æi AlO2- t├Īc dß╗źng vß╗øi dung dß╗ŗch H+
PhŲ░ŲĪng tr├¼nh:
AlO2- + H+ + H2O ŌåÆ Al(OH)3
Khi H+ dŲ░ tiß║┐p tß╗źc xß║Ży ra phß║Żn ß╗®ng:
Al(OH)3 + 3H+ ŌåÆ Al3+ + 3H2O
- Hiß╗ćn tŲ░ß╗Żng: Xuß║źt hiß╗ćn kß║┐t tß╗¦a t─āng dß║¦n ─æß║┐n cß╗▒c ─æß║Īi, sau ─æ├│ tan cho ─æß║┐n hß║┐t
- nŌåōcß╗▒c ─æß║Īi = a khi ─æ├│ nH+ = a
- 0 < n Ōåō < a khi ─æ├│ c├│ 2 trŲ░ß╗Øng hß╗Żp:
TH1: Kß║┐t tß╗¦a chŲ░a ─æß║Īt cß╗▒c ─æß║Īi: nŌåō = nH+
TH2: Kß║┐t tß╗¦a ─æß║Īt cß╗▒c ─æß║Īi sau ─æ├│ bß╗ŗ H+ h├▓a tan: nH+ = 4a ŌĆō 3nŌåō
PhŲ░ŲĪng ph├Īp 7: PhŲ░ŲĪng ph├Īp ─æŲ░ß╗Øng ch├®o trong h├│a hß╗Źc
1. Nội dung
+ PhŲ░ŲĪng ph├Īp n├Āy ├Īp dß╗źng cho c├Īc b├Āi to├Īn hß╗Śn hß╗Żp chß╗®a 2 th├Ānh phß║¦n m├Ā y├¬u cß║¦u cß╗¦a b├Āi l├Ā x├Īc ─æß╗ŗnh tß╗ē lß╗ć giß╗»a 2 th├Ānh phß║¦n ─æ├│.
+ Ta c├│ thß╗ā sß╗Ł dß╗źng ─æß║Ęt ß║®n ŌĆō giß║Żi hß╗ć ─æß╗ā thay thß║┐ cho phŲ░ŲĪng ph├Īp ─æŲ░ß╗Øng ch├®o, tuy nhi├¬n ├Īp dß╗źng ─æŲ░ß╗Øng ch├®o hß╗Żp l├Ł, ─æ├║ng c├Īch trong nhiß╗üu b├Āi to├Īn sß║Į gi├║p tß╗æc ─æß╗Ö l├Ām b├Āi nhanh hŲĪn.
2. Phß║Īm vi sß╗Ł dß╗źng
+ B├Āi to├Īn vß╗ü ─æß╗ōng vß╗ŗ: Ta ├Īp dß╗źng sŲĪ ─æß╗ō ─æŲ░ß╗Øng ch├®o cho ─æß║Īi lŲ░ß╗Żng khß╗æi lŲ░ß╗Żng ph├ón tß╗Ł v├Ā sß╗æ khß╗æi
+ B├Āi to├Īn hß╗Śn hß╗Żp kh├Ł: Ta ├Īp dß╗źng sŲĪ ─æß╗ō ─æŲ░ß╗Øng ch├®o cho tß╗ē lß╗ć mol tŲ░ŲĪng ß╗®ng vß╗øi tß╗ē lß╗ć ch├¬nh lß╗ćch ph├ón tß╗Ł khß╗æi c├Īc chß║źt so vß╗øi gi├Ī trß╗ŗ trung b├¼nh
+ B├Āi to├Īn pha chß║┐: Ta ├Īp dß╗źng sŲĪ ─æß╗ō ─æŲ░ß╗Øng ch├®o cho c├Īc ─æß║Īi lŲ░ß╗Żng C%, CM, d,ŌĆ”
+ B├Āi to├Īn x├Īc ─æß╗ŗnh c├┤ng thß╗®c, t├Łnh tß╗ē lß╗ć c├Īc chß║źt: Ta ├Īp dß╗źng cho c├Īc ─æß║Īi lŲ░ß╗Żng, ph├ón tß╗Ł khß╗æi trung b├¼nh, sß╗æ nguy├¬n tß╗Ł trung b├¼nh,ŌĆ”
PhŲ░ŲĪng ph├Īp 8: PhŲ░ŲĪng ph├Īp trung b├¼nh trong h├│a hß╗Źc
1. Nội dung
Giß║Ż sß╗Ł hß╗Śn hß╗Żp gß╗ōm c├Īc phß║¦n tß╗Ł A1,A2,A3,... c├│ khß╗æi lŲ░ß╗Żng mol lß║¦n lŲ░ß╗Żt l├Ā M1, M2, M3,ŌĆ”c├│ sß╗æ mol mß╗Śi phß║¦n tß╗Ł lß║¦n lŲ░ß╗Żt l├Ā a1, a2, a3... hoß║Ęc ta c├│ phß║¦n tr─ām sß╗æ mol mß╗Śi phß║¦n tß╗Ł l├Ā x1, x2, x3,....
Ta sß║Į t├Łnh ─æŲ░ß╗Żc khß╗æi lŲ░ß╗Żng mol trung b├¼nh ( ) theo c├┤ng thß╗®c:
\(\overline M = \frac{{{M_1}{a_1} + {M_2}{a_2} + {M_3}{a_3} + ...}}{{{a_1} + {a_2} + {a_3} + ...}}\)
Hay \(\overline M = {M_1}{x_1} + {M_2}{x_2} + {M_3}{x_3} + ...\) ( vß╗øi x1 + x2 + x3 = 100%)
2. Phß║Īm vi sß╗Ł dß╗źng
+ B├Āi to├Īn c├│ nhiß╗üu hß╗Śn hß╗Żp c├│ t├Łnh chß║źt h├│a hß╗Źc tŲ░ŲĪng tß╗▒ nhau
Thay v├¼ ta viß║┐t nhiß╗üu phŲ░ŲĪng tr├¼nh h├│a hß╗Źc cho nhiß╗üu chß║źt, th├¼ ta gß╗Źi c├┤ng thß╗®c trung b├¼nh v├Ā viß║┐t mß╗Öt phŲ░ŲĪng tr├¼nh ─æß║Īi diß╗ćn
+ B├Āi to├Īn x├Īc ─æß╗ŗnh th├Ānh phß║¦n %
+ B├Āi to├Īn x├Īc ─æß╗ŗnh nguy├¬n tß╗æ, c├┤ng thß╗®c ph├ón tß╗Ł
Ch├║ ├Į:
- Mß╗Öt sß╗æ b├Āi tß║Łp thŲ░ß╗Øng c├│ sß╗▒ kß║┐t hß╗Żp giß╗»a phŲ░ŲĪng ph├Īp trung b├¼nh v├Ā phŲ░ŲĪng ph├Īp ─æŲ░ß╗Øng ch├®o ─æß╗ā r├║t ngß║»n thß╗Øi gian t├Łnh to├Īn.
- Vß╗øi mß╗Źi gi├Ī trß╗ŗ trung b├¼nh ta lu├┤n c├│ hß╗ć thß╗®c \({M_{\min }} \le \overline M \le {M_{\max }}\,({M_{min}},{M_{max}}\) lß║¦n lŲ░ß╗Żt l├Ā gi├Ī trß╗ŗ nhß╗Å nhß║źt v├Ā lß╗øn nhß║źt cß╗¦a ─æß║Īi lŲ░ß╗Żng mang gi├Ī trß╗ŗ trung b├¼nh).
- Nß║┐u c├Īc chß║źt trong hß╗Śn hß╗Żp c├│ sß╗æ mol bß║▒ng nhau ŌćÆ G├Ła trß╗ŗ trung b├¼nh bß║▒ng trung b├¼nh cß╗Öng v├Ā ngŲ░ß╗Żc lß║Īi
PhŲ░ŲĪng ph├Īp 9: PhŲ░ŲĪng ph├Īp quy ─æß╗Ģi trong h├│a hß╗Źc
1. Nội dung
Quy ─æß╗Ģi l├Ā phŲ░ŲĪng ph├Īp biß║┐n ─æß╗Ģi to├Īn hß╗Źc ─æŲ░a b├Āi to├Īn ban ─æß║¦u vß╗øi mß╗Öt hß╗Śn hß╗Żp c├Īc chß║źt phß╗®c tß║Īp trß╗¤ th├Ānh mß╗Öt b├Āi to├Īn ─æŲĪn giß║Żn hŲĪn, qua ─æ├│ l├Ām c├Īc ph├®p t├Łnh trß╗¤ n├¬n ngß║»n gß╗Źn, dß╗ģ d├Āng.
2. Phß║Īm vi sß╗Ł dß╗źng
Khi gß║Ęp c├Īc b├Āi to├Īn hß╗Śn hß╗Żp nhiß╗üu chß║źt nhŲ░ng bß║Żn chß║źt chß╗ē gß╗ōm 2 ( hoß║Ęc 3) nguy├¬n tß╗æ:
+ B├Āi to├Īn vß╗ü hß╗Śn hß╗Żp hß╗Żp chß║źt cß╗¦a Fe, Cu,ŌĆ”
+ B├Āi to├Īn vß╗ü hß╗Śn hß╗Żp ─æß╗ōng ─æß║│ng, thß╗¦y ph├ón h├│a, hi─æro h├│a, ankan h├│a,ŌĆ”
Ch├║ ├Į:
Sß╗æ electron nhŲ░ß╗Øng, nhß║Łn kh├┤ng ─æß╗Ģi
- Trong qu├Ī tr├¼nh t├Łnh to├Īn theo phŲ░ŲĪng ph├Īp quy ─æß╗Ģi ─æ├┤i khi ta gß║Ęp sß╗æ ├óm ─æ├│ l├Ā do sß╗▒ b├╣ trß╗½ khß╗æi lŲ░ß╗Żng cß╗¦a c├Īc chß║źt trong hß╗Śn hß╗Żp. Trong trŲ░ß╗Øng hß╗Żp n├Āy ta vß║½n t├Łnh to├Īn b├¼nh thŲ░ß╗Øng v├Ā kß║┐t quß║Ż cuß╗æi c├╣ng vß║½n thß╗Åa m├Żn.
- Khi giß║Ż ─æß╗ŗnh hß╗Śn hß╗Żp c├Īc chß║źt th├Ānh mß╗Öt chß║źt th├¼ chß║źt ─æ├│ c├│ thß╗ā kh├┤ng c├│ thß╗▒c, hß╗ć sß╗æ cß╗¦a c├Īc nguy├¬n tß╗Ł trong c├┤ng thß╗®c c├│ thß╗ā kh├┤ng phß║Żi l├Ā sß╗æ tß╗▒ nhi├¬n m├Ā c├│ thß╗ā l├Ā sß╗æ thß║Łp ph├ón dŲ░ŲĪng.
- PhŲ░ŲĪng ph├Īp quy ─æß╗Ģi mß║Ęc d├╣ ─æŲ░ß╗Żc coi l├Ā phŲ░ŲĪng ph├Īp rß║źt hay d├╣ng ─æß╗ā giß║Żi quyß║┐t mß╗Öt sß╗æ b├Āi to├Īn li├¬n quan ─æß║┐n Fe v├Ā hß╗Żp chß║źt cß╗¦a Fe ... Tuy nhi├¬n nß║┐u chß╗ē ├Īp dß╗źng phŲ░ŲĪng ph├Īp quy ─æß╗Ģi th├¼ ta kh├┤ng thß╗ā giß║Żi to├Īn n├¬n khi ├Īp dß╗źng phŲ░ŲĪng ph├Īp quy ─æß╗Ģi ta cß║¦n phß║Żi kß║┐t hß╗Żp vß╗øi c├Īc phŲ░ŲĪng ph├Īp kh├Īc nhŲ░:
+ ─Éß╗ŗnh luß║Łt bß║Żo to├Ān khß╗æi lŲ░ß╗Żng
+ ─Éß╗ŗnh luß║Łt bß║Żo to├Ān nguy├¬n tß╗æ
+ ─Éß╗ŗnh luß║Łt bß║Żo to├Ān electron
+ ─Éß╗ŗnh luß║Łt bß║Żo to├Ān ─æiß╗ćn t├Łch
PhŲ░ŲĪng ph├Īp 10: PhŲ░ŲĪng ph├Īp sß╗Ł dß╗źng phŲ░ŲĪng tr├¼nh ion thu gß╗Źn trong h├│a hß╗Źc
1. Nội dung
PhŲ░ŲĪng tr├¼nh h├│a hß╗Źc thŲ░ß╗Øng ─æŲ░ß╗Żc viß║┐t dŲ░ß╗øi hai dß║Īng l├Ā phŲ░ŲĪng tr├¼nh h├│a hß╗Źc ß╗¤ dß║Īng ph├ón tß╗Ł v├Ā dß║Īng ion r├║t gß╗Źn. Ngo├Āi viß╗ćc thß╗ā hiß╗ćn ─æ├║ng bß║Żn chß║źt cß╗¦a phß║Żn ß╗®ng h├│a hß╗Źc, phŲ░ŲĪng tr├¼nh ion thu gß╗Źn c├▓n gi├║p giß║Żi nhanh rß║źt nhiß╗üu dß║Īng b├Āi tß║Łp kh├│a hß╗Źc kh├┤ng thß╗ā giß║Żi theo c├Īc phŲ░ŲĪng tr├¼nh h├│a hß╗Źc ß╗¤ dß║Īng ph├ón tß╗Ł.
2. Phß║Īm vi sß╗Ł dß╗źng
V├¼ ─æß╗ā r├║t gß╗Źn phŲ░ŲĪng tr├¼nh ph├ón tß╗Ł th├Ānh phŲ░ŲĪng tr├¼nh ion r├║t gß╗Źn ta sß╗Ł dß╗źng cho c├Īc chß║źt ─æiß╗ćn li mß║Īnh, do vß║Ły phŲ░ŲĪng ph├Īp n├Āy ├Īp dß╗źng chß╗¦ yß║┐u cho c├Īc chß║źt axit bazŲĪ, muß╗æi trong v├┤ cŲĪ ( c├Īc chß║źt hß╗»u cŲĪ thŲ░ß╗Øng l├Ā chß║źt ─æiß╗ćn li yß║┐u)
+ Phß║Żn ß╗®ng axit, bazŲĪ v├Ā x├Īc ─æß╗ŗnh pH cß╗¦a dung dß╗ŗch
+ B├Āi to├Īn CO2 , SO2 t├Īc dß╗źng vß╗øi dung dß╗ŗch bazŲĪ
+ B├Āi to├Īn li├¬n quan tß╗øi oxit, hi─æroxit lŲ░ß╗Īng t├Łnh
+ B├Āi to├Īn chß║źt khß╗Ł t├Īc dß╗źng vß╗øi dung dß╗ŗch chß╗®a H+ v├Ā NO3-
+ C├Īc phß║Żn ß╗®ng ß╗¤ dß║Īng ion thu gß╗Źn tß║Īo ra chß║źt kß║┐t tß╗¦a, chß║źt dß╗ģ bay hŲĪi, chß║źt ─æiß╗ćn li yß║┐u
PhŲ░ŲĪng ph├Īp 11: PhŲ░ŲĪng ph├Īp t─āng giß║Żm khß╗æi lŲ░ß╗Żng trong h├│a hß╗Źc
1. Nội dung
+ Mß╗Źi sß╗▒ biß║┐n ─æß╗Ģi h├│a hß╗Źc ( ─æŲ░ß╗Żc m├┤ tß║Ż bß║▒ng phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng) ─æß╗üu c├│ li├¬n quan ─æß║┐n t─āng hoß║Ęc giß║Żm khß╗æi lŲ░ß╗Żng.
+ Dß╗▒a v├Āo sß╗▒ t─āng hoß║Ęc giß║Żm khß╗æi lŲ░ß╗Żng khi chuyß╗ān 1 mol chß║źt X th├Ānh 1 hoß║Ęc nhiß╗üu mol chß║źt Y ( c├│ thß╗ā qua c├Īc giai ─æoß║Īn trung gian) ta dß╗ģ d├Āng t├Łnh ─æŲ░ß╗Żc sß╗æ mol cß╗¦a c├Īc chß║źt v├Ā ngŲ░ß╗Żc lß║Īi. tß╗½ sß╗æ mol hoß║Ęc quan hß╗ć sß╗æ mol cß╗¦a c├Īc chß║źt ta sß║Į biß║┐t ─æŲ░ß╗Żc sß╗▒ t─āng giß║Żm khß╗æi lŲ░ß╗Żng cß╗¦a c├Īc chß║źt X,Y.
Ch├║ ├Į:
+ X├Īc ─æß╗ŗnh ─æ├║ng mß╗æi li├¬n hß╗ć tß╗ē lß╗ć giß╗»a c├Īc chß║źt ─æ├Ż biß║┐t vß╗øi chß║źt cß║¦n x├Īc ─æß╗ŗnh, sß╗Ł dß╗źng ─æß╗ŗnh luß║Łt bß║Żo to├Ān nguy├¬n tß╗æ ─æß╗ā x├Īc ─æß╗ŗnh ch├Łnh x├Īc tß╗ē lß╗ć n├Āy
+ X├Īc ─æß╗ŗnh khi chuyß╗ān tß╗½ chß║źt X th├Ānh Y ( hoß║Ęc ngŲ░ß╗Żc lß║Īi) th├¼ khß╗æi lŲ░ß╗Żng t─āng l├¬n hoß║Ęc giß║Żm ─æi theo tß╗ē lß╗ć phß║Żn ß╗®ng v├Ā theo ─æß╗ü b├Āi cho
+ Lß║Łp phŲ░ŲĪng tr├¼nh to├Īn hß╗Źc ─æß╗ā giß║Żi
2. Phß║Īm vi sß╗Ł dß╗źng
+ C├Īc b├Āi to├Īn hß╗Śn hß╗Żp nhiß╗üu chß║źt.
+ ChŲ░a biß║┐t r├Ą phß║Żn ß╗®ng xß║Ży ra ho├Ān to├Ān hay kh├┤ng ho├Ān to├Ān
+ C├Īc b├Āi to├Īn li├¬n quan ─æß║┐n phß║Żn ß╗®ng thß║┐
+ C├Īc b├Āi to├Īn vß╗ü nhiß╗ćt luyß╗ćn
...
Tr├¬n ─æ├óy l├Ā tr├Łch ─æoß║Īn nß╗Öi dung 11 PhŲ░ŲĪng ph├Īp giß║Żi nhanh b├Āi tß║Łp H├│a hß╗Źc hß╗»u cŲĪ, v├┤ cŲĪ. ─Éß╗ā xem th├¬m nhiß╗üu t├Āi liß╗ću tham khß║Żo hß╗»u ├Łch kh├Īc c├Īc em vui l├▓ng ─æ─āng nhß║Łp v├Āo trang hoc247.net ─æß╗ā tß║Żi t├Āi liß╗ću vß╗ü m├Īy t├Łnh.
Ch├║c c├Īc em hß╗Źc tß║Łp tß╗æt !
TŲ░ liß╗ću nß╗Ģi bß║Łt tuß║¦n
- Xem thêm






