Bài tập 40.13 trang 64 SBT Hóa học 11
Hỗn hợp A chứa 2 ancol no, đơn chức, mạch hở. Để đốt cháy hoàn toàn hỗn hợp A cần dùng vừa hết 3,36 lít O2 (đktc). Trong sản phẩm cháy, khối lượng CO2 nhiều hơn khối lượng H2O là 1,88 g.
1. Xác định khối lượng hỗn hợp A.
2. Xác định công thức phân tử và phần trăm khối lượng của từng chất trong A nếu biết thêm rằng hai ancol đó khác nhau 2 nguyên tử cacbon.
Hướng dẫn giải chi tiết bài 40.13
Cách 1.
1. Hỗn hợp A gồm X mol CnH2n+1OH và y mol CmH2m+1OH.
Khối lượng hỗn hợp A là :
(14n + 18)x + (14m + 18)y = 14 (nx + my) + 18(x + y)
CnH2n+1OH + 1,5nO2 → nCO2 + (n+1) H2O
x mol 1,5nxmol nx mol (n + 1)x mol
CmH2m+1OH + 1,5mO2 → mCO2 + (m+1)H2O
y mol 1,5my mol my mol (m + 1)y mol
Số mol O2 là: \(\frac{3}{2}.({n_x} + {m_y}) = \frac{{3,36}}{{22,4}} = 0,15 \to nx + my = 0,1\,\,\,(1)\)
Hiệu khối lượng của CO2 và của H2O :
44(nx + my) - 18[(n + 1)x + (m + 1)y] = 1,88
26(nx + my) - 18(x + y) = 1,88 (2)
Từ (1) và (2), tìm được : x + y = 0,04.
Khối lượng hỗn hợp A là : 14.0,1 + 18.0,04 = 2,12 (g).
2. Vì m = n + 2 ; ta có : nx + (n + 2)y = 0,1
n(x + y) + 2y = 0,1 y = 0,05 - 0,02n
0 < y < 0,04 0,5 < n < 2,5
Nếu n=1, hai ancoỉ là CH3OH và C3H7OH
y = 0,03 và x = 0,01
CH3OH chiếm 15,1% ; C3H7OH chiếm 84,9% khối lượng hỗn hợp A.
Nếu n=2, hai ancol là C2H5OH và C4H9OH
y = 0,01 và x = 0,03
C2H5OH chiếm 65,1%, C4H9OH chiếm 84,9% khối lượng hỗn hợp A.
Cách 2.
1. Công thức chung của hai ancol là CnH2n+1OH và tổng số mol của chúng là a. Khối lượng hỗn hợp : (14n + 18)a.
CnH2n+1OH + 1,5nO2 → nCO2 + (n+1)H2O
a mol 1,5na mol mol (n+1)a mol
\(\left\{ \begin{array}{l}
1,5na = 0,15\\
44na - 18(n + 1)a = 1,88
\end{array} \right. \to \left\{ \begin{array}{l}
n = 2,5\\
a = 0,04
\end{array} \right.\)
Khối lượng hỗn hợp : (14.2,5 + 18).0,04 = 2,12 (g)
2. n < 2,5 < n + 2 0,5 < n < 2,50
Phần cuối giống như ở cách giải 1.
-- Mod Hóa Học 11 HỌC247
-


Một ancol no đơn chức có %H = 13,04% về khối lượng. CTPT của ancol là
A. C6H5CH2OH
B. CH3OH
C. C2H5OH
D. CH2=CHCH2OH
Theo dõi (0) 1 Trả lời -


Một ancol no có công thức thực nghiệm là (C2H5O)n. CTPT của ancol có thể là
bởi Nguyễn Minh Minh
 27/05/2020
27/05/2020
A. C2H5O
B. C4H10O2
C. C4H10O
D. C6H15O3
Theo dõi (0) 1 Trả lời -


Đun nóng một ancol X với H2SO4 đặc ở nhiệt độ thích hợp thu được một olefin duy nhất. Công thức tổng quát của X là (với n > 0, n nguyên)
bởi Hoang Viet
 27/05/2020
27/05/2020
A. CnH2n + 1OH
B. ROH
C. CnH2n + 2O
D. CnH2n + 1CH2OH
Theo dõi (0) 1 Trả lời -


Gọi tên ancol CH3CH2OH?
bởi Dũng Hoàng Art
 27/05/2020
Gọi tên ancolTheo dõi (0) 0 Trả lời
27/05/2020
Gọi tên ancolTheo dõi (0) 0 Trả lời -


Gọi tên (CH3)2CH-CH2-CH2OH?
bởi Linh Nguyen
 25/05/2020
Gọi tên ancolTheo dõi (0) 1 Trả lời
25/05/2020
Gọi tên ancolTheo dõi (0) 1 Trả lời -


Tính số mol của ancol?
bởi Thái Xuân Trúc Giang
 23/05/2020
Dạ cho em hỏi là em thấy bth khi tính số mol là phải lấy m/M nhưng tại sao ở đây lại là M/m vậy ạ
23/05/2020
Dạ cho em hỏi là em thấy bth khi tính số mol là phải lấy m/M nhưng tại sao ở đây lại là M/m vậy ạ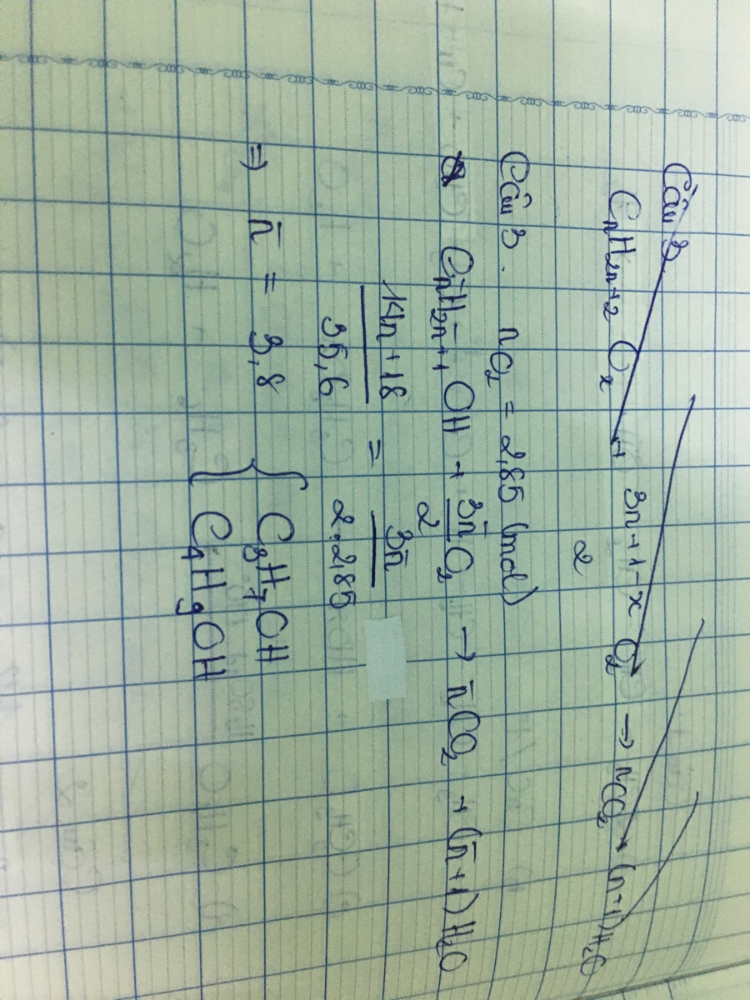 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Hỗn hợp X gồm 2 chất hữu cơ thuộc cùng dãy đồng đẳng. Phân tử của chúng chỉ có một loại nhóm chức. Chia X làm 2 phần bằng nhau.
bởi Bao Chau
 23/05/2020
23/05/2020
- Phần 1: Đem đốt cháy hoàn toàn rồi cho toàn bộ sản phẩm cháy (chỉ có CO2 và hơi H2O) lần lượt qua bình (l) đựng dung dịch H2SO4 đặc, bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (l) tăng 2,16 gam, ở bình (2) có 7 gam kết tủa.
- Phần 2: Cho tác dụng hết với Na dư thì thể tích khí H2 (đktc) thu được là bao nhiêu?
A. 2,24 lít
B. 0,224 lít
C. 0,56 lít
D. 1,12 lít
Theo dõi (0) 5 Trả lời -


Đốt cháy hoàn toàn m gam một rượu X thu được 1,344 lít CO2 (đktc) và 1,44 gam H2O. X tác dụng với Na dư cho khí H2 có số mol bằng số mol của X. Công thức phân tử của X và giá trị m lần lượt là
bởi bala bala
 23/05/2020
23/05/2020
A. C3H8O2 và 1,52
B. C4H10O2 và 7,28
C. C3H8O2 và 7,28
D. C3H8O3 và 1,52
Theo dõi (0) 5 Trả lời
Bài tập SGK khác
Bài tập 40.11 trang 64 SBT Hóa học 11
Bài tập 40.12 trang 64 SBT Hóa học 11
Bài tập 40.14 trang 64 SBT Hóa học 11
Bài tập 40.15 trang 64 SBT Hóa học 11
Bài tập 40.16 trang 64 SBT Hóa học 11
Bài tập 1 trang 224 SGK Hóa học 11 nâng cao
Bài tập 2 trang 224 SGK Hóa học 11 nâng cao
Bài tập 3 trang 224 SGK Hóa học 11 nâng cao
Bài tập 4 trang 224 SGK Hóa học 11 nâng cao
Bài tập 5 trang 224 SGK Hóa học 11 nâng cao
Bài tập 6 trang 224 SGK Hóa học 11 nâng cao
Bài tập 1 trang 228 SGK Hóa học 11 nâng cao
Bài tập 2 trang 229 SGK Hóa học 11 nâng cao
Bài tập 3 trang 229 SGK Hóa học 11 nâng cao
Bài tập 4 trang 229 SGK Hóa học 11 nâng cao
Bài tập 5 trang 229 SGK Hóa học 11 nâng cao
Bài tập 6 trang 229 SGK Hóa học 11 nâng cao





