Nội dung bài học Cacbon tìm hiểu vị trí của cacbon trong bảng tuần hoàn các nguyên tố hoá học, cấu hình electron nguyên tử, các dạng thù hình của cacbon, tính chất vật lí (cấu trúc tinh thể, độ cứng, độ dẫn điện), ứng dụng. Cacbon có tính phi kim yếu (oxi hóa hiđro và kim loại canxi), tính khử ( khử oxi, oxit kim loại). Trong một số hợp chất, cacbon thường có số oxi hóa +2 hoặc +4.
Tóm tắt lý thuyết
1.1. Vị trí và cấu hình electron nguyên tử
- Vị trí: Ô thứ 6, nhóm IVA, chu kì 2
- Cấu hình e: 1s2 2s2 2p2→ Có 4 e lớp ngoài cùng, tạo 4 liên kết cộng hoá trị
- Các số oxi hoá: -4, 0, +2 và +4
1.2. Tính chất vật lí
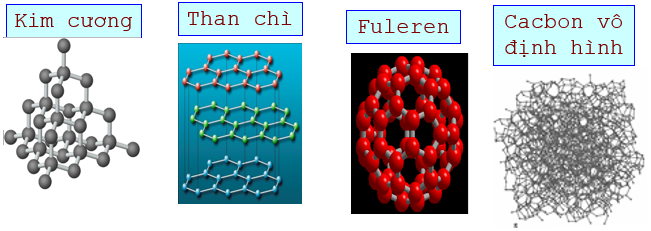
Hình 1: Cấu trúc tinh thể của Kim cương, than chì, Fulere và cacbon vô định hình
|
Dạng thù hình |
Cấu trúc |
Tính chất vật lí |
Ứng dụng |
|
Kim cương |
Tứ diện đều |
Trong suốt, không màu, không dẫn điện, dẫn nhiệt kém |
Đồ trang sức, mũi khoan, dao cắt thuỷ tinh... |
|
Than chì |
Cấu trúc lớp. Các lớp liên kết yếu với nhau |
màu xám đen, dẫn điện tốt, mềm, các lớp dễ tách nhau |
Làm điên cực, làm nồi nấu chảy các hợp kim chịu nhiệt, chế tạo chất bôi trơn, làm bút chì đen |
|
Cacbon vô định hình |
Xốp |
Khả năng hấp phụ mạnh |
Than cốc dùng làm chất khử trong luyện kim; Than hoạt tính dùng trong mặt nạ phòng độc; Than muội dùng làm chất độn cao su, sản xuất mực in, xi đánh giày... |
1.3. Tính chất hóa học
Cacbon vừa thể hiện tính khử vừa thể hiện tính oxi hoá
1.3.1. Tính khử
Tác dụng với oxi
Cacbon cháy trong không khí, toả nhiều nhiệt
\(\mathop C\limits^0 + \mathop {{O_2}}\limits^0\)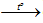
Tác dụng với hợp chất
Ở nhiệt độ cao, cacbon khử được nhiều oxit, nhiều chất oxi hoá khác nhau
Video 1: Cacbon khử Đồng (II) oxit tạo thành CO2 , khí CO2 làm đục nước vôi trong
1.3.2. Tính oxi hoá. Ở nhiệt độ cao
Tác dụng với hiđro
\(\mathop C\limits^0 + 2{H_2}\)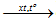
Tác dụng với kim loại
\(4\mathop {Al}\limits^0 + 3\mathop C\limits^0\)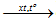
\(\mathop {Ca}\limits^0 + 2\mathop C\limits^0\)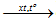
1.4. Trạng thái tự nhiên
Hình 2: Các dạng tồn tại của Cacbon
1.5. Tổng kết
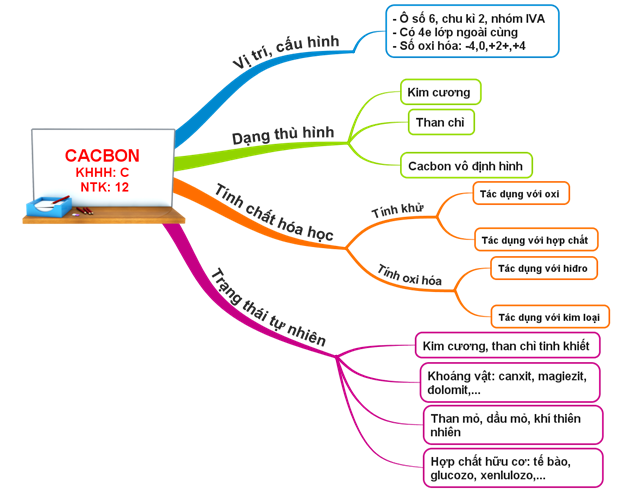
Hình 3: Sơ đồ tư duy Bài Cacbon
2. Luyện tập Bài 15 Hóa học 11
Sau bài học cần nắm:
- Vị trí của cacbon trong bảng tuần hoàn các nguyên tố hoá học, cấu hình electron nguyên tử.
- Các dạng thù hình của cacbon, tính chất vật lí (cấu trúc tinh thể, độ cứng, độ dẫn điện), ứng dụng.
2.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 15 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. Kim cương có cấu trúc tinh thể nguyên tử dạng tứ diện đều, than chì có cấu trúc lớp, trong đó khoảng cách giữa các lớp khá lớn
- B. Kim cương có kiểu liên kết cộng hóa trị bền vững
- C. Than chì có các electron tự do
- D. Một nguyên nhân khác
-
- A. Có cấu tạo mạng tinh thể giống nhau
- B. Có tính chất vật lý tương tự nhau
- C. Đều do nguyên tố các bon tạo nên
- D. Có màu sắc giống nhau
-
- A. 3C + 4Al → Al4C3
- B. C + 2H2 → CH4
- C. C + 2CuO → Cu + CO2
- D. Không có phản ứng nào
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
2.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 15.
Bài tập 1 trang 70 SGK Hóa học 11
Bài tập 2 trang 70 SGK Hóa học 11
Bài tập 3 trang 70 SGK Hóa học 11
Bài tập 4 trang 70 SGK Hóa học 11
Bài tập 5 trang 70 SGK Hóa học 11
Bài tập 15.1 trang 22 SBT Hóa học 11
Bài tập 15.2 trang 22 SBT Hóa học 11
Bài tập 15.3 trang 22 SBT Hóa học 11
Bài tập 15.4 trang 22 SBT Hóa học 11
Bài tập 15.5 trang 22 SBT Hóa học 11
Bài tập 15.6 trang 23 SBT Hóa học 11
Bài tập 15.7 trang 23 SBT Hóa học 11
Bài tập 1 trang 82 SGK Hóa học 11 nâng cao
Bài tập 2 trang 82 SGK Hóa học 11 nâng cao
Bài tập 3 trang 82 SGK Hóa học 11 nâng cao
Bài tập 4 trang 82 SGK Hóa học 11 nâng cao
3. Hỏi đáp về Bài 15 chương 3 Hóa học 11
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.