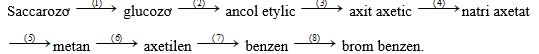Để các em có thêm nhiều tài liệu tham khảo hữu ích chúng tôi xin giới thiệu đến các em học sinh nội dung Đề thi chọn đội tuyển học sinh giỏi môn Hóa học 9- Trường THCS Lý Thái Tổ có đáp án dưới đây. Tài liệu được HOC247 tổng hợp với nội dung các bài tập hay và khó có hướng dẫn giải chi tiết. Mời các em cùng tham khảo.
TRƯỜNG THCS LÝ THÁI TỔ
ĐỀ THI CHỌN ĐỘI TUYỂN HỌC SINH GIỎI
MÔN HÓA HỌC 9
THỜI GIAN: 150 PHÚT
Câu 1: (2,0 điểm)
1. Cho biết A, B, C, D, E là các hợp chất của Natri. Cho A lần lượt tác dụng với các dung dịch B, C thu được các khí tương ứng X, Y. Cho D, E lần lượt tác dụng với nước thu được các khí tương ứng Z, T. Biết X, Y, Z, T là các khí thông thường, chúng tác dụng với nhau từng đôi một. Tỉ khối của X so với Z bằng 2 và tỉ khối của Y so với T cũng bằng 2. Viết tất cả các phương trình phản ứng xảy ra.
2. Cho hỗn hợp gồm 3 chất rắn: Al2O3, SiO2, Fe3O4 vào dung dịch chứa một chất tan A, thì thu được một chất rắn B duy nhất. Hãy cho biết A, B có thể là những chất gì? Cho ví dụ và viết các PTHH minh hoạ.
Câu 2: (2,0 điểm)
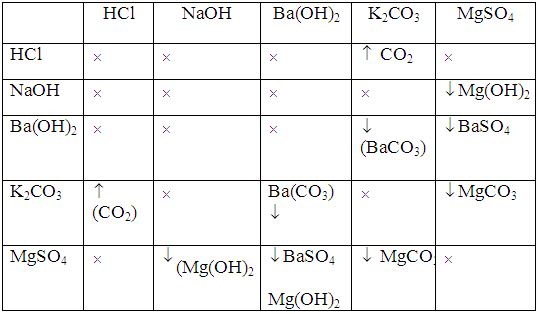
1. Không dùng thêm hóa chất nào khác, bằng phương pháp hóa học hãy phân biệt các dung dịch đựng trong các lọ riêng biệt bị mất nhãn sau: HCl, NaOH, Ba(OH)2, K2CO3, MgSO4.
2. Từ photphat tự nhiên, quặng pirit sắt, nước và chất xúc tác (thiết bị cần thiết khác xem như có đủ). Viết PTHH điều chế supephotphat đơn, supephotphat kép, sắt (III) sunfat.
Câu 3: (2,0 điểm)
Từ nguyên liệu là than đá, đá vôi và các hợp chất vô cơ (thiết bị cần thiết khác xem như có đủ). Viết PTHH điều chế các chất: PVC, Poli Propilen, CH2=CH-COOH và HOCH2-CHOH-CH2OH.
Câu 4: (2,0 điểm)
1. Viết các PTHH theo sơ đồ chuyển hoá sau:
2. Có 3 hỗn hợp khí, mỗi hỗn hợp đều có: SO2, CO2, CH4, C2H2.
Tiến hành thí nghiệm như sau:
- Cho hỗn hợp thứ nhất tác dụng với dung dịch Ca(OH)2 dư.
- Cho hỗn hợp thứ hai tác dụng với dung dịch nước Brom dư.
- Đốt cháy hoàn toàn hỗn hợp thứ ba trong oxi dư.
Nêu hiện tượng hoá học xảy ra trong mỗi thí nghiệm. Viết các phương trình hoá học.
Câu 5: (2,0 điểm)
1. Độ tan của NaCl ở 900C là 50g và ở 00C là 35g. Cho 20g NaCl khan vào 300g dung dịch NaCl bão hòa ở 900C, đun nóng và khuấy đều dung dịch cho NaCl tan hết. Sau đó, đưa dung dịch về 00C thấy tách ra m gam muối.
a. Tính C% của dung dịch NaCl bão hòa ở 00C và ở 900C.
b. Tính m.
2. Tính khối lượng CuSO4.5H2O và khối lượng nước cần lấy để pha chế được 200g dung dịch CuSO4 20%.
Câu 6: (2,0 điểm)
Cho sơ đồ phản ứng sau đây :
Biết A1 gồm các nguyên tố C, H, O, N với tỉ lệ khối lượng tương ứng 3 : 1 : 4 : 7 và trong phân tử A1 có 2 nguyên tử nitơ.
1. Hãy xác định CTHH của A1, A2, A3 và viết các PTHH theo sơ đồ chuyển hoá trên.
2. Chọn chất thích hợp để:
a. Làm khô khí A3.
b. Làm khô khí A4.
Câu 7: (2,0 điểm)
1. Cho hỗn hợp X gồm: Ba, Na, CuO và Fe2O3. Trình bày phương pháp tách thu lấy từng kim loại từ hỗn hợp X và viết các phương trình phản ứng xảy ra.
2. Thủy ngân là một kim loại nặng rất độc. Người bị nhiễm thủy ngân bị run chân tay, run mí mắt, mất ngủ, giảm trí nhớ, rối loạn thần kinh, … thậm trí có thể bị tử vong khi bị nhiễm thủy ngân với nồng độ lớn (từ 100 microgam/m3 trở lên). Thủy ngân độc hơn khi ở thể hơi vì dễ dàng hấp thụ vào cơ thể qua nhiều con đường như: đường hô hấp, đường tiêu hóa, qua da, … Vậy ta cần xử lý như thế nào khi cần thu hồi thủy ngân rơi vãi? Liên hệ với tình huống xử lý an toàn khi vô tình làm vỡ nhiệt kế thủy ngân trong phòng thí nghiệm?
Câu 8: (2,0 điểm)
Trộn CuO với RO (R là kim loại có một hóa trị) theo tỉ lệ số mol tương ứng 1 : 2 thu được hỗn hợp A. Dẫn dòng khí CO dư đi qua ống sứ đựng 9,6 gam hỗn hợp A nung nóng thu được chất rắn B. Hòa tan hết chất rắn B cần dùng vừa đủ 86,9565ml dung dịch HNO3 25,2% (D = 1,15 g/ml) thu được V lít khí NO (đktc).
1. Xác định kim loại R.
2. Tính V.
Câu 9: (2,0 điểm)
Một hỗn hợp A gồm một axit đơn chức, một rượu đơn chức và este đơn chức tạo ra từ hai chất trên. Đốt cháy hoàn toàn 3,06 gam hỗn hợp A cần dùng 4,368 lít khí oxi (đo ở đktc). Khi cho 3,06 gam hỗn hợp A phản ứng hoàn toàn với dung dịch NaOH cần dùng 200ml dung dịch NaOH 0,1 M thu được 1,88 gam muối và m gam hợp chất hữu cơ B. Đun nóng m gam B với axit sunfuric đặc ở 1800C thu được m1 gam B1. Tỉ khối hơi của B1 so vớí B bằng 0,7 (giả thiết hiệu suất đạt 100% ).
1. Xác định công thức cấu tạo B1 và các chất trong A.
2. Tính m, m1.
Câu 10: (2,0 điểm)
1. Trình bày cách khai thác muối ăn đã được học và nêu các ứng dụng của muối NaCl.
2. Trong phòng thí nghiệm, khi điều chế CO2 từ CaCO3 và dung dịch HCl, khí CO2 thu được bị lẫn một ít khí hiđroclorua và hơi nước. Hãy trình bày phương pháp hóa học để thu được khí CO2 tinh khiết. Viết các phương trình hóa học xảy ra.
ĐÁP ÁN
|
Câu |
Hướng dẫn chấm |
Điểm |
|
1 (2,0đ) |
1. X: SO2, Y: H2S, Z : O2, T: NH3 Các chất A, B, C, D, E có công thức lần lượt là: NaHSO4, Na2SO3 hoặc NaHSO3, Na2S, Na2O2, Na3N PTHH: ........ 2. TH1: - Chất tan A là dung dịch kiềm: NaOH; KOH; Ba(OH)2… thì B là Fe3O4. Ví dụ: 2NaOH + Al2O3 → 2 NaAlO2 + H2O 2NaOH + SiO2 → Na2SiO3 + H2O TH2: - Chất tan A là dung dịch axit: HCl; H2SO4… thì B là SiO2. Ví dụ: 6 HCl +Al2O3 → 2AlCl3 + 3H2O 8HCl + Fe3O4 → FeCl2 + 2FeCl3 + 4 H2O |
0,5 PTHH viết đúng 0,5 điểm
0,5
0,5 |
|
2 (2,0đ) |
1. Trích mẫu thử, đánh số thứ tự và tiến hành thí nghiệm. Cho lần lượt các mẫu thử tác dụng với nhau, quan sát hiện tượng. Ta có bảng thí nghiệm: Mẫu thử nào cho kết quả ứng với 1 khí => HCl Mẫu thử nào cho kết quả ứng với 1 kết tủa => NaOH Mẫu thử nào cho kết quả ứng với 2 kết tủa=> Ba(OH)2 Mẫu thử nào cho kết quả ứng với 2 kết tủa và 1 khí => K2CO3 Mẫu thử nào cho kết quả ứng với 3 kết tủa => MgSO4 Các PTHH: 2HCl + K2CO3 → 2KCl + H2O + CO2↑ 2NaOH + MgSO4 → Na2SO4 + Mg(OH)2 Ba(OH)2 + K2CO3 → BaCO3 + 2KOH Ba(OH)2 + MgSO4 → Mg(OH)2 + BaSO4 K2CO3 + MgSO4 → MgCO3 + K2SO4 2. 2H2O \(\xrightarrow{{dien\,phan}}\)2H2 + O2 4FeS2 + 11O2 \(\xrightarrow{{{t^o}}}\)2Fe2O3 + 8SO2 2SO2 + O2 \(\xrightarrow{{{t^o},{V_2}{O_5}}}\) 2SO3 SO3 + H2O → H2SO4 2H2SO4 + Ca3(PO4)2 → Ca(H2PO4)2 + 2CaSO4 3H2SO4 + Ca3(PO4)2 → 3CaSO4 + 2H3PO4 Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2 Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O |
Nhận biết đúng 1,0 điểm
Mỗi PTHH cho 0,125 điểm |
---Để xem đầy đủ nội dung và đáp án của đề thi các em vui lòng xem online hoặc tải về máy---
Trên đây là trích dẫn một phần nội dung tài liệu Đề thi chọn đội tuyển học sinh giỏi môn Hóa học 9- Trường THCS Lý Thái Tổ có đáp án. Để xem thêm nhiều tài liệu tham khảo hữu ích khác các em chọn chức năng xem online hoặc đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Ngoài ra các em học sinh có thể tham khảo các tài liệu cùng chuyên mục:
- Bộ đề thi tuyển chọn học sinh giỏi môn Lịch sử 9 có đáp án chi tiết
- Đề thi học sinh giỏi cấp huyện môn Hóa học 9- Phòng GD & ĐT Ngọc Lặc có đáp án
Chúc các em học tốt!