Đề thi chọn HSG THPT Chuyên và chọn đội tuyển dự thi HSG Quốc Gia môn Hóa học năm 2019-2020 Sở GD&ĐT Quảng Nam được Hoc247 sưu tầm và biên tập, nhằm giúp các em học sinh ôn tập và củng cố lại các kiến thức đã học, đồng thời làm quen với các bài tập ôn luyện đội tuyển HSG, hình thành cơ sở kiến thức vững chắc để các em tự tin bước vào kì thi của mình. Mời các em cùng theo dõi!
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO QUẢNG NAM
|
KỲ THI HỌC SINH GIỎI THPT CHUYÊN VÀ CHỌN ĐỘI TUYỂN DỰ THI HỌC SINH GIỎI QUỐC GIA MÔN HÓA HỌC Năm học 2019-2020 |
Câu I. (2,0 điểm)
I.1. Năm 1888, Rydberg và Ritz đã đưa ra một công thức kinh nghiệm để xác định vị trí của các vạch phổ hiđro bằng sự hấp thụ ánh sáng: \(\frac{1}{\lambda } = R.\left( {\frac{1}{{n_1^2}} - \frac{1}{{n_2^2}}} \right)\)
Trong đó: λ là bước sóng, R là hằng số Rydberg, n1 và n2 là các số tự nhiên.
Năm 1913, Bohr phát triển mô hình nguyên tử hiđro. Mô hình này dựa trên giả thiết nguyên tử có electron chuyển động theo quỹ đạo tròn xác định quanh hạt nhân mà không có sự phát xạ năng lượng. Sự chuyển electron từ quỹ đạo n1 đến n2 kèm theo sự hấp thụ hoặc phát xạ ánh sáng (photon) với bước sóng cụ thể. Thế năng của electron trong trường lực hạt nhân là En = \( - \frac{{{e^2}}}{{4\pi {\varepsilon _o}{r_n}}}\) .
Trong đó: e = 1,6.10-19 C, εo = 8,85.10-12 F/m, rn: bán kính quỹ đạo thứ n và rn = ao.n2 với ao là bán kính quỹ đạo đầu tiên của Bohr. Biết động năng của electron trong nguyên tử hiđro bằng một nửa thế năng và có dấu ngược lại.
Cho hằng số R = 0,01102 nm-1 .
1. Tính năng lượng của 1 mol nguyên tử hiđro ở trạng thái cơ bản.
2. Tính bán kính Bohr ao và khoảng cách ngắn nhất giữa quỹ đạo thứ 2 và thứ 3.
3. Tính năng lượng ion hóa của nguyên tử hiđro.
I.2.
1. Hoàn thành các phản ứng hạt nhân sau:
a. 18O + p → …+ n b. … + \(_1^2{\rm{D}}\) → 18F + a
c. 19F + \(_1^2{\rm{D}}\) → 20F + … d. 16O + … → 18F + p + n
2. Phản ứng (a) ở trên được dùng để tổng hợp 18F (chu kì bán hủy của 18F là 109,7 phút), nguyên liệu sử dụng là nước được làm giàu H218O. Sự có mặt của nước thường H216O dẫn tới phản ứng phụ với 16O và hình thành đồng vị 17F.
a. Tính hiệu suất gắn 18F vào D-glucozơ nếu hoạt độ phóng xạ ban đầu của một mẫu 18F là 600 MBq và hoạt độ phóng xạ của 18F-2-đeoxi-D-glucozơ (FDG) sau khi gắn là 528,3 MBq. Thời gian tổng hợp là 3,5 phút.
b. Thời gian bán hủy sinh học của 18F-2-đeoxi-D-glucozơ là 120 phút. Tính hoạt độ phóng xạ còn lại theo MBq trong bệnh nhân sau một giờ tiêm FDG? Biết hoạt độ phóng xạ ban đầu là 450 MBq.
Câu II.
II.1. Ba nguyên tố flo, clo và oxi tạo thành nhiều hợp chất với nhau:
(a) ClO2F (b) ClOF3 (c) OF2 (d) ClF5 (e) ClF3
1. Với mỗi chất trên hãy viết công thức cấu tạo Lewis, nêu dạng hình học theo mô hình.
2. Xác định trạng thái lai hóa của nguyên tử trung tâm.
|
II.2. Ngày nay Cu2O được sử dụng rộng rãi trong pin mặt trời do giá thành rẻ và không độc hại. Cho hai hình ảnh về mạng tinh thể Cu2O, với hằng số mạng là 427,0 pm. 1. Cho biết nguyên tử nào là nguyên tử Cu (A hay B)? Cho biết kiểu kết tinh cơ bản của các nguyên tử A và các nguyên tử B (lập phương đơn giản, lập phương tâm khối, lập phương tâm mặt, kim cương) và số phối trí của mỗi loại nguyên tử? |
|
2. Tính khối lượng riêng của Cu2O?
3. Một khuyết tật mạng phổ biến của Cu2O là thiếu một vài nguyên tử Cu trong khi mạng tinh thể của oxi không thay đổi. Trong một mẫu nghiên cứu, có 0,2% nguyên tử Cu được tìm thấy ở trạng thái oxi hóa +2. Tính phần trăm vị trí Cu thông thường bị khuyết trong mẫu tinh thể? Cho biết giá trị x trong công thức thực nghiệm của tinh thể Cu2-xO?
Câu III.
III.1. N2O4 là một thành phần quan trọng của nhiên liệu tên lửa. Tại điều kiện thường, NO2 là chất khí, có màu nâu đỏ. Khi làm lạnh NO2, màu nâu đỏ giảm. Ở nhiệt độ sôi (ts = 21oC) chỉ còn màu nâu nhạt và trở nên không màu ở trạng thái rắn. NO2 nằm cân bằng với N2O4 theo phương trình sau:
N2O4(k) ⇔ 2NO2(k); ∆Ho = 57kJ.mol-1; ∆So = 176 J.mol-1.K-1 ở 25oC.
1. Giải thích tại sao: NO2 có màu trong khi N2O4 không màu và sự thay đổi màu sắc khi làm lạnh NO2?
2. Giả sử hỗn hợp có áp suất tổng không đổi là 1 atm và trong khoảng nhiệt độ khảo sát ∆Ho, ∆So không phụ thuộc vào nhiệt độ.
a. Tính áp suất riêng phần của NO2 và N2O4 ở 25oC?
b. Tại nhiệt độ nào thì nồng độ NO2 và N2O4 bằng nhau?
III.2. Nạp 10,0 mmol but-1-in vào một lò phản ứng có thể tích thay đổi được với Vo = 0,1 m3 chỉ chứa không khí ở P = 1,0 atm và T = 298K. Tiến hành đốt cháy hoàn toàn hiđrocacbon này ở điều kiện đoạn nhiệt đẳng áp (là phản ứng duy nhất xảy ra trong điều kiện này). Sau khi đốt cháy hoàn toàn thì trong bình phản ứng chỉ chứa cacbonic, hơi nước, nitơ và oxi.
1. Tính entanpy tiêu chuẩn của phản ứng ở 298K (theo kJ.mol-1). Từ đó suy ra lượng nhiệt tỏa ra tương ứng với số mol but-1-in nạp vào.
2. Tính số mol các chất có trong bình phản ứng sau khi quá trình đốt cháy xảy ra hoàn toàn. Giả sử không khí là hỗn hợp của oxi và nitơ với tỉ lệ mol lần lượt là 1 : 4.
3. Tính nhiệt độ cực đại trong bình sau phản ứng cháy.
Cho các dữ kiện nhiệt động ở điều kiện tiêu chuẩn, 298K.
|
Chất |
C4H6(k) |
CO2(k) |
H2O(k) |
O2(k) |
N2(k) |
|
(kJ.mol-1) |
165,2 |
-393,5 |
-241,8 |
0 |
0 |
|
Cp (J.K-1.mol-1) |
13,5 |
46,6 |
41,2 |
32,2 |
27,6 |
Giả sử các giá trị nhiệt dung và nhiệt tạo thành không phụ thuộc nhiệt độ.
Câu IV.
NO là chất gây ô nhiễm không khí, thường được hình thành chủ yếu từ sấm sét và do quá trình đốt cháy nhiên liệu của động cơ. Ở nhiệt độ cao, NO có thể phản ứng với H2 tạo ra khí N2O là một chất gây ra hiệu ứng nhà kính:
2 NO (k) + H2 (k) ⇔ N2O (k) + H2O (k) (1)
IV.1. Để nghiên cứu động học của phản ứng ở 820oC, tốc độ đầu của phản ứng tại các áp suất ban đầu khác nhau của NO và H2.
|
Thí nghiệm |
Áp suất đầu, torr |
Tốc độ đầu hình thành N2O, torr.s-1 |
|
|
\({P_{NO}}\) |
\({P_{{H_2}}}\) |
||
|
1 |
120,0 |
60,0 |
8,66.10-2 |
|
2 |
60,0 |
60,0 |
2,17.10-2 |
|
3 |
60,0 |
180,0 |
6,62.10-2 |
Bài tập này không sử dụng nồng độ. Dùng đơn vị áp suất là torr, đơn vị thời gian là giây.
1. Viết biểu thức tốc độ phản ứng và tính hằng số tốc độ phản ứng.
2. Tính tốc độ tiêu thụ ban đầu của NO ở 820oC khi hỗn hợp ban đầu có áp suất riêng phần của NO bằng 2,00.102 torr và của H2 bằng 1,00.102 torr.
3. Tính thời gian để áp suất riêng phần của H2 giảm đi một nửa, nếu áp suất ban đầu của NO là 8,00.102 torr và của H2 là 1,0 torr ở 820oC
IV.2. Người ta đề nghị cơ chế sau đây cho phản ứng giữa NO và H2:
2 NO (k) ⇔ N2O2 (k)
N2O2 (k) + H2 (k) → N2O (k) + H2O (k)
1. Sử dụng phương pháp gần đúng trạng thái dừng, từ cơ chế trên hãy rút ra biểu thức của định luật tốc độ cho sự hình thành N2O.
2. Trong điều kiện nào thì định luật tốc độ tìm được có thể đơn giản hóa trở thành định luật tốc độ thực nghiệm ở phần IV.1.
Câu V.
V.1. Một pin nhiên liệu được hình thành khi đốt cháy metanol, chất dẫn điện là dung dịch axit loãng. Thế điện cực chuẩn của pin ở 298K là 1,21V và ở 373K giảm 10mV. Nhiệt độ chuẩn 298K và áp suất 1 bar.
1. Viết các bán phản ứng tại anot và catot. Viết phản ứng tổng quát xảy ra trong pin.
2. Sử dụng phương trình Van’t Hoff, hãy tính ∆Ho và ∆So của phản ứng trong pin metanol ở 298K với hệ số nguyên tối giản ở phản ứng đốt cháy.
Giả sử entanpy và entropy không phụ thuộc vào nhiệt độ.
V.2. Bromothymol xanh là chất chỉ thị được dùng để đánh giá chất lượng nước của các hồ cá. Phổ hấp thụ của bromothymol xanh được thể hiện trên hình:
|
|
Đường 1: Ứng với dạng bazơ. Đường 2: Ứng với dạng axit.
|
Điểm đẳng quang của chất chỉ thị là bước sóng tại đó dạng axit và dạng bazơ của chất chỉ thị có hệ số hấp thụ phân tử (ε) giống nhau. Điểm này giúp xác định nồng độ tổng của chất chỉ thị trong dung dịch.
Dung dịch đo quang được chuẩn bị như sau: Lấy 4 mL dung dịch gốc có nồng độ 1,0093 mM trộn với 6 mL dung dịch HCl 0,1M. Mật độ quang đo được ở bước sóng 500 nm (điểm đẳng quang) và cuvet có bề dày l = 1 cm là 0,166.
1. Tính hệ số hấp thụ phân tử ε500 theo L.mol-1.cm-1
2. Mỗi thí nghiệm trộn 5 mL dung dịch gốc có nồng độ 1,0093 mM với 5 mL dung dịch đệm. Phổ được ghi lại và giá trị mật độ quang được xác định.
Sự hấp thụ cực đại của bromothymol xanh tại các bước sóng với pH = 6,90.
|
λ (nm) |
A |
εaxit (L.mol-1.cm-1) |
εbazơ (L.mol-1.cm-1) |
|
450 |
0,338 |
1129 |
238 |
|
615 |
0,646 |
2,70 |
2603 |
Từ các giá trị đo ở bảng trên, hãy tính nồng độ dạng axit tại bước sóng λ = 450 nm và nồng độ dạng bazơ tại bước sóng λ = 615 nm.
Câu VI.
VI.1. CaF2 tan kém nhất trong các florua của kim loại kiềm và kim loại kiềm thổ.
1. Tính độ tan của CaF2 trong nước theo mg/L?
2. Độ tan của CaF2 thay đổi thế nào trong dung dịch axit? Tính độ tan của CaF2 trong dung dịch có pH = 1 theo mg/L?
Cho biết ở 25oC: Tích số tan Ks(CaF2) = 10-10,40; pKa (HF) = 3,17.
VI.2. Cho hai hỗn hợp A và B. Hỗn hợp A chứa Na2CO3 và NaHCO3. Hỗn hợp B chứa Na2CO3 và NaOH. Hòa tan một trong hai hỗn hợp này vào nước và pha thành 100 ml dung dịch. Chuẩn độ 20,00 mL dung dịch thu được bằng dung dịch HCl 0,200 M với chất chỉ thị phenolphtalein, hết 36,15 mL HCl. Nếu sử dụng chất chỉ thị metyl da cam thì thể tích HCl tiêu thụ là 43,8 ml.
1. Hãy cho biết phản ứng nào xảy ra khi dung dịch chuyển màu và hỗn hợp phân tích là hỗn hợp A hay B? Giải thích.
2. Xác định thành phần phần trăm khối lượng của hỗn hợp đã phân tích.
3. Tính thể tích dung dịch HCl 0,2M cần để chuẩn độ 20 mL dung dịch phân tích ở trên đến pH = 6,5.
Cho biết: Khoảng chuyển màu của phenolphtalein: pH = 8,3 đến 10,0; của metyl da cam: pH = 3,1 đến 4,4.
pKa1(CO2 + H2O)= 6,35; pKa2(CO2 + H2O)= 10,33.
Câu VII. (2,0 điểm)
VII.1. Xiclohexan có thể tồn tại ở một số dạng như: dạng ghế (chair), dạng thuyền (boat), nửa ghế (half-chair), xoắn (twist-boat):
.png)
Trans-4-floxiclohexanol tồn tại chủ yếu ở dạng ghế, trong khi đồng phân cis tồn tại chủ yếu ở dạng xoắn. Hãy giải thích ngắn gọn.
VII.2. So sánh các tính chất của mỗi cặp chất sau và giải thích ngắn gọn:
1. Giá trị pKa1 và pKa2 của axit oxalic (HOOC-COOH) và axit glutaric (HOOC-CH2-CH2-CH2-COOH).
2. Độ tan trong nước của THF (tetrahiđrofuran) và đietyl ete.
.png)
3. Nhiệt độ sôi của chất 1 và 2.
.png)
Câu VIII. (2,0 điểm)
VIII.1. Đề xuất cơ chế cho các phản ứng sau:
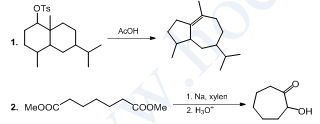
VIII.2. Cacben là tiểu phân có nguyên tử cacbon còn 2 electron chưa tham gia liên kết. Cacben tồn tại ở 2 dạng cấu trúc là singlet (2 electron không liên kết thuộc cùng 1 AO) và triplet (2 electron không liên kết thuộc 2 AO). Cơ chế phản ứng của cacben metylen singlet và triplet với ankan có sự khác nhau. Metylen singlet phản ứng với ankan không có sự chọn lọc giữa các bậc H trong khi đó metylen triplet có sự chọn lọc, ưu tiên bậc III > bậc II > bậc I. Đề xuất cơ chế phản ứng của ankan với cacben metylen singlet và triplet.
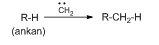
Câu IX. (2,0 điểm)
IX.1. Trong tế bào, hợp chất glutathione đóng vai trò là chất chống oxi hóa. Glutathione phản ứng mạnh với các tác nhân oxi hóa gây hại cho tế bào. Cấu trúc của glutathione như sau:
.png)
1. Hãy cho biết glutathione được cấu tạo từ các đơn vị amino axit nào?
2. Khi tác dụng với các chất oxi hóa, chuyển hóa thành sản phẩm 3 (C20H30N6O12S22-). Đề xuất công thức cấu tạo của 3.
3. Đề xuất cơ chế phản ứng của glutathione với peoxit R-O-O-R.
IX.2.
1. Năm 1911, Wilstatter đã tổng hợp được xicloocta-1,3,5,7-tetraen từ amin vòng theo sơ đồ sau:
.png)
2. Từ axit 2-oxoxiclohexancacboxylic và các hợp chất vô cơ cần thiết, viết sơ đồ tổng hợp lysin.
.png)
Câu X.
X.1. Khi tiến hành metyl hóa D-glucozơ bằng CH3OH (xúc tác HCl khan), lượng sản phẩm metyl α-D-glucopiranozit thu được cao hơn so với sản phẩm metyl β-D-glucopiranozit. Hãy giải thích ngắn gọn. Viết cơ chế phản ứng metyl hóa D-glucozơ bằng CH3OH (xúc tác HCl khan), tạo thành sản phẩm metyl α-D-glucopiranozit.
X.2. Xác định công thức các chất trong sơ đồ tổng hợp sau:
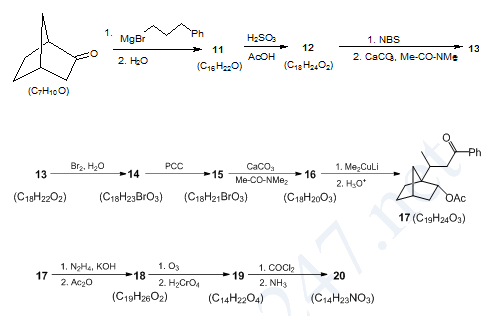
Xác định công thức cấu tạo các chất trong sơ đồ phản ứng.
Cho biết: Tác nhân CaCO3, Me-CO-NMe2 có tác dụng tách hiđro halogenua.
---Để xem tiếp đáp án của Đề thi chọn HSG THPT Chuyên và chọn đội tuyển dự thi HSG Quốc Gia môn Hóa học năm 2019-2020 Sở GD&ĐT Quảng Nam, các em vui lòng đăng nhập vào trang hoc247.net để xem online hoặc tải về máy tính---
Trên đây là một phần trích đoạn nội dung Đề thi chọn HSG THPT Chuyên và chọn đội tuyển dự thi HSG Quốc Gia môn Hóa học năm 2019-2020 Sở GD&ĐT Quảng Nam. Để xem toàn bộ nội dung các em chọn chức năng xem online hoặc đăng nhập vào website hoc247.net để tải tài liệu về máy tính.
Chúc các em học tốt!


.png?enablejsapi=1)
.png)




