HOC247 xin chia sẻ với các em học sinh nội dung Bài tập về hóa trị và số oxi hóa môn Hóa học 10 năm 2021. Với nội dung đầy đủ với các cấp độ khác nhau, hi vọng rằng đây sẽ là tài liệu giúp các em học tập tốt hơn.
A. TÓM TẮT LÝ THUYẾT
I. HÓA TRỊ
1. Hoá trị trong hợp chất ion
- Khái niệm: Trong hợp chất ion, hoá trị của một nguyên tố bằng diện tích của ion và được gọi là điện hoá trị của nguyên tố đó.
Thí dụ:
Trong hợp chất KCl, K có điện hoá trị 1 + và Cl có điện hoá trị 1-.
Trong hợp chất MgF2, Mg có điện hoá trị 2+ và F có điện hoá trị 1-.
- Quy ước: khi viết điện hoá trị của một nguyên tố, ghi giá trị điện tích trước, dấu của điện tích sau.
* Nhận xét:
- Trong hợp chất ion, các nguyên tố kim loại thuộc nhóm IA, IIA, IIIA có điện hoá trị 1+, 2+, 3+.
- Các nguyên tố phi kim thuộc nhóm VIA, VIIA có thể có điện hoá trị 2-, 1-.
2. Hoá trị trong hợp chất cộng hoá trị
- Khái niệm: Trong hợp chất cộng hoá trị, hoá trị của một nguyên tố được xác định bằng số liên kết của nguyên tử nguyên tố đó trong phân tử và được gọi là cộng hoá trị của nguyên tố đó.
Thí dụ:
- Trong công thức cấu tạo của phân tử NH3,
.png?enablejsapi=1)
N có cộng hoá trị 3; H có cộng hoá trị 1.
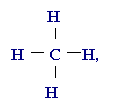
- Trong công thức cấu tạo của phân tử CH4, nguyên tố C có cộng hoá trị 4, nguyên tố H có cộng hoá trị 1.
II. SỐ OXI HOÁ
1. Khái niệm
- Số oxi hoá của một nguyên tố trong phân tử là điện tích của nguyên tử nguyên tố đó trong phân tử. (Giả định rằng: liên kết giữa các nguyên tử trong phân tử là liên kết ion).
2. Quy tắc xác định
Để xác định số oxi hoá người ta đưa ra một số quy tắc sau đây:
- Quy tắc 1: Số oxi hoá của nguyên tố trong các đơn chất bằng không.
Thí dụ: Số oxi hoá của các nguyên tố Cu, Zn, H, N, O trong đơn chất Cu, Zn, H2, N2, O2 ... đều bằng 0.
- Quy tắc 2: Trong một phân tử, tổng số số oxi hoá của các nguyên tố bằng không.
- Quy tắc 3: Số oxi hoá của các ion đơn nguyên tử bằng điện tích của ion đó. Trong ion đa nguyên tử, tổng số oxi hoá của các nguyên tố bằng điện tích của ion.
- Quy tắc 4: Trong hầu hết các hợp chất, số oxi hoá của hiđro bằng +1, trừ một số trường hợp như hiđrua kim loại (NaH, CaH2 ....). Số oxi hoá của oxi bằng -2, trừ trường hợp OF2, peoxit (chẳng hạn H2O2)...
Thí dụ 1: Số oxi hoá của các nguyên tố ở các ion K+, Ca2+, Cl-, S2- lần lượt bằng +1, +2, -1, -2.
Thí dụ 2: Tính số oxi hoá (x) của nitơ trong amoniac NH3, axit nitrơ HNO2, và anion nitrat NO3-.
Trong NH3 : x + 3. (+1) = 0 Þ x = -3.
Trong HNO2 : (+1) + x + 2.(-2) = 0 Þ x = +3.
Trong NO3- : x + 3.(-2) = 1 Þ x = +5.
Cách viết số oxi hoá: Số oxi hoá được viết bằng chữ số thường, dấu đặt phía trước và được đặt ở trên kí hiệu nguyên tố.
B. BÀI TẬP MINH HỌA
Ví dụ 1. Số oxi hóa của nitơ trong NH4+, NO2- , và HNO3 lần lượt là:
A. +5, -3, +3.
B. -3, +3, +5
C. +3, -3, +5
D. +3, +5, -3.
Hướng dẫn giải
Đặt x, y, z lần lượt là số oxi hóa của nguyên tố nitơ trong NH4+, NO2-, và HNO3
Ta có: x + 4.1 = 1 ⇒ x = -3. Số OXH của N trong NH4+ là -3
y + 2.(-2) = -1 ⇒ y = 3. Số OXH của N trong NO2- là +3
z + 1 + 3.(-2) = 0 ⇒ z = 5. Số OXH của N trong HNO3 là +5
⇒ Chọn B.
Ví dụ 2. Xác định số oxi hóa của các nguyên tố trong hợp chất , đơn chất và ion sau:
a) H2S, S, H2SO3, H2SO4.
b) HCl, HClO, NaClO2, HClO3.
c) Mn, MnCl2, MnO2, KMnO4.
Hướng dẫn giải
a) Số oxi hóa của S trong các chất lần lượt là: S-2, S0, S+4, S+6
b) Số oxi hóa của Cl trong các hợp chất: Cl-1, Cl+1,Cl+3, Cl+5, Cl+7.
c) Số oxi hóa của Mn trong các chất: Mn0, Mn+2, Mn+4, Mn+7
Ví dụ 3. Hóa trị và số oxi hóa của N trong phân tử NH4Cl lần lượt là
A. 4 và -3
B. 3 và +5
C. 5 và +5
D. 3 và -3
Hướng dẫn giải
N thuộc nhóm IVA nên có hóa trị 4
Số OXH: x + 4.1 + (-1)=0 ⇒ x = -3.
Ví dụ 4. Xác định số oxi hóa của Mn, Cr, Cl, P trong phân tử: KMnO4, Na2Cr2O7, KClO3, H3PO4
Hướng dẫn giải
Số oxi hóa của Mn, Cr, P: KMn+7O4, Na2Cr+62O7, KCl+5O3, H3P+5O4
Ví dụ 5. Xác định điện hóa trị của các nguyên tố trong các hợp chất sau: KCl, Na2S; Ca3N2.
Hướng dẫn giải
Hóa trị của một nguyên tố trong hợp chất ion gọi là điện hóa trị và bằng điện tích ion đó.
+) KCl: Điện hóa trị của K là: 1+ và của Cl là: 1-
+) Na2S: Điện hóa trị của Na là: 1+ và của S là: 2-
+) Ca3N2: Điện hóa trị của Ca là: 2+ và của N là: 3-
C. LUYỆN TẬP
Câu 1: Trong phân tử NaCl, điện hóa trị của Na và Cl lần lượt là
A. +1 và -1
B. +1 và +1
C. -1 và -1
D. -1 và +1
Câu 2: Trong phân tử H2O2 và O2, cộng hóa trị của O lần lượt là
A. 2 và 0
B. 2 và 2
C. 1 và 0
D. 1 và 2
Câu 3: Nguyên tố R là phi kim thuộc nhóm A. Hợp chất của R với hidro là RH3. Hóa trị với số oxi hóa của R trong oxit tương úng với hóa trị cao nhất lần lượt là
A. 3 và -3
B. 5 và -5
C. 5 và +5
D. 3 và +3
Câu 4: Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4. Công thức hợp chất của R với H và công thức oxit tương ứng với hóa trị cao nhất của R lần lượt là
A. RH2 và RO
B. RH2 và RO2
C. RH4 và RO2
D. RH2 và RO3
Câu 5: Hóa trị với số oxi hóa của N trong phân tử HNO3 lần lượt là
A. 3 và -3
B. 5 và -5
C. 4 và +5
D. 3 và +3
Câu 6: Hóa trị và số oxi hóa của N trong phân tử NH4Cl lần lượt là
A. 4 và -3
B. 3 và +5
C. 5 và +5
D. 3 và -3
Câu 7: Dãy các chất nào dưới đây được sắp xếp theo chiều tăng dần số oxi hóa của nitơ?
A. NO, N2O, NH3, NO3-
B. NH4+, N2, N2O, NO, NO2, NO3-
C. NH3, N2, NO2, NO, NO3-
D. NH3, NO, N2O, NO2, N2O5
Câu 8: Cho một số hợp chất: H2S, H2SO3, H2SO4, NaHS, Na2SO3, SO3, K2S, SO2. Dãy các chất trong đó lưu huỳnh có cùng số oxi hóa là
A. H2S, H2SO3, H2SO4
B. H2SO3, H2SO4, Na2SO3, SO3
C. H2SO3, H2SO4, Na2SO3, SO2
D. H2S, NaHS, K2S
Câu 9: Số oxi hóa của nguyên tố Mn trong hợp chất K2MnO4 là:
A. +7
B. 7+
C. +6
D. 6+
Câu 10: Điện hóa trị của nguyên tố Cl trong hợp chất CaCl2 là:
A. -1
B. +1
C. 1-
D. 1+
Câu 11: Nhận định nào chưa chính xác về số oxi hóa:
A. Đơn chất luôn có số oxi hóa bằng 0
B. Trong hợp chất, tổng số oxi hóa của các nguyên tố bằng 0
C. Trong hợp chất, kim loại luôn có số oxi hóa dương bằng hóa trị của chúng
D. Trong hợp chất, phi kim luôn có số oxi hóa âm và giá trị bằng hóa trị của chúng
Câu 12: Trong phản ứng: 2H2S + O2 → 2S + 2H2O. Số oxi hóa của S trong H2S và S lần lượt là:
A. +2 và 0
B. -2 và 0
C. +4 và -2
D. -2 và +4
Câu 13: Trong hợp chất cộng hóa trị, hóa trị của một nguyên tố:
A. Bằng số liên kết của nguyên tử nguyên tố đó tạo ra được với các nguyên tử khác trong phân tử và được gọi là cộng hóa trị của nguyên tố đó
B. Bằng số liên kết của nguyên tử nguyên tố đó trong phân tử và được gọi là điện hóa trị của nguyên tố đó
C. Bằng số electron liên kết với nguyên tử của nguyên tố khác trong phân tử
D. Bằng số liên kết của nguyên tử nguyên tố đó với nguyên tử gần nhất
Câu 14: Số oxi hóa của Nitơ trong NH4+, NO2- và HNO3 lần lượt là:
A. -3; +3; +5
B. +5; -3; +3
C. +3; -3; +5
D. -3;+5; +3
Câu 15: Trong hợp chất CH4 cộng hóa trị của C là:
A. 4
B. 3
C.2
D. 1
Trên đây là toàn bộ nội dung tài liệu Bài tập về hóa trị và số oxi hóa môn Hóa học 10 năm 2021. Để xem thêm nhiều tài liệu tham khảo hữu ích khác các em chọn chức năng xem online hoặc đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Chúc các em học tốt!