DŲ░ß╗øi ─æ├óy l├Ā HŲ░ß╗øng dß║½n giß║Żi H├│a 10 SGK n├óng cao ChŲ░ŲĪng 4 B├Āi 25 Phß║Żn ß╗®ng oxi h├│a khß╗Ł ─æŲ░ß╗Żc hoc247 bi├¬n soß║Īn v├Ā tß╗Ģng hß╗Żp, nß╗Öi dung b├Īm s├Īt theo chŲ░ŲĪng tr├¼nh SGK H├│a hß╗Źc 10 n├óng cao gi├║p c├Īc em hß╗Źc sinh nß║»m vß╗»ng phŲ░ŲĪng ph├Īp giß║Żi b├Āi tß║Łp v├Ā ├┤n tß║Łp kiß║┐n thß╗®c hiß╗ću quß║Ż hŲĪn.
B├Āi 1 trang 102 SGK H├│a 10 n├óng cao
Mß╗Öt nguy├¬n tß╗Ł lŲ░u huß╗│nh (S) chuyß╗ān th├Ānh ion sunfua (S2-) bß║▒ng c├Īch:
A. nhß║Łn th├¬m mß╗Öt electron.
B. nhŲ░ß╗Øng ─æi mß╗Öt electron,
C. nhß║Łn th├¬m hai electron.
D. nhŲ░ß╗Øng ─æi hai electron.
H├Ży t├¼m ─æ├Īp ├Īn ─æ├║ng.
HŲ░ß╗øng dß║½n giß║Żi:
Chß╗Źn C.
B├Āi 2 trang 103 SGK H├│a 10 n├óng cao
Trong phß║Żn ß╗®ng: Cl2 + 2KBr ŌåÆ Br2 + 2KCl, nguy├¬n tß╗æ clo:
A. chß╗ē bß╗ŗ oxi h├│a.
B. chß╗ē bß╗ŗ khß╗Ł.
C. kh├┤ng bß╗ŗ oxi h├│a, c┼®ng kh├┤ng bß╗ŗ khß╗Ł.
D. vß╗½a bß╗ŗ oxi h├│a, vß╗½a bß╗ŗ khß╗Ł.
H├Ży t├¼m ─æ├Īp ├Īn ─æ├║ng.
HŲ░ß╗øng dß║½n giß║Żi:
Chß╗Źn B.
\(\mathop {C{l_2}}\limits^0 + 2e \to 2\mathop {Cl}\limits^{ - 1} \)
Sß╗▒ khß╗Ł ŌćÆ Cl2 l├Ā chß║źt oxi h├│a (chß║źt bß╗ŗ khß╗Ł).
B├Āi 3 trang 103 SGK H├│a 10 n├óng cao
Trong phß║Żn ß╗®ng: 2Fe(OH)3 ŌåÆ Fe2O3 + 3H2O, nguy├¬n tß╗æ sß║»t:
A. bß╗ŗ oxi h├│a.
B. bß╗ŗ khß╗Ł.
C. kh├┤ng bß╗ŗ oxi h├│a, c┼®ng kh├┤ng bß╗ŗ khß╗Ł.
D. vß╗½a bß╗ŗ oxi h├│a, vß╗½a bß╗ŗ khß╗Ł.
H├Ży t├¼m ─æ├Īp ├Īn ─æ├║ng.
HŲ░ß╗øng dß║½n giß║Żi:
Chß╗Źn C.
V├¼ sß╗æ oxi h├│a cß╗¦a Fe trŲ░ß╗øc v├Ā sau phß║Żn ß╗®ng kh├┤ng ─æß╗Ģi n├¬n bß╗ŗ oxi h├│a, c┼®ng kh├┤ng bß╗ŗ khß╗Ł.
B├Āi 4 trang 103 SGK H├│a 10 n├óng cao
C├Īc c├óu sau ─æ├óy ─æ├║ng hay sai?
a) Sß╗▒ ─æß╗æt ch├Īy natri trong kh├Ł clo l├Ā mß╗Öt phß║Żn ß╗®ng oxi h├│a ŌĆō khß╗Ł.
b) Na2O bao gß╗ōm c├Īc ion Na2+ v├Ā O2ŌłÆ.
c) Khi t├Īc dß╗źng vß╗øi CuO, CO l├Ā chß║źt khß╗Ł.
d) Sß╗▒ oxi h├│a ß╗®ng vß╗øi sß╗▒ giß║Żm sß╗æ oxi h├│a cß╗¦a mß╗Öt nguy├¬n tß╗æ
e) Sß╗▒ khß╗Ł ß╗®ng vß╗øi sß╗▒ t─āng sß╗æ oxi h├│a cß╗¦a mß╗Öt nguy├¬n tß╗æ.
HŲ░ß╗øng dß║½n giß║Żi:
C├óu ─æ├║ng l├Ā a, c.
C├óu sai l├Ā b, d, e.
B├Āi 5 trang 103 SGK H├│a 10 n├óng cao
T├Łnh sß╗æ oxi h├│a cß╗¦a:
a) cacbon trong CH4, CO, C, CO2, CO32-, HCO3- .
b) lŲ░u huß╗│nh trong SO2, H2SO3, S2-, S, SO32-, HSO4-, HS-.
c) clo trong ClO4- , ClO- , Cl2, Cl-, ClO3, Cl2O7.
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
Sß╗æ oxi h├│a cß╗¦a cacbon lß║¦n lŲ░ß╗Żt l├Ā: +4, +2 , 0, +4, +4, +4
Câu b:
Sß╗æ oxi h├│a cß╗¦a lŲ░u huß╗│nh lß║¦n lŲ░ß╗Żt l├Ā: +4, +4, -2, 0,+4, + 6, -2
Câu c:
Sß╗æ oxi h├│a cß╗¦a clo lß║¦n lŲ░ß╗Żt l├Ā: +7, +1, 0, -1, +5, +7
B├Āi 6 trang 103 SGK H├│a 10 n├óng cao
Lß║Łp c├Īc phŲ░ŲĪng tr├¼nh h├│a hß╗Źc cß╗¦a phß║Żn ß╗®ng oxi h├│a - khß╗Ł theo c├Īc sŲĪ ─æß╗ō dŲ░ß╗øi ─æ├óy v├Ā x├Īc ─æß╗ŗnh vai tr├▓ cß╗¦a tß╗½ng chß║źt trong phß║Żn ß╗®ng:
a) Na2SO3 + KMnO4 + H2O ŌåÆ Na2SO4 + MnO2 + KOH
b) FeSO4 + K2Cr2O7 + H2SO4 ŌåÆ Fe2(SO4)3 + K2SO4 + Cr2(SO4)2 + H2O
c) Cu + HNO3 ŌåÆ Cu(NO3)2 + NO2 + H2O
d) Cu + HNO3 ŌåÆ Cu(NO3)2 + NO + H2O
e) Fe3O4 + HNO3 ŌåÆ Fe(NO3)3 + NO + H2O
g) Fe + H2SO4 ŌåÆ Fe2(SO4)3 + SO2 + H2O
h) Cl2 + NaOH ŌåÆ NaCl + NaClO + H2O.
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
.png?enablejsapi=1)
.png)
3Na2SO3 + 2KMnO4 + H2O ŌåÆ 3Na2SO4 + MnO2 + KOH
Vß║Ły Na2SO3 l├Ā chß║źt khß╗Ł; KMnO4 l├Ā chß║źt oxi h├│a v├Ā H2O l├Ā m├┤i trŲ░ß╗Øng.
Câu b:
.png)
.png)
6FeSO4 + K2Cr2O7 + 7H2SO4 ŌåÆ 3Fe2(SO4)3 + K2SO4 + Cr2(SO4)2 + 7H2O
Vß║Ły FeSO4 l├Ā chß║źt khß╗Ł; K2Cr2O7 l├Ā chß║źt oxi h├│a v├Ā H2SO4 l├Ā m├┤i trŲ░ß╗Øng.
Câu c:
.png)
.png)
Cu + 4HNO3 ŌåÆ Cu(NO3)2 + 2NO2 + 2H2O
Vß║Ły chß║źt khß╗Ł l├Ā Cu, chß║źt oxi h├│a v├Ā m├┤i trŲ░ß╗Øng l├Ā HNO3
Câu d:
.png)
.png)
3Cu + 8HNO3 ŌåÆ 3Cu(NO3)2 + 2NO + 2H2O
Vß║Ły chß║źt khß╗Ł l├Ā Cu, chß║źt oxi h├│a v├Ā m├┤i trŲ░ß╗Øng l├Ā HNO3
Câu e:
.png)
.png)
3Fe3O4 + 28HNO3 ŌåÆ 9Fe(NO3)3 + NO + 14H2O
Vß║Ły chß║źt khß╗Ł l├Ā Fe3O4; chß║źt oxi h├│a v├Ā m├┤i trŲ░ß╗Øng l├Ā HNO3
Câu g:
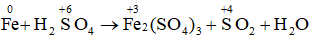
.png)
2Fe + 6H2SO4 ŌåÆ Fe2(SO4)3 + 3SO2 + 6H2O
Vß║Ły chß║źt khß╗Ł l├Ā Fe; chß║źt oxi h├│a v├Ā m├┤i trŲ░ß╗Øng l├Ā H2SO4
Câu h:
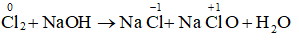
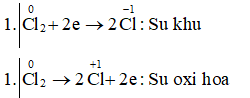
Cl2 + 2NaOH ŌåÆ NaCl + NaClO + H2O.
B├Āi 7 trang 104 SGK H├│a 10 n├óng cao
─Éiiot pentaoxit (I2O5) t├Īc dß╗źng vß╗øi cacbon monoxit tß║Īo ra cacbon ─æioxit v├Ā iot.
a) Lß║Łp phŲ░ŲĪng tr├¼nh h├│a hß╗Źc cß╗¦a phß║Żn ß╗®ng oxi h├│a - khß╗Ł tr├¬n.
b) Khi cho mß╗Öt l├Łt hß╗Śn hß╗Żp c├│ chß╗®a CO v├Ā CO2 tham gia phß║Żn ß╗®ng th├¼ khß╗æi lŲ░ß╗Żng ─æiiot pentaoxit bß╗ŗ khß╗Ł l├Ā 0,5 gam. T├Łnh th├Ānh phß║¦n phß║¦n tr─ām vß╗ü thß╗ā t├Łch cß╗¦a CO trong hß╗Śn hß╗Żp kh├Ł. Biß║┐t rß║▒ng ß╗¤ ─æiß╗üu kiß╗ćn th├Ł nghiß╗ćm, thß╗ā t├Łch mol cß╗¦a chß║źt kh├Ł V = 24 l├Łt.
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
PhŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng
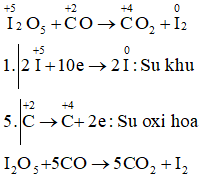
Câu b:
T├Łnh phß║¦n tr─ām vß╗ü thß╗ā t├Łch CO trong hß╗Śn hß╗Żp kh├Ł:
Chß╗ē c├│ CO tham gia phß║Żn ß╗®ng. Theo phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng:
nCO = 5nI2O5 = (5.0,5)/334 = 5/668 mol
VCO = (24. 5)/668 Ōēł 0,18 lit
ŌćÆ %VCO = 0,18.100% Ōēł 18%
Tr├¬n ─æ├óy l├Ā nß╗Öi dung chi tiß║┐t Giß║Żi b├Āi tß║Łp n├óng cao H├│a 10 ChŲ░ŲĪng 4 B├Āi 25, vß╗øi hŲ░ß╗øng dß║½n giß║Żi chi tiß║┐t, r├Ą r├Āng, tr├¼nh b├Āy khoa hß╗Źc. Hoc247 hy vß╗Źng ─æ├óy sß║Į l├Ā t├Āi liß╗ću hß╗»u ├Łch gi├║p c├Īc bß║Īn hß╗Źc sinh lß╗øp 10 hß╗Źc tß║Łp thß║Łt tß╗æt!
T├Āi liß╗ću li├¬n quan
TŲ░ liß╗ću nß╗Ģi bß║Łt tuß║¦n
- Xem thêm








