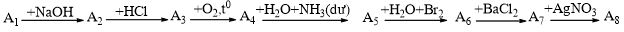Ban bi├¬n tß║Łp HOC247 ─Éß╗ü thi hß╗Źc sinh giß╗Åi cß║źp tß╗ēnh m├┤n H├│a hß╗Źc 9- Sß╗¤ GD & ─ÉT Quß║Żng Trß╗ŗ c├│ ─æ├Īp ├Īn ─æŲ░ß╗Żc tß╗Ģng hß╗Żp b├¬n dŲ░ß╗øi ─æ├óy, t├Āi liß╗ću gß╗ōm c├Īc c├óu hß╗Åi c├│ hŲ░ß╗øng dß║½n giß║Żi chi tiß║┐t. Hi vß╗Źng sß║Į gi├║p c├Īc em ├┤n luyß╗ćn thß║Łt tß╗æt, mß╗Øi c├Īc em c├╣ng theo d├Ąi.
Sß╗× GD & ─ÉT QUß║óNG TRß╗Ŗ
─Éß╗Ć THI Hß╗īC SINH GIß╗ÄI Cß║żP Tß╗łNH
M├öN H├ōA Hß╗īC 9
THỜI GIAN: 150 PHÚT
C├óu 1. (4,0 ─æiß╗ām)
1. Viß║┐t 6 phŲ░ŲĪng tr├¼nh h├│a hß╗Źc c├│ bß║Żn chß║źt kh├Īc nhau tß║Īo th├Ānh kh├Ł oxi.
2. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng theo sŲĪ ─æß╗ō chuyß╗ān h├│a sau:
FeCl3 ŌåÆ Fe2(SO4)3 ŌåÆ Fe(NO3)3 ŌåÆ Fe(NO3)2 ŌåÆ Fe(OH)2 ŌåÆ FeO ŌåÆ Al2O3
3. Cho mol Na t├Īc dß╗źng ho├Ān to├Ān vß╗øi 200 ml dung dß╗ŗch H2SO4 1M. Kß║┐t th├║c phß║Żn ß╗®ng, thu ─æŲ░ß╗Żc dung dß╗ŗch h├▓a tan vß╗½a hß║┐t 0,05 mol Al2O3. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā t├Łnh .
4. Cho gam hß╗Śn hß╗Żp gß╗ōm Cu v├Ā Fe3O4 t├Īc dß╗źng vß╗øi dung dß╗ŗch HCl dŲ░, phß║Żn ß╗®ng ho├Ān to├Ān, c├▓n lß║Īi 8,32 gam chß║źt rß║»n kh├┤ng tan v├Ā dung dß╗ŗch X. C├┤ cß║Īn dung dß╗ŗch X, thu ─æŲ░ß╗Żc 61,92 gam chß║źt rß║»n khan.Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā t├Łnh gi├Ī trß╗ŗ cß╗¦a .
C├óu 2. (5,0 ─æiß╗ām)
1. Cho Al v├Āo dung dß╗ŗch HNO3, thu ─æŲ░ß╗Żc dung dß╗ŗch A1, kh├Ł N2O. Cho dung dß╗ŗch NaOH dŲ░ v├Āo A1, thu ─æŲ░ß╗Żc dung dß╗ŗch B1 v├Ā kh├Ł C1. Cho dung dß╗ŗch H2SO4 ─æß║┐n dŲ░ v├Āo B1. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng xß║Ży ra.
2. Dung dß╗ŗch A chß╗®a hß╗Śn hß╗Żp HCl 1,4M v├Ā H2SO4 0,5M. Cho V l├Łt dung dß╗ŗch chß╗®a hß╗Śn hß╗Żp NaOH 2M v├Ā Ba(OH)2 4M v├Āo 500 ml dung dß╗ŗch A, thu ─æŲ░ß╗Żc kß║┐t tß╗¦a B v├Ā dung dß╗ŗch C. Cho thanh nh├┤m v├Āo dung dß╗ŗch C, phß║Żn ß╗®ng kß║┐t th├║c, thu ─æŲ░ß╗Żc 0,15 mol H2. T├Łnh gi├Ī trß╗ŗ cß╗¦a V.
3. Nung 9,28 gam hß╗Śn hß╗Żp gß╗ōm FeCO3 v├Ā vß╗øi kh├Ł O2 dŲ░ trong b├¼nh k├Łn. Kß║┐t th├║c phß║Żn ß╗®ng, thu ─æŲ░ß╗Żc 0,05 mol Fe2O3 duy nhß║źt v├Ā 0,04 mol CO2. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā x├Īc ─æß╗ŗnh .
4. Cho mol SO3 tan hß║┐t trong 100 gam dung dß╗ŗch H2SO4 91% th├¼ tß║Īo th├Ānh oleum c├│ h├Ām lŲ░ß╗Żng SO3 l├Ā 71%. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā t├Łnh gi├Ī trß╗ŗ cß╗¦a .
C├óu 3. (5,0 ─æiß╗ām)
1. X├Īc ─æß╗ŗnh c├Īc chß║źt A1, A2ŌĆ”A8 v├Ā viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng theo sŲĪ ─æß╗ō chuyß╗ān h├│a sau:
Biß║┐t A1 chß╗®a 3 nguy├¬n tß╗æ trong ─æ├│ c├│ lŲ░u huß╗│nh v├Ā ph├ón tß╗Ł khß╗æi bß║▒ng 51. A8 l├Ā chß║źt kh├┤ng tan.
2. Trong mß╗Öt b├¼nh k├Łn chß╗®a hß╗Śn hß╗Żp gß╗ōm CO, SO2, SO3, CO2 ß╗¤ thß╗ā hŲĪi. Tr├¼nh b├Āy phŲ░ŲĪng ph├Īp h├│a hß╗Źc ─æß╗ā nhß║Łn biß║┐t tß╗½ng chß║źt v├Ā viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng xß║Ży ra.
3. H├▓a tan ho├Ān to├Ān m gam hß╗Śn hß╗Żp R gß╗ōm Fe v├Ā MgCO3 bß║▒ng dung dß╗ŗch HCl, thu ─æŲ░ß╗Żc hß╗Śn hß╗Żp kh├Ł A gß╗ōm H2 v├Ā CO2. Nß║┐u c┼®ng m gam hß╗Śn hß╗Żp tr├¬n t├Īc dß╗źng hß║┐t vß╗øi dung dß╗ŗch H2SO4 ─æß║Ęc, n├│ng, dŲ░; thu ─æŲ░ß╗Żc hß╗Śn hß╗Żp kh├Ł B gß╗ōm SO2 v├Ā CO2. Biß║┐t tß╗ē khß╗æi cß╗¦a B ─æß╗æi vß╗øi A l├Ā 3,6875. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā t├Łnh % khß╗æi lŲ░ß╗Żng mß╗Śi chß║źt trong hß╗Śn hß╗Żp R.
4. Cho gam hß╗Śn hß╗Żp X gß╗ōm Fe v├Ā Fe3O4 t├Īc dß╗źng vß╗øi dung dß╗ŗch H2SO4 ─æß║Ęc n├│ng. Kß║┐t th├║c phß║Żn ß╗®ng, thu ─æŲ░ß╗Żc 0,1 mol SO2 (sß║Żn phß║®m khß╗Ł duy nhß║źt) v├Ā c├▓n 0,14 gam kim loß║Īi kh├┤ng tan. H├▓a tan hß║┐t lŲ░ß╗Żng kim loß║Īi n├Āy trong dung dß╗ŗch HCl (dŲ░ 10% so vß╗øi lŲ░ß╗Żng cß║¦n phß║Żn ß╗®ng), thu ─æŲ░ß╗Żc dung dß╗ŗch Y. Biß║┐t dung dß╗ŗch Y t├Īc dß╗źng vß╗½a hß║┐t vß╗øi dung dß╗ŗch chß╗®a tß╗æi ─æa 0,064 mol KMnO4 ─æun n├│ng, ─æ├Ż axit h├│a bß║▒ng H2SO4 dŲ░. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā t├Łnh sß╗æ mol Fe3O4 trong gam hß╗Śn hß╗Żp X.
C├óu 4. (6,0 ─æiß╗ām)
1. Cho c├Īc chß║źt: KCl, C2H4, CH3COOH, C2H5OH, CH3COOK. H├Ży sß║»p xß║┐p c├Īc chß║źt n├Āy th├Ānh mß╗Öt d├Ży chuyß╗ān h├│a v├Ā viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng xß║Ży ra.
2. ─Éß╗æt ch├Īy ho├Ān to├Ān 0,06 mol hß╗Śn hß╗Żp gß╗ōm metan, etilen, axetilen trong O2, dß║½n to├Ān bß╗Ö sß║Żn phß║®m ch├Īy v├Āo dung dß╗ŗch Ca(OH)2 dŲ░, thu ─æŲ░ß╗Żc 11 gam kß║┐t tß╗¦a v├Ā khß╗æi lŲ░ß╗Żng dung dß╗ŗch trong b├¼nh giß║Żm 4,54 gam. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā t├Łnh sß╗æ mol mß╗Śi kh├Ł trong hß╗Śn hß╗Żp ─æß║¦u.
3. Cho hai hß╗Żp chß║źt hß╗»u cŲĪ X, Y (chß╗®a C, H, O v├Ā chß╗ē chß╗®a mß╗Öt loß║Īi nh├│m chß╗®c ─æ├Ż hß╗Źc) phß║Żn ß╗®ng ─æŲ░ß╗Żc vß╗øi nhau v├Ā ─æß╗üu c├│ khß╗æi lŲ░ß╗Żng mol bß║▒ng 46 gam. X├Īc ─æß╗ŗnh c├┤ng thß╗®c cß║źu tß║Īo cß╗¦a c├Īc chß║źt X, Y. Biß║┐t chß║źt X, Y ─æß╗üu phß║Żn ß╗®ng vß╗øi Na, dung dß╗ŗch cß╗¦a Y l├Ām quß╗│ t├Łm ho├Ī ─æß╗Å. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng xß║Ży ra.
4. ─Éß╗æt ch├Īy vß╗½a hß║┐t 0,4 mol hß╗Śn hß╗Żp N gß╗ōm 1 ancol no X1 v├Ā 1 axit ─æŲĪn chß╗®c Y1, ─æß╗üu mß║Īch hß╗¤ cß║¦n 1,35 mol O2, thu ─æŲ░ß╗Żc 1,2 mol CO2 v├Ā 1,1 mol nŲ░ß╗øc. Nß║┐u ─æß╗æt ch├Īy mß╗Öt lŲ░ß╗Żng x├Īc ─æß╗ŗnh N cho d├╣ sß╗æ mol X1, Y1 thay ─æß╗Ģi th├¼ lu├┤n thu ─æŲ░ß╗Żc mß╗Öt lŲ░ß╗Żng CO2 x├Īc ─æß╗ŗnh. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng v├Ā x├Īc ─æß╗ŗnh c├Īc chß║źt X1, Y1.
5. ─Éun n├│ng 0,1 mol este ─æŲĪn chß╗®c Z, mß║Īch hß╗¤ vß╗øi 30 ml dung dß╗ŗch MOH 20% (D=1,2gam/ml, M l├Ā kim loß║Īi kiß╗üm). Sau khi kß║┐t th├║c phß║Żn ß╗®ng, c├┤ cß║Īn dung dß╗ŗch, thu ─æŲ░ß╗Żc chß║źt rß║»n A v├Ā 3,2 gam ancol B. ─Éß╗æt ch├Īy ho├Ān to├Ān A, thu ─æŲ░ß╗Żc 9,54 gam muß╗æi cacbonat, 8,26 gam hß╗Śn hß╗Żp gß╗ōm CO2 v├Ā hŲĪi nŲ░ß╗øc. Biß║┐t rß║▒ng, khi nung n├│ng A vß╗øi NaOH ─æß║Ęc c├│ CaO, thu ─æŲ░ß╗Żc hi─ærocacbon T. ─Éß╗æt ch├Īy T, thu ─æŲ░ß╗Żc sß╗æ mol H2O lß╗øn hŲĪn sß╗æ mol CO2. Viß║┐t c├Īc phŲ░ŲĪng tr├¼nh phß║Żn ß╗®ng, x├Īc ─æß╗ŗnh kim loß║Īi M v├Ā c├┤ng thß╗®c cß║źu tß║Īo cß╗¦a chß║źt Z.
Cho: H=1; C=12; N=14; O=16; Na=23; Mg=24; S=32; Cl=35,5; K=39; Ca=40; Fe=56; Cu=64.
ĐÁP ÁN
|
Câu |
├Ø |
Nội dung |
─Éiß╗ām |
|---|---|---|---|
|
Câu 1 |
|
|
|
|
|
1 |
2KClO3 \(\xrightarrow{{Mn{O_2},{t^o}}}\) 2KCl+3O2,2H2O \(\xrightarrow{{dpnc}}\) H2+O2,2KNO3 \(\xrightarrow{{{t^o}}}\)2KNO2 + O2 2O3 \(\xrightarrow{{{t^o}}}\) 3O2, 2H2O2 \(\xrightarrow{{Mn{O_2},{t^o}}}\)2H2O +O2, 2Al2O3 \(\xrightarrow{{dpnc,c{\text{r}}i{\text{o}}lit}}\)4Al+3O2 |
1,0 |
|
|
2 |
2FeCl3 + 3Ag2 SO4 ŌåÆ Fe2(SO4)3 + 6AgCl Fe2(SO4)3 + Ba(NO3)2 ŌåÆ BaSO4 + Fe(NO3)3 2Fe(NO3)3 + Fe ŌåÆ 3Fe(NO3)2 Fe(NO3)2 + 2NaOH ŌåÆ 2NaNO3 + Fe(OH)2 Fe(OH)2 ŌåÆH2O + FeO 3FeO + 2Al ŌåÆ 3Fe + Al2O3 |
1,0 |
|
|
3 |
2Na + H2SO4 ŌåÆ Na2SO4 + H2 (1) C├│ thß╗ā: 2Na + 2H2O ŌåÆ 2NaOH + H2 (2) Nß║┐u axit dŲ░: 3H2SO4 + Al2O3 ŌåÆ Al2(SO4)3 + 3H2O (3) Nß║┐u Na dŲ░: 2NaOH + Al2O3 ŌåÆ 2NaAlO2 + H2O (4) TH1: Axit dŲ░, kh├┤ng c├│ (2,4) nNa=2(0,2-0,15)=0,1 mol TH2: Na dŲ░, kh├┤ng c├│ (3) nNa=2.0,2+0,1=0,5 mol |
1,0 |
|
|
4 |
Do Cu dŲ░ Dung dß╗ŗch chß╗ē c├│ HCl, FeCl2 v├Ā CuCl2 Fe3O4 + 8HCl ŌåÆ FeCl2 + 2FeCl3 + 4H2O Cu + 2FeCl3 ŌåÆ CuCl2 + 2FeCl2 Gß╗Źi sß╗æ mol Fe3O4 (1) = a mol 127.3a + 135.a = 61,92 a = 0,12 mol m = 8,32 + 232. 0,12 + 64. 0,12 = 43,84 gam |
1,0 |
|
Câu 2 |
|
|
|
|
|
1 |
8Al + 30 HNO3 ŌåÆ 8Al(NO3)3 + 3N2O + 15H2O (1) 8Al + 30 HNO3 ŌåÆ 8Al(NO3)3 + 4NH4NO3 + 15H2O (2) ├× dung dß╗ŗch A1: Al(NO3)3 , NH4NO3, HNO3 dŲ░ NaOH + HNO3 ŌåÆ NaNO3 + H2O (3) NaOH + NH4NO3 ŌåÆ NaNO3 + NH3 + H2O (4) ├× Kh├Ł C1: NH3 4NaOH + Al(NO3)3 ŌåÆ NaAlO2 + 3NaNO3 + 2H2O (5) ├× Dung dß╗ŗch B1: NaNO3, NaAlO2, NaOH dŲ░ 2NaOH + H2SO4 ŌåÆ Na2SO4 + 2H2O (6) 2NaAlO2 + H2SO4 + 2H2O ŌåÆ Na2SO4 + 2Al(OH)3 (7) 2NaAlO2 + 4H2SO4ŌåÆ Na2SO4 + Al2(SO4)3 + 4H2O (8) |
2,0 |
Tr├¬n ─æ├óy l├Ā tr├Łch dß║½n mß╗Öt phß║¦n nß╗Öi dung t├Āi liß╗ću ─Éß╗ü thi hß╗Źc sinh giß╗Åi cß║źp tß╗ēnh m├┤n H├│a hß╗Źc 9- Sß╗¤ GD & ─ÉT Quß║Żng Trß╗ŗ c├│ ─æ├Īp ├Īn. ─Éß╗ā xem th├¬m nhiß╗üu t├Āi liß╗ću tham khß║Żo hß╗»u ├Łch kh├Īc c├Īc em chß╗Źn chß╗®c n─āng xem online hoß║Ęc ─æ─āng nhß║Łp v├Āo trang hoc247.net ─æß╗ā tß║Żi t├Āi liß╗ću vß╗ü m├Īy t├Łnh.
Ngo├Āi ra c├Īc em hß╗Źc sinh c├│ thß╗ā tham khß║Żo c├Īc t├Āi liß╗ću c├╣ng chuy├¬n mß╗źc:
- ─Éß╗ü thi hß╗Źc sinh giß╗Åi cß║źp huyß╗ćn m├┤n H├│a hß╗Źc 9- Ph├▓ng GD & ─ÉT Tam DŲ░ŲĪng c├│ ─æ├Īp ├Īn
- ─Éß╗ü thi hß╗Źc sinh giß╗Åi cß║źp huyß╗ćn m├┤n H├│a hß╗Źc 8- Ph├▓ng GD & ─ÉT Thß╗Ź Xu├ón c├│ ─æ├Īp ├Īn
Ch├║c c├Īc em hß╗Źc tß╗æt!