Vß╗øi mong muß╗æn gi├║p c├Īc em c├│ th├¬m nhiß╗üu nguß╗ōn t├Āi liß╗ću ─æß╗ā ├┤n tß║Łp thß║Łt tß╗æt cho kß╗│ thi hß╗Źc k├¼ sß║»p tß╗øi ban bi├¬n tß║Łp HOC247 xin giß╗øi thiß╗ću ─Éß╗ü cŲ░ŲĪng ├┤n tß║Łp HK1 m├┤n H├│a hß╗Źc 10 C├Īnh Diß╗üu n─ām 2022-2023. Nß╗Öi dung t├Āi liß╗ću bao gß╗ōm c├Īc kiß║┐n thß╗®c trß╗Źng t├óm v├Ā b├Āi tß║Łp c├│ ─æ├Īp ├Īn chi tiß║┐t. Mß╗Øi c├Īc em tham khß║Żo!
1. T├ōM Tß║«T L├Ø THUYß║ŠT
1.1. Cß║żU Tß║ĀO NGUY├ŖN Tß╗¼
A. Th├Ānh phß║¦n cß╗¦a nguy├¬n tß╗Ł
Cß║źu tr├║c cß╗¦a nguy├¬n tß╗Ł
Nguy├¬n tß╗Ł bao gß╗ōm:
- Lß╗øp vß╗Å: ─æŲ░ß╗Żc tß║Īo n├¬n bß╗¤i c├Īc hß║Īt electron, k├Ł hiß╗ću l├Ā e
- Hß║Īt nh├ón: ─æŲ░ß╗Żc tß║Īo n├¬n bß╗¤i c├Īc hß║Īt proton v├Ā hß║Īt neutron
+ Hß║Īt proton, k├Ł hiß╗ću l├Ā p
+ Hß║Īt neutron, k├Ł hiß╗ću l├Ā n
Khß╗æi lŲ░ß╗Żng v├Ā ─æiß╗ćn t├Łch c├Īc hß║Īt cŲĪ bß║Żn
|
Loß║Īi hß║Īt |
Electron |
Proton |
Neutron |
|
Khß╗æi lŲ░ß╗Żng (amu) |
0,00055 |
1 |
1 |
|
─Éiß╗ćn t├Łch (e0) |
-1 |
+1 |
0 |
- Trong mß╗Öt nguy├¬n tß╗Ł: sß╗æ proton = sß╗æ electron
- Trong tß║źt cß║Ż c├Īc nguy├¬n tß╗æ, chß╗ē c├│ duy nhß║źt mß╗Öt loß║Īi nguy├¬n tß╗Ł cß╗¦a hydrogen (H) ─æŲ░ß╗Żc tß║Īo n├¬n bß╗¤i proton v├Ā electron (kh├┤ng c├│ neutron).
Khß╗æi lŲ░ß╗Żng v├Ā k├Łch thŲ░ß╗øc cß╗¦a nguy├¬n tß╗Ł
- Khß╗æi lŲ░ß╗Żng nguy├¬n tß╗Ł tß║Łp trung chß╗¦ yß║┐u ß╗¤ hß║Īt nh├ón nguy├¬n tß╗Ł.
- K├Łch thŲ░ß╗øc cß╗¦a nguy├¬n tß╗Ł l├Ā v├┤ c├╣ng nhß╗Å
- Hß║Īt nh├ón nguy├¬n tß╗Ł c├│ k├Łch thŲ░ß╗øc rß║źt nhß╗Å so vß╗øi nguy├¬n tß╗Ł (phß║¦n kh├┤ng gian rß╗Śng chiß║┐m chß╗¦ yß║┐u trong nguy├¬n tß╗Ł).
B. NGUY├ŖN Tß╗É H├ōA Hß╗īC
Nguy├¬n tß╗æ h├│a hß╗Źc
Nguy├¬n tß╗æ h├│a hß╗Źc l├Ā tß║Łp hß╗Żp c├Īc nguy├¬n tß╗Ł c├│ c├╣ng sß╗æ hß║Īt proton.
Sß╗æ hiß╗ću nguy├¬n tß╗Ł, sß╗æ khß╗æi
Sß╗æ hiß╗ću nguy├¬n tß╗Ł: Z.
Số khối (A) = số proton (P) + số neutron (N)
K├Ł hiß╗ću nguy├¬n tß╗Ł
\(_Z^AX\)
K├Ł hiß╗ću nguy├¬n tß╗Ł \(_Z^AX\) cho biß║┐t k├Ł hiß╗ću ho├Ī hß╗Źc cß╗¦a nguy├¬n tß╗æ (X), sß╗æ hiß╗ću nguy├¬n tß╗Ł (Z) v├Ā sß╗æ khß╗æi (A).
─Éß╗ōng vß╗ŗ
C├Īc ─æß╗ōng vß╗ŗ cß╗¦a mß╗Öt nguy├¬n tß╗æ ho├Ī hß╗Źc l├Ā nhß╗»ng nguy├¬n tß╗Ł c├│ c├╣ng sß╗æ proton (P), c├╣ng sß╗æ hiß╗ću nguy├¬n tß╗Ł (Z), nhŲ░ng kh├Īc nhau vß╗ü sß╗æ neutron (N).
Nguy├¬n tß╗Ł khß╗æi v├Ā nguy├¬n tß╗Ł khß╗æi trung b├¼nh
- Nguy├¬n tß╗Ł khß╗æi cß╗¦a mß╗Öt nguy├¬n tß╗Ł cho biß║┐t khß╗æi lŲ░ß╗Żng cß╗¦a nguy├¬n tß╗Ł ─æ├│ nß║Ęng gß║źp bao nhi├¬u lß║¦n ─æŲĪn vß╗ŗ khß╗æi lŲ░ß╗Żng nguy├¬n tß╗Ł (1 amu).
- C├┤ng thß╗®c t├Łnh nguy├¬n tß╗Ł khß╗æi trung b├¼nh cß╗¦a nguy├¬n tß╗æ X:
\(\overline {{{\rm{A}}_{\rm{x}}}} = \frac{{{a_1}.{A_1} + {a_2}.{A_2} + ... + {a_i}.{A_i}}}{{100}}\)
\(\overline {{{\rm{A}}_{\rm{x}}}} \): l├Ā nguy├¬n tß╗Ł khß╗æi trung b├¼nh cß╗¦a X.
Ai l├Ā nguy├¬n tß╗Ł khß╗æi ─æß╗ōng vß╗ŗ thß╗® i.
ai l├Ā tß╗ē lß╗ć % sß╗æ nguy├¬n tß╗Ł ─æß╗ōng vß╗ŗ thß╗® i.
C. M├ö H├īNH NGUY├ŖN Tß╗¼ V├Ć ORBITAL NGUY├ŖN Tß╗¼
M├┤ h├¼nh nguy├¬n tß╗Ł
- Theo chiß╗üu tß╗½ hß║Īt nh├ón ra ngo├Āi lß╗øp vß╗Å, c├Īc electron ─æŲ░ß╗Żc sß║»p xß║┐p v├Āo c├Īc lß╗øp electron. K├Ł hiß╗ću cß╗¦a mß╗Śi lß╗øp nhŲ░ sau:
+ Lß╗øp thß╗® nhß║źt gß╗Źi l├Ā lß╗øp K.
+ Lß╗øp thß╗® hai gß╗Źi l├Ā lß╗øp L.
+ Lß╗øp thß╗® ba gß╗Źi l├Ā lß╗øp M.
+ Lß╗øp thß╗® tŲ░ gß╗Źi l├Ā lß╗øp N.
LŲ░u ├Į:
- C├Īc electron ─æŲ░ß╗Żc ph├ón bß╗æ lß║¦n lŲ░ß╗Żt v├Āo lß╗øp gß║¦n hß║Īt nh├ón trŲ░ß╗øc.
- Sß╗æ electron tß╗æi ─æa trong mß╗Śi lß╗øp l├Ā 2n2 (n l├Ā sß╗æ thß╗® tß╗▒ lß╗øp electron).
Orbital nguy├¬n tß╗Ł
- Orbital nguy├¬n tß╗Ł (AO) l├Ā khu vß╗▒c kh├┤ng gian xung quanh hß║Īt nh├ón nguy├¬n tß╗Ł m├Ā x├Īc suß║źt t├¼m thß║źy electron trong khu vß╗▒c ─æ├│ l├Ā lß╗øn nhß║źt (khoß║Żng 90%).
- Orbial nguy├¬n tß╗Ł c├│ mß╗Öt sß╗æ h├¼nh dß║Īng kh├Īc nhau.
+ AO h├¼nh cß║¦u, c├▓n gß╗Źi l├Ā AO s;
+ AO h├¼nh sß╗æ t├Īm nß╗Ģi, c├▓n gß╗Źi l├Ā AO p (t├╣y theo vß╗ŗ tr├Ł cß╗¦a AO p tr├¬n hß╗ć trß╗źc tß╗Źa ─æß╗Ö ─Éß╗ü - c├Īc, sß║Į gß╗Źi l├Ā AO px, py v├Ā pz).
H├¼nh dß║Īng cß╗¦a AO s(a) v├Ā AO p (b, c, d)
- Mß╗Öt AO chß╗ē chß╗®a tß╗æi ─æa 2 electron
LŲ░u ├Į:
- C├Īc AO p trong c├╣ng mß╗Öt lß╗øp electron c├│ h├¼nh dß║Īng v├Ā k├Łch thŲ░ß╗øc tŲ░ŲĪng tß╗▒ nhau nhŲ░ng kh├Īc nhau vß╗ü ─æß╗ŗnh hŲ░ß╗øng trong kh├┤ng gian.
- Ngo├Āi c├Īc AO hay gß║Ęp l├Ā s v├Ā p, c├▓n c├│ c├Īc AO kh├Īc nhŲ░ d, f c├│ h├¼nh dß║Īng phß╗®c tß║Īp hŲĪn.
D. Lß╗ÜP, PH├éN Lß╗ÜP V├Ć Cß║żU H├īNH ELECTRON
Lß╗øp v├Ā ph├ón lß╗øp electron
Lß╗øp
- Trong nguy├¬n tß╗Ł, c├Īc electron ─æŲ░ß╗Żc sß║»p xß║┐p th├Ānh tß╗½ng lß╗øp (k├Ł hiß╗ću K, L, M, N, O, P,Q) tß╗½ gß║¦n ─æß║┐n xa hß║Īt nh├ón, theo thß╗® tß╗▒ tß╗½ lß╗øp n = 1 ─æß║┐n n = 7
- C├Īc electron tr├¬n c├╣ng mß╗Öt lß╗øp c├│ n─āng lŲ░ß╗Żng gß║¦n bß║▒ng nhau.
Sß╗æ lŲ░ß╗Żng AO v├Ā sß╗æ electron tß╗æi ─æa trong mß╗Śi lß╗øp
|
Lß╗øp |
K (n = 1) |
L (n = 2) |
M (n = 3) |
N (n = 4) |
|
Sß╗æ lŲ░ß╗Żng AO |
1 |
4 |
9 |
16 |
|
Số electron tối đa |
2 |
8 |
18 |
32 |
Lß╗øp thß╗® n c├│ tß╗æi ─æa 2n2 electron.
Ph├ón lß╗øp electron
- Mß╗Śi lß╗øp electron (trß╗½ lß╗øp thß╗® nhß║źt) lß║Īi ─æŲ░ß╗Żc chia th├Ānh c├Īc ph├ón lß╗øp theo nguy├¬n tß║»c: C├Īc electron thuß╗Öc c├╣ng mß╗Öt ph├ón lß╗øp c├│ n─āng lŲ░ß╗Żng bß║▒ng nhau.
- Sß╗æ lŲ░ß╗Żng v├Ā k├Ł hiß╗ću c├Īc ph├ón lß╗øp trong mß╗Öt lß╗øp: Lß╗øp electron thß╗® n c├│ n ph├ón lß╗øp v├Ā ─æŲ░ß╗Żc k├Ł hiß╗ću lß║¦n lŲ░ß╗Żt l├Ā ns, np, nd, nf, ...
+ Lß╗øp K (n =1): c├│ 1 ph├ón lß╗øp, ─æŲ░ß╗Żc k├Ł hiß╗ću l├Ā 1s.
+ Lß╗øp L (n =2): c├│ 2 ph├ón lß╗øp, ─æŲ░ß╗Żc k├Ł hiß╗ću l├Ā 2s v├Ā 2p.
+ Lß╗øp M (n =3): c├│ 3 ph├ón lß╗øp, ─æŲ░ß╗Żc k├Ł hiß╗ću l├Ā 3s, 3p v├Ā 3d.
- Sß╗æ lŲ░ß╗Żng AO trong mß╗Śi ph├ón lß╗øp
+ Ph├ón lß╗øp ns chß╗ē c├│ 1 AO.
+ Ph├ón lß╗øp np c├│ 3 AO.
+ Ph├ón lß╗øp nd c├│ 5 AO.
+ Ph├ón lß╗øp nf c├│ 7 AO.
- Sß╗æ electron trong mß╗Śi ph├ón lß╗øp ─æŲ░ß╗Żc biß╗āu diß╗ģn bß║▒ng chß╗ē sß╗æ ph├Ła tr├¬n, b├¬n phß║Żi k├Ł hiß╗ću ph├ón lß╗øp. Ph├ón lß╗øp n├Āo ─æ├Ż c├│ tß╗æi ─æa electron ─æŲ░ß╗Żc gß╗Źi l├Ā ph├ón lß╗øp b├Żo h├▓a.
LŲ░u ├Į: Sß╗æ lŲ░ß╗Żng electron tß╗æi ─æa trong mß╗Śi ph├ón lß╗øp
- Ph├ón lß╗øp ns chß╗®a tß╗æi ─æa 2 electron.
- Ph├ón lß╗øp np chß╗®a tß╗æi ─æa 6 electron.
- Ph├ón lß╗øp nd chß╗®a tß╗æi ─æa 10 electron.
- Ph├ón lß╗øp nf chß╗®a tß╗æi ─æa 14 electron.
Cß║źu h├¼nh electron nguy├¬n tß╗Ł
C├Īch viß║┐t cß║źu h├¼nh electron nguy├¬n tß╗Ł
- Cß║źu h├¼nh electron biß╗āu diß╗ģn sß╗▒ ph├ón bß╗æ electron v├Āo lß╗øp vß╗Å nguy├¬n tß╗Ł theo c├Īc lß╗øp v├Ā ph├ón lß╗øp.
- C├Īc bŲ░ß╗øc viß║┐t cß║źu h├¼nh electron nguy├¬n tß╗Ł theo nhß╗»ng nguy├¬n tß║»c sau:
+ Quy tß║»c 1: ─Éiß╗ün electron theo thß╗® tß╗▒ c├Īc mß╗®c n─āng lŲ░ß╗Żng tß╗½ thß║źp ─æß║┐n cao (d├Ży Klechkovski):
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s...
─Éiß╗ün electron b├Żo h├▓a ph├ón lß╗øp trŲ░ß╗øc rß╗ōi mß╗øi ─æiß╗ün tiß║┐p v├Āo ph├ón lß╗øp sau.
- Quy tß║»c 2: ─Éß╗Ģi lß║Īi vß╗ŗ tr├Ł c├Īc ph├ón lß╗øp sao cho sß╗æ thß╗® tß╗▒ lß╗øp (n) t─āng dß║¦n tß╗½ tr├Īi qua phß║Żi, c├Īc ph├ón lß╗øp trong c├╣ng mß╗Öt lß╗øp theo thß╗® tß╗▒ s, p, d, f.
- Cß║źu h├¼nh electron cho biß║┐t thß╗® tß╗▒ mß╗®c n─āng lŲ░ß╗Żng c├Īc electron giß╗»a c├Īc ph├ón lß╗øp. N─āng lŲ░ß╗Żng cß╗¦a electron trong mß╗Śi ph├ón lß╗øp t─āng theo chiß╗üu tß╗½ tr├Īi qua phß║Żi.
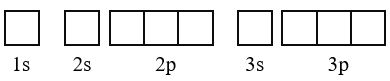
Biß╗āu diß╗ģn cß║źu h├¼nh electron theo ├┤ orbital
- Quy tß║»c 1: Viß║┐t cß║źu h├¼nh electron cß╗¦a nguy├¬n tß╗Ł
- Quy tß║»c 2: Biß╗āu diß╗ģn mß╗Śi AO bß║▒ng mß╗Öt ├┤ vu├┤ng (orbital hay ├┤ lŲ░ß╗Żng tß╗Ł), c├Īc AO trong c├╣ng ph├ón lß╗øp th├¼ viß║┐t liß╗ün nhau, c├Īc AO kh├Īc ph├ón lß╗øp th├¼ viß║┐t t├Īch nhau. Thß╗® tß╗▒ c├Īc ├┤ orbital tß╗½ tr├Īi sang phß║Żi theo thß╗® tß╗▒ nhŲ░ ß╗¤ cß║źu h├¼nh electron.
- Quy tß║»c 3: ─Éiß╗ün electron v├Āo tß╗½ng ├┤ orbital theo thß╗® tß╗▒ lß╗øp v├Ā ph├ón lß╗øp, mß╗Śi electron biß╗āu diß╗ģn bß║▒ng mß╗Öt m┼®i t├¬n.
LŲ░u ├Į:
- Trong mß╗Śi ph├ón lß╗øp, electron ─æŲ░ß╗Żc ph├ón bß╗æ sao cho sß╗æ electron ─æß╗Öc th├ón l├Ā lß╗øn nhß║źt, electron ─æŲ░ß╗Żc ─æiß╗ün v├Āo c├Īc orbital theo thß╗® tß╗▒ tß╗½ tr├Īi sang phß║Żi.
- Trong mß╗Öt ├┤ orbital, electron ─æß║¦u ti├¬n ─æŲ░ß╗Żc biß╗āu diß╗ģn bß║▒ng m┼®i t├¬n quay l├¬n, electron thß╗® hai ─æŲ░ß╗Żc biß╗āu diß╗ģn bß║▒ng m┼®i t├¬n quay xuß╗æng.
Dß╗▒ ─æo├Īn t├Łnh chß║źt h├│a hß╗Źc cŲĪ bß║Żn cß╗¦a nguy├¬n tß╗æ dß╗▒a theo cß║źu h├¼nh electron cß╗¦a nguy├¬n tß╗Ł
Dß╗▒a v├Āo ─æß║Ęc ─æiß╗ām vß╗ü cß║źu h├¼nh electron lß╗øp ngo├Āi c├╣ng ─æß╗ā dß╗▒ ─æo├Īn t├Łnh chß║źt h├│a hß╗Źc cŲĪ bß║Żn cß╗¦a nguy├¬n tß╗æ:
|
─Éß║Ęc ─æiß╗ām cß╗¦a lß╗øp electron ngo├Āi c├╣ng |
||||
|
Số electron |
1, 2, 3 |
4 |
5, 6, 7 |
8 |
|
Loß║Īi nguy├¬n tß╗æ |
Kim loß║Īi |
Kim loß║Īi hoß║Ęc phi kim |
Phi kim |
Kh├Ł hiß║┐m (trß╗½ He) |
1.2. Bß║óNG TUß║”N HO├ĆN C├üC NGUY├ŖN Tß╗É H├ōA Hß╗īC
A. Cß║żU Tß║ĀO Bß║óNG TUß║”N HO├ĆN C├üC NGUY├ŖN Tß╗É H├ōA Hß╗īC
Nguy├¬n tß║»c sß║»p xß║┐p c├Īc nguy├¬n tß╗æ trong bß║Żng tuß║¦n ho├Ān
- C├Īc nguy├¬n tß╗æ ─æŲ░ß╗Żc xß║┐p theo chiß╗üu t─āng dß║¦n cß╗¦a ─æiß╗ćn t├Łch hß║Īt nh├ón nguy├¬n tß╗Ł.
- C├Īc nguy├¬n tß╗æ c├│ c├╣ng sß╗æ lß╗øp electron trong nguy├¬n tß╗Ł ─æŲ░ß╗Żc xß║┐p c├╣ng mß╗Öt chu k├¼.
- C├Īc nguy├¬n tß╗æ c├│ c├╣ng sß╗æ electron ho├Ī trß╗ŗ trong nguy├¬n tß╗Ł ─æŲ░ß╗Żc xß║┐p c├╣ng mß╗Öt nh├│m, trß╗½ nh├│m VIIIB.
LŲ░u ├Į: Electron h├│a trß╗ŗ l├Ā nhß╗»ng electron c├│ khß║Ż n─āng tham gia h├¼nh th├Ānh li├¬n kß║┐t h├│a hß╗Źc (thŲ░ß╗Øng l├Ā nhß╗»ng electron ß╗¤ lß╗øp ngo├Āi c├╣ng).
Cß║źu tß║Īo cß╗¦a bß║Żng tuß║¦n ho├Ān
- ├ö nguy├¬n tß╗æ: Sß╗æ thß╗® tß╗▒ cß╗¦a mß╗Öt ├┤ nguy├¬n tß╗æ bß║▒ng sß╗æ hiß╗ću nguy├¬n tß╗Ł cß╗¦a nguy├¬n tß╗æ ho├Ī hß╗Źc trong ├┤ ─æ├│.
- Chu k├¼ l├Ā tß║Łp hß╗Żp c├Īc nguy├¬n tß╗æ h├│a hß╗Źc m├Ā nguy├¬n tß╗Ł cß╗¦a ch├║ng c├│ c├╣ng sß╗æ lß╗øp electron
+ C├Īc chu k├¼ 1, 2 v├Ā 3 l├Ā c├Īc chu k├¼ nhß╗Å.
+ C├Īc chu k├¼ 4, 5, 6 v├Ā 7 l├Ā c├Īc chu k├¼ lß╗øn.
- Nh├│m l├Ā tß║Łp hß╗Żp c├Īc nguy├¬n tß╗æ h├│a hß╗Źc m├Ā nguy├¬n tß╗Ł c├│ cß║źu h├¼nh electron tŲ░ŲĪng tß╗▒ nhau
Sß╗æ thß╗® tß╗▒ cß╗¦a nh├│m A bß║▒ng sß╗æ electron ß╗¤ lß╗øp ngo├Āi c├╣ng cß╗¦a nguy├¬n tß╗Ł c├Īc nguy├¬n tß╗æ trong nh├│m.
Ph├ón loß║Īi nguy├¬n tß╗æ dß╗▒a theo cß║źu h├¼nh electron v├Ā t├Łnh chß║źt ho├Ī hß╗Źc
- Dß╗▒a v├Āo cß║źu h├¼nh electron: nguy├¬n tß╗æ s, nguy├¬n tß╗æ p, nguy├¬n tß╗æ d v├Ā nguy├¬n tß╗æ f.
- Dß╗▒a v├Āo t├Łnh chß║źt ho├Ī hß╗Źc: nguy├¬n tß╗æ kim loß║Īi, nguy├¬n tß╗æ phi kim v├Ā nguy├¬n tß╗æ kh├Ł hiß║┐m.
B. XU HŲ»ß╗ÜNG BIß║ŠN ─Éß╗öI TRONG Bß║óNG TUß║”N HO├ĆN
B├Īn k├Łnh nguy├¬n tß╗Ł
- B├Īn k├Łnh nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ nh├│m A c├│ xu huong bi├¬n ─æß╗æi tuß║¦n ho├Ān theo chiß╗üu t─āng cß╗¦a ─æiß╗ćn t├Łch hß║Īt nh├ón:
+ Trong mß╗Öt chu k├¼, tß╗½ tr├Īi sang phß║Żi, b├Īn k├Łnh nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ c├│ xu hŲ░ß╗øng giß║Żm dß║¦n
+ Trong mß╗Öt nh├│m, theo chiß╗üu tß╗½ tr├¬n xuß╗æng dŲ░ß╗øi b├Īn k├Łnh nguy├¬n tß╗Ł c├│ xu hŲ░ß╗øng t─āng.
─Éß╗Ö ├óm ─æiß╗ćn
- ─Éß╗Ö ├óm ─æiß╗ćn cß╗¦a mß╗Öt nguy├¬n tß╗Ł ─æß║Ęc trŲ░ng cho khß║Ż n─āng h├║t electron cß╗¦a nguy├¬n tß╗Ł ─æ├│ khi tß║Īo th├Ānh li├¬n kß║┐t ho├Ī hß╗Źc.
- ─Éß╗Ö ├óm ─æiß╗ćn cß╗¦a nguy├¬n tß╗Ł c├Īc nguy├¬n tß╗æ nh├│m A c├│ xu hŲ░ß╗øng biß║┐n ─æß╗æi tuß║¦n ho├Ān theo chiß╗üu t─āng cß╗¦a ─æiß╗ćn t├Łch hß║Īt nh├ón:
+ Trong mß╗Öt chu k├¼, ─æß╗Ö ├óm diß╗ćn cß╗¦a nguy├¬n tß╗½ c├Īc nguy├¬n tß╗æ c├│ xu hŲ░ß╗øng t─āng dß║¦n.
+ Trong mß╗Öt nh├│m, ─æß╗Ö ├óm ─æiß╗ćn cß╗¦a nguy├¬n tß╗Ł c├Īc nguy├¬n tß╗æ c├│ xu hŲ░ß╗øng giß║Żm dß║¦n.
T├Łnh kim loß║Īi, t├Łnh phi kim
- T├Łnh kim loß║Īi l├Ā t├Łnh chß║źt cß╗¦a mß╗Öt nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł dß╗ģ nhŲ░ß╗Øng electron.
- T├Łnh phi kim l├Ā t├Łnh chß║źt cß╗¦a mß╗Öt nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł dß╗ģ nhß║Łn electron.
- T├Łnh kim loß║Īi, t├Łnh phi kim cß╗¦a c├Īc nguy├¬n tß╗æ nh├│m A c├│ xu hŲ░ß╗øng biß║┐n ─æß╗Ģi tuß║¦n ho├Ān theo chiß╗üu t─āng cß╗¦a ─æiß╗ćn t├Łch hß║Īt nh├ón:
+ Trong mß╗Öt chu k├¼, t├Łnh kim loß║Īi cß╗¦a c├Īc nguy├¬n tß╗æ giß║Żm dß║¦n, t├Łnh phi kim t─āng dß║¦n.
+ Trong mß╗Öt nh├│m, t├Łnh kim loß║Īi cß╗¦a c├Īc nguy├¬n tß╗æ t─āng dß║¦n, t├Łnh phi kim giß║Żm dß║¦n.
LŲ░u ├Į: T├Łnh kim loß║Īi v├Ā t├Łnh phi kim lu├┤n biß║┐n ─æß╗Ģi ngŲ░ß╗Żc chiß╗üu nhau. ─Éß╗Ö ├óm ─æiß╗ćn v├Ā t├Łnh phi kim cß╗¦a c├Īc nguy├¬n tß╗Ł cß╗¦a nguy├¬n tß╗æ h├│a hß╗Źc biß║┐n ─æß╗Ģi c├╣ng chiß╗üu trong mß╗Öt chu k├¼ v├Ā trong mß╗Öt nh├│m.
T├Łnh acid - base cß╗¦a oxide v├Ā hydroxide
Xu hŲ░ß╗øng biß║┐n ─æß╗Ģi t├Łnh acid, t├Łnh base cß╗¦a oxide v├Ā hydroxide trong mß╗Öt chu k├¼: t├Łnh acid c├│ xu hŲ░ß╗øng t─āng dß║¦n, t├Łnh base c├│ xu hŲ░ß╗øng giß║Żm dß║¦n theo chiß╗üu t─āng ─æiß╗ćn t├Łch hß║Īt nh├ón.
C. ─Éß╗ŖNH LUß║¼T TUß║”N HO├ĆN
─Éß╗ŗnh luß║Łt tuß║¦n ho├Ān
─Éß╗ŗnh luß║Łt tuß║¦n ho├Ān: T├Łnh chß║źt cß╗¦a c├Īc nguy├¬n tß╗æ v├Ā ─æŲĪn chß║źt, c┼®ng nhŲ░ th├Ānh phß║¦n v├Ā t├Łnh chß║źt cß╗¦a c├Īc hß╗Żp chß║źt tß║Īo n├¬n tß╗½ c├Īc nguy├¬n tß╗æ ─æ├│ biß║┐n ─æß╗Ģi tuß║¦n ho├Ān theo chiß╗üu t─āng cß╗¦a ─æiß╗ćn t├Łch hß║Īt nh├ón nguy├¬n tß╗Ł.
├Ø ngh─®a cß╗¦a bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc
Khi biß║┐t vß╗ŗ tr├Ł cß╗¦a mß╗Öt nguy├¬n tß╗æ trong bß║Żng tuß║¦n ho├Ān, c├│ thß╗ā ─æŲ░a ra dß╗▒ ─æo├Īn vß╗ü t├Łnh chß║źt cß╗¦a ─æŲĪn chß║źt c┼®ng nhŲ░ hß╗Żp chß║źt cß╗¦a n├│.
1.3. LI├ŖN Kß║ŠT H├ōA Hß╗īC
A. QUY TẮC OCTET
- Li├¬n kß║┐t ho├Ī hß╗Źc l├Ā sß╗▒ kß║┐t hß╗Żp giß╗»a c├Īc nguy├¬n tß╗Ł tß║Īo th├Ānh ph├ón tß╗Ł hay tinh thß╗ā bß╗ün vß╗»ng hŲĪn.
- Quy tß║»c octet: Khi h├¼nh th├Ānh li├¬n kß║┐t ho├Ī hß╗Źc, c├Īc nguy├¬n tß╗Ł c├│ xu hŲ░ß╗øng nhŲ░ß╗Øng, nhß║Łn hoß║Ęc g├│p chung electron ─æß╗ā ─æß║Īt tß╗øi cß║źu h├¼nh electron bß╗ün vß╗»ng cß╗¦a nguy├¬n tß╗Ł kh├Ł hiß║┐m.
B. LI├ŖN Kß║ŠT ION
- Li├¬n kß║┐t ion ─æŲ░ß╗Żc h├¼nh th├Ānh bß╗¤i lß╗▒c h├║t t─®nh ─æiß╗ćn giß╗»a c├Īc ion tr├Īi dß║źu.
- Li├¬n kß║┐t ion thŲ░ß╗Øng ─æŲ░ß╗Żc h├¼nh th├Ānh giß╗»a kim loß║Īi ─æiß╗ān h├¼nh v├Ā phi kim ─æiß╗ān h├¼nh. Hß╗Żp chß║źt ion ─æŲ░ß╗Żc tß║Īo n├¬n tß╗½ cation v├Ā anion.
- ß╗× ─æiß╗üu kiß╗ćn thŲ░ß╗Øng, hß╗Żp chß║źt ion thŲ░ß╗Øng tß╗ōn tß║Īi ß╗¤ dß║Īng tinh thß╗ā rß║»n.
C. LI├ŖN Kß║ŠT Cß╗śNG H├ōA TRß╗Ŗ
- Li├¬n kß║┐t cß╗Öng h├│a trß╗ŗ: H├¼nh th├Ānh do mß╗Öt hay nhiß╗üu cß║Ęp electron d├╣ng chung giß╗»a 2 nguy├¬n tß╗Ł
+ Li├¬n kß║┐t cß╗Öng h├│a trß╗ŗ kh├┤ng cß╗▒c
+ Li├¬n kß║┐t cß╗Öng h├│a trß╗ŗ c├│ cß╗▒c
+ Li├¬n kß║┐t cho ŌĆō nhß║Łn
- Sß╗▒ xen phß╗¦ orbital theo trß╗źc li├¬n kß║┐t tß║Īo ra li├¬n kß║┐t \(\sigma \). Sß╗▒ xen phß╗¦ b├¬n cß╗¦a c├Īc orbital tß║Īo ra li├¬n kß║┐t \(\pi \)
- C├Īc li├¬n kß║┐t cß╗Öng ho├Ī trß╗ŗ ─æŲĪn ─æß╗üu l├Ā li├¬n kß║┐t \(\sigma \), 1 li├¬n kß║┐t ─æ├┤i gß╗ōm 1 li├¬n kß║┐t \(\sigma \) v├Ā 1 li├¬n kß║┐t \(\pi \), 1 li├¬n kß║┐t ba gß╗ōm li├¬n kß║┐t \(\sigma \) v├Ā 2 li├¬n kß║┐t \(\pi \)
- N─āng lŲ░ß╗Żng li├¬n kß║┐t l├Ā n─āng lŲ░ß╗Żng cß║¦n thiß║┐t ─æß╗ā ph├Ī vß╗Ī mß╗Öt li├¬n kß║┐t x├Īc ─æß╗ŗnh trong ph├ón tß╗Ł ß╗¤ thß╗ā kh├Ł, tß║Īi 25┬░C v├Ā 1 bar. ─ÉŲĪn vß╗ŗ cß╗¦a n─āng lŲ░ß╗Żng li├¬n kß║┐t thŲ░ß╗Øng l├Ā k mol-1. N─āng lŲ░ß╗Żng li├¬n kß║┐t c├Āng lß╗øn, li├¬n kß║┐t c├Āng bß╗ün.
- Dß╗▒a tr├¬n hiß╗ću ─æß╗Ö ├óm ─æiß╗ćn x├Īc ─æß╗ŗnh loß║Īi li├¬n kß║┐t h├│a hß╗Źc:
|
Hiß╗ću ─æß╗Ö ├óm ─æiß╗ćn (Ōłåx) |
Loß║Īi li├¬n kß║┐t |
|
0 Ōēż Ōłåx < 0,4 |
Cß╗Öng h├│a trß╗ŗ kh├┤ng cß╗▒c |
|
0,4 Ōēż Ōłåx < 1,7 |
Cß╗Öng h├│a trß╗ŗ c├│ cß╗▒c |
|
Ōēź 1,7 |
Ion |
D. LI├ŖN Kß║ŠT HYDROGEN V├Ć TŲ»ŲĀNG T├üC VAN DER WAALS
- Li├¬n kß║┐t hydrogen l├Ā mß╗Öt loß║Īi li├¬n kß║┐t yß║┐u ─æŲ░ß╗Żc h├¼nh th├Ānh giß╗»a nguy├¬n tß╗Ł H (─æ├Ż li├¬n kß║┐t vß╗øi mß╗Öt nguy├¬n tß╗Ł c├│ ─æß╗Ö ├óm ─æiß╗ćn lß╗øn) vß╗øi mß╗Öt nguy├¬n tß╗Ł kh├Īc (c├│ ─æß╗Ö ├óm ─æiß╗ćn lß╗øn) c├▓n cß║Ęp electron ri├¬ng. C├Īc nguy├¬n tß╗Ł c├│ ─æß╗Ö ├óm ─æiß╗ćn lß╗øn thŲ░ß╗Øng gß║Ęp trong li├¬n kß║┐t hydrogen l├Ā N, O, F.
- TŲ░ŲĪng t├Īc van der Waals l├Ā mß╗Öt loß║Īi li├¬n kß║┐t rß║źt yß║┐u, tß║Īo th├Ānh bß╗¤i tŲ░ŲĪng t├Īc h├║t t─®nh ─æiß╗ćn giß╗»a c├Īc cß╗▒c tr├Īi dß║źu cß╗¦a ph├ón tß╗Ł.
- Li├¬n kß║┐t hydrogen v├Ā tŲ░ŲĪng t├Īc van der Waals l├Ām t─āng nhiß╗ćt ─æß╗Ö n├│ng chß║Ży v├Ā nhiß╗ćt ─æß╗Ö s├┤i cß╗¦a c├Īc chß║źt. Trong ─æ├│, li├¬n kß║┐t hydrogen c├│ ß║Żnh hŲ░ß╗¤ng mß║Īnh hŲĪn.
2. B├ĆI Tß║¼P
C├óu 1: Nguy├¬n tß╗Ł trung h├▓a v├¼ ─æiß╗ćn v├¼
A. tß╗Ģng sß╗æ hß║Īt neutron bß║▒ng tß╗Ģng sß╗æ hß║Īt proton.
B. ─æŲ░ß╗Żc tß║Īo th├Ānh tß╗½ c├Īc hß║Īt kh├┤ng mang ─æiß╗ćn.
C. c├│ tß╗Ģng sß╗æ hß║Īt electron bß║▒ng tß╗Ģng sß╗æ hß║Īt proton.
D. c├│ tß╗Ģng sß╗æ hß║Īt electron bß║▒ng tß╗Ģng sß╗æ hß║Īt neutron.
C├óu 2: Mß╗Öt loß║Īi nguy├¬n tß╗Ł potassium c├│ 19 proton, 19 electron v├Ā 20 neutron. Sß╗æ khß╗æi cß╗¦a nguy├¬n tß╗Ł n├Āy l├Ā
A. 38. ŌĆāŌĆā
B. 39. ŌĆāŌĆā
C. 40. ŌĆāŌĆā
D. 58.
C├óu 3: Ph├Īt biß╗āu n├Āo sau ─æ├óy kh├┤ng ─æ├║ng?
A. Hß║¦u hß║┐t c├Īc nguy├¬n tß╗Ł ─æŲ░ß╗Żc cß║źu th├Ānh tß╗½ c├Īc hß║Īt cŲĪ bß║Żn l├Ā proton, neutron v├Ā electron.
B. Nguy├¬n tß╗Ł c├│ cß║źu tr├║c ─æß║Ęc kh├Łt, gß╗ōm vß╗Å nguy├¬n tß╗Ł v├Ā hß║Īt nh├ón nguy├¬n tß╗Ł.
C. Hß║Īt nh├ón cß╗¦a hß║¦u hß║┐t nguy├¬n tß╗Ł cß║źu th├Ānh tß╗½ c├Īc hß║Īt proton v├Ā neutron.
D. Vß╗Å nguy├¬n tß╗Ł cß║źu th├Ānh tß╗½ c├Īc hß║Īt electron.
C├óu 4: Trong tß╗▒ nhi├¬n, ─æß╗ōng (copper) c├│ hai ─æß╗ōng vß╗ŗ bß╗ün l├Ā v├Ā . Nguy├¬n tß╗Ł khß╗æi trung b├¼nh cß╗¦a ─æß╗ōng l├Ā 63,54. Phß║¦n tr─ām sß╗æ nguy├¬n tß╗Ł cß╗¦a ─æß╗ōng vß╗ŗ l├Ā
A. 63%.
B. 73%.
C. 65%.
D. 27%.
C├óu 5: Ph├Īt biß╗āu n├Āo sau ─æ├óy ─æ├║ng?
A. C├Īc nguy├¬n tß╗Ł cß╗¦a nguy├¬n tß╗æ kh├Ł hiß║┐m ─æß╗üu c├│ 8 electron lß╗øp ngo├Āi c├╣ng.
B. C├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ 1, 2 hoß║Ęc 3 electron lß╗øp ngo├Āi c├╣ng ─æß╗üu l├Ā kim loß║Īi.
C. Chß╗ē c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ 5, 6 hoß║Ęc 7 electron lß╗øp ngo├Āi c├╣ng mß╗øi l├Ā phi kim.
D. Nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ 4 electron lß╗øp ngo├Āi c├╣ng c├│ thß╗ā l├Ā kim loß║Īi hoß║Ęc phi kim
C├óu 6: Sß╗æ orbital trong c├Īc ph├ón lß╗øp s, p, d lß║¦n lŲ░ß╗Żt l├Ā
A. 1, 3, 5.
B. 1, 2, 4.
C. 3, 5, 7.
D. 1, 2, 3.
C├óu 7: Sß╗æ electron tß╗æi ─æa c├│ trong lß╗øp M l├Ā
A. 3. ŌĆāŌĆā
B. 4. ŌĆāŌĆā
C. 9. ŌĆāŌĆā
D. 18.
C├óu 8: ß╗× trß║Īng th├Īi cŲĪ bß║Żn, nguy├¬n tß╗Ł calcium (Z = 20) c├│ sß╗æ electron ─æß╗Öc th├ón l├Ā
A. 1. ŌĆāŌĆā
B. 2. ŌĆāŌĆā
C. 0. ŌĆāŌĆā
D. 4.
C├óu 9: Cho c├Īc cß║źu h├¼nh electron sau:
(1) 1s22s1
(2) 1s22s22p4
(3) 1s22s22p63s23p63d104s24p5
(4) 1s22s22p63s23p1
Sß╗æ cß║źu h├¼nh electron cß╗¦a nguy├¬n tß╗æ phi kim l├Ā
A. 4. ŌĆāŌĆā
B. 2. ŌĆāŌĆā
C. 1. ŌĆāŌĆā
D. 7.
C├óu 10: Trong bß║Żng hß╗ć thß╗æng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc, sß╗æ chu k├¼ nhß╗Å v├Ā chu k├¼ lß╗øn lß║¦n lŲ░ß╗Żt l├Ā
A. 3 v├Ā 3.
B. 4 v├Ā 3.
C. 3 v├Ā 4.
D. 4 v├Ā 4.
C├óu 11: Nguy├¬n tß╗Ł Y c├│ tß╗Ģng sß╗æ hß║Īt mang ─æiß╗ćn trong nguy├¬n tß╗Ł l├Ā 34. Sß╗æ hß║Īt mang ─æiß╗ćn nhiß╗üu hŲĪn sß╗æ hß║Īt kh├┤ng mang ─æiß╗ćn 10 hß║Īt. Vß╗ŗ tr├Ł cß╗¦a Y trong bß║Żng tuß║¦n ho├Ān l├Ā
A. sß╗æ thß╗® tß╗▒ 17, chu k├¼ 3, nh├│m VIIA.
B. sß╗æ thß╗® tß╗▒ 11, chu k├¼ 3, nh├│m IA.
C. sß╗æ thß╗® tß╗▒ 11, chu k├¼ 2, nh├│m VIIA
D. sß╗æ thß╗® tß╗▒ 17, chu k├¼ 3, nh├│m IA.
C├óu 12: Trong mß╗Öt nh├│m A, theo chiß╗üu tß╗½ tr├¬n xuß╗æng dŲ░ß╗øi, b├Īn k├Łnh nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ
A. t─āng dß║¦n.
B. giß║Żm dß║¦n.
C. kh├┤ng thay ─æß╗Ģi.
D. biß║┐n ─æß╗Ģi kh├┤ng theo quy luß║Łt.
C├óu 13: Ph├Īt biß╗āu n├Āo sau ─æ├óy kh├┤ng ─æ├║ng?
A. Trong bß║Żng tuß║¦n ho├Ān, fluorine (F) l├Ā nguy├¬n tß╗æ c├│ ─æß╗Ö ├óm ─æiß╗ćn lß╗øn nhß║źt.
B. Trong mß╗Öt nh├│m A, khi ─æiß╗ćn t├Łch hß║Īt nh├ón t─āng l├¬n th├¼ ─æß╗Ö ├óm ─æiß╗ćn c┼®ng t─āng l├¬n.
C. B├Īn k├Łnh nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ trong c├╣ng mß╗Öt chu k├¼ giß║Żm tß╗½ tr├Īi qua phß║Żi.
D. ─Éß╗Ö ├óm ─æiß╗ćn ─æß║Ęc trŲ░ng cho khß║Ż n─āng h├║t electron li├¬n kß║┐t cß╗¦a mß╗Öt nguy├¬n tß╗Ł trong ph├ón tß╗Ł.
C├óu 14: Oxide n├Āo dŲ░ß╗øi ─æ├óy l├Ā oxide lŲ░ß╗Īng t├Łnh?
A. Na2O.
B. SO2.
C. MgO.
D. Al2O3.
C├óu 15: C├┤ng thß╗®c oxide cao nhß║źt cß╗¦a nguy├¬n tß╗æ R (Z = 15) l├Ā
A. R2O.
B. R2O3.
C. R2O5.
D. R2O7.
ĐÁP ÁN
|
1C |
2B |
3B |
4B |
5D |
6A |
7D |
8C |
9B |
10C |
|
11B |
12A |
13B |
14D |
15C |
16D |
17C |
18C |
19D |
20A |
|
21D |
22D |
23B |
24D |
25B |
26C |
27D |
28A |
29B |
30D |
Tr├¬n ─æ├óy l├Ā mß╗Öt phß║¦n tr├Łch ─æoß║Īn nß╗Öi dung ─Éß╗ü cŲ░ŲĪng ├┤n tß║Łp HK1 m├┤n H├│a hß╗Źc 10 C├Īnh Diß╗üu n─ām 2022-2023. ─Éß╗ā xem to├Ān bß╗Ö nß╗Öi dung c├Īc em chß╗Źn chß╗®c n─āng xem online hoß║Ęc ─æ─āng nhß║Łp v├Āo trang hoc247.net ─æß╗ā tß║Żi t├Āi liß╗ću vß╗ü m├Īy t├Łnh.
Mß╗Øi c├Īc em tham khß║Żo t├Āi liß╗ću c├│ li├¬n quan:
- ─Éß╗ü cŲ░ŲĪng ├┤n tß║Łp HK1 m├┤n ─Éß╗ŗa l├Ł 10 C├Īnh diß╗üu n─ām 2022-2023
- ─Éß╗ü cŲ░ŲĪng ├┤n tß║Łp HK1 m├┤n Tiß║┐ng Anh 10 C├Īnh diß╗üu n─ām 2022-2023
Hy vß╗Źng t├Āi liß╗ću n├Āy sß║Į gi├║p c├Īc em hß╗Źc sinh ├┤n tß║Łp tß╗æt v├Ā ─æß║Īt th├Ānh t├Łch cao trong hß╗Źc tß║Łp.
T├Āi liß╗ću li├¬n quan
TŲ░ liß╗ću nß╗Ģi bß║Łt tuß║¦n
- Xem thêm


.JPG?enablejsapi=1)
.JPG)










