Giải bài 6.15 trang 20 SBT Khoa học tự nhiên 7 Chân trời sáng tạo
Magnesium oxide (gồm 1 nguyên tử magnesium và 1 nguyên tử oxygen) có nhiều ứng dụng trong đời sống. Nó là thành phần chính trong các lò sản xuất sắt, thép, các kim loại màu, thuỷ tỉnh hay xi măng, .. Em hãy cho biết thêm các ứng dụng khác của magnesium oxide. Vẽ sơ đồ hình thành liên kết tạo ra phân tử magnesium oxide và tính khối lượng phân tử của nó.

Hướng dẫn giải chi tiết bài 6.15
Phương pháp giải:
Khối lượng phân tử (KLPT) của một chất bằng tổng khối lượng của các nguyên tử trong phân tử khối của chất đó.
Lời giải chi tiết:
- Các ứng dụng khác của magnesium oxide:
+ xử lý nước thải, nước sinh hoạt, xử lý đất, xử lý nước ngầm,… để ổn định pH.
+ giúp cơ thể cải thiện chứng khó tiêu, ổn định acid trong dạ dạy,…
+ dùng làm lõi cửa chống cháy,…
- Sự hình thành phân tử magnesium oxide:
+ Nguyên tử của nguyên tố magnesium nhường 2 electron lớp ngoài cùng để tạo thành ion dương có 8 electron lớp ngoài cùng bền vững.
+ Nguyên tử của nguyên tố oxygen nhận 2 electron để tạo ion âm có 8 electron lớp ngoài cùng bền vững.
+ Hai ion trái dấu hút nhau bằng lực hút tĩnh điện và tạo thành liên kết ion.
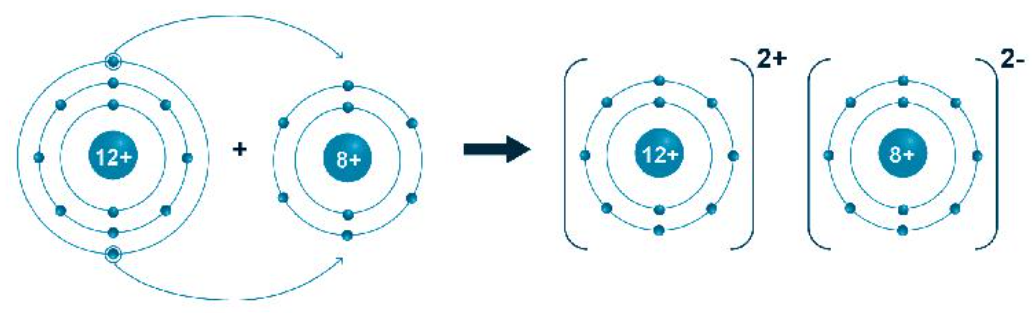
- Phân tử magnesium oxide được tạo bởi một nguyên tử của nguyên tố Mg và một nguyên tử của nguyên tố O.
- KLPT (MgO) = 1.24 + 1.16 = 40 (amu)
-- Mod Khoa học tự nhiên 7 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.
Bài tập SGK khác
Giải bài 6.13 trang 20 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.14 trang 20 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.16 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.17 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.18 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.19 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.20 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.21 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 6.22 trang 21 SBT Khoa học tự nhiên 7 Chân trời sáng tạo - CTST





