Với mong muốn giúp các em ôn luyện thật tốt, ban biên tập HOC247 đã biên soạn Đề cương ôn tập HK1 môn Hóa 9 năm 2020 trường THCS Trần Cao Vân có đáp án bên dưới đây. Tài liệu bao gồm phần tóm tắt kiến thức cơ bản và bài tập tham khảo để các em nắm vững lý thuyết và rèn luyện kĩ năng làm bài tập. Mời các em cùng tham khảo.
TRƯỜNG THCS TRẦN CAO VÂN
ĐỀ CƯƠNG ÔN TẬP HỌC KÌ I MÔN HÓA HỌC 9
A. KIẾN THỨC CƠ BẢN
I- Mối quan hệ giữa các hợp chất vô cơ
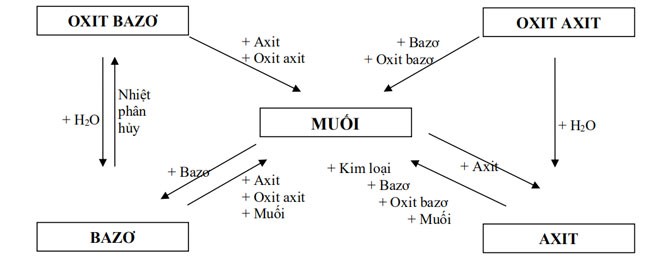
II – Các loại hợp chất vô cơ
OXIT
a) Định nghĩa: Oxit là hợp chất gồm 2 nguyên tố, trong đó có một nguyên tố là oxi.
Vd: CaO, SO2, CO, Na2O, Fe3O4, P2O5, …
b) Tính chất hóa học:
|
Tính chất hóa học |
OXIT AXIT |
OXIT BAZƠ |
|
1. Tác dụng với nước |
Một số oxit axit (SO2, CO2, N2O5, P2O5, …) + nước à dd axit Vd: CO2 + H2O → H2CO3 P2O5 + 3H2O → 2H3PO4 |
Một số oxit bazơ (Na2O, BaO, CaO, K2O, …) + nước à dd bazơ Vd: Na2O + H2O → 2NaOH Ø Các oxit bazơ như: MgO, CuO, Al2O3, FeO, Fe2O3, … không tác dụng với nước. |
|
2. Tác dụng với axit |
< Không phản ứng > |
Oxit bazơ + axit à muối + nước Vd: CuO + 2HCl → CuCl2 + H2O CaO + H2SO4 → CaSO4 + H2O |
|
3. Tác dụng với dd bazơ (kiềm) |
Oxit axit + dd bazơ à muối + nước Vd: SO2 + Ca(OH)2 → CaSO3 + H2O CO2 + Ba(OH)2→ BaCO3 + H2O |
< Không phản ứng > |
|
4. Tác dụng với oxit axit |
< Không phản ứng > |
Oxit bazơ + oxit axit à muối Vd: CaO + CO2 → CaCO3 |
|
5. Tác dụng với oxit bazơ |
Oxit axit + oxit bazơ à muối Vd: SO2 + BaO → BaSO3 |
< Không phản ứng > |
AXIT
a) Định nghĩa:Axit là hợp chất mà phân tử gồm có một hay nhiều nguyên tử H liên kết với gốc axit. Các nguyên tử H này có thể thay thế bằng các ng/tử kim loại.
Vd: HCl, HNO3, H2SO4, H3PO4, …
b) Tính chất hóa học:
|
1. Tác dụng với chất chỉ thị: Dd axit làm giấy quỳ tím chuyển sang màu đỏ. 2. Tác dụng với kim loại: Một số dd axit (HCl, H2SO4 loãng) + các kim loại đứng trước H (trong dãy HĐHH của kim loại) à muối + H2 Vd: 2Al + 3H2SO4loãng → Al2(SO4)3 +3H2 Zn + 2HCl → ZnCl2 + H2 Ø H2SO4 đặc và HNO3 tác dụng với hầu hết các kim loại tạo muối nhưng không giải phóng khí H2. Vd: Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O - H2SO4 đặc có tính háo nước. |
3. Tác dụng với oxit bazơ: Axit + oxit bazơ à muối + nước Vd: CaO + H2SO4 → CaSO4 + H2O 4. Tác dụng với bazơ: Axit + bazơ à muối + nước (phản ứng trung hòa) Vd: 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O 5. Tác dụng với muối: Axit + muối à muối mới + axit mới Vd: H2SO4 + BaCl2 → BaSO4 + 2HCl 2HCl + Na2CO3 → 2NaCl + H2O + CO2‹ - Điều kiện phản ứng xảy ra: Sản phẩm phải có chất không tan hoặc chất khí. |
B. BÀI TẬP THAM KHẢO
Câu 1: Viết các phương trình hóa học thực hiện chuỗi biến hóa sau đây, ghi rõ điều kiện phản ứng (nếu có):
\(Mg\xrightarrow{{(1)}}Mg{\text{S}}{O_4}\xrightarrow{{(2)}}Mg{(OH)_2}\xrightarrow{{(3)}}MgC{l_2}\xrightarrow{{(4)}}Mg{(N{O_3})_2}\)
Trả lời:
\(Mg + {H_2}S{O_4} \to Mg{\text{S}}{O_4} + {H_2}\)
\(Mg{\text{S}}{O_4} + 2NaOH \to Mg{(OH)_2} + N{a_2}S{O_4}\)
\(Mg{(OH)_2} + 2HCl \to MgC{l_2} + 2{H_2}O\)
\(MgC{l_2} + 2AgN{O_3} \to 2AgCl + Mg{(N{O_3})_2}\)
Câu 2 : Cho các kim loại sau: Mg, Cu, Al, Ag
a/ Hãy sắp xếp các kim loại trên theo chiều mức độ hoạt động hóa học giảm dần.
b/ Các kim loại trên kim loại nào tác dụng được với dung dịch HCl. Viết các phương trình hóa học xảy ra.
c/ Trong các kim loại trên kim loại nào được sử dụng làm bình đựng axit H2SO4 đặc nguội? Giải thích.
Trả lời:
a/ Thứ tự kim loại theo chiều mức độ hoạt động hóa học giảm dần là: Mg, Al, Cu, Ag.
b/ Các kim loại tác dụng được với dung dịch HCl là Al và Mg
\(2{\text{A}}l + 6HCl \to 2{\text{A}}lC{l_3} + 3{H_2}\)
\(Mg + 2HCl \to MgC{l_2} + {H_2}\)
c/ Kim loại Al được sử dụng làm bình đựng axit H2SO4 đặc nguội, do Al bị thụ động hóa với axit H2SO4 đặc nguội.
---(Để xem tiếp nội dung của đề cương các em vui lòng xem tại online hoặc đăng nhập để tải về máy)---
Trên đây là trích dẫn một phần nội dung Đề cương ôn tập HK1 môn Hóa 9 năm 2020 trường THCS Trần Cao Vân có đáp án. Để theo dõi nhiều tài liệu tham khảo hữu ích khác, các em vui lòng đăng nhập vào hệ thống hoc247.net chọn chức năng xem online hoặc tải về máy!
Ngoài ra các em học sinh có thể tham khảo các tài liệu cùng chuyên mục:
- Bộ 2 đề thi HK1 môn Hóa học 9 năm 2020 - Trường THCS Nguyễn Trường Tộ có đáp án
- Đề thi HK1 môn Hóa học 9 năm 2020 - Trường THCS Trần Quốc Tuấn có đáp án
Chúc các em học tập thật tốt!






