Hướng dẫn Giải bài tập Hóa học 10 Kết nối tri thức Bài 11 Bài 11: Liên kết ion môn Hóa học lớp 10 KNTT giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức.
-
Giải câu hỏi 1 trang 52 SGK Hóa học 10 Kết nối tri thức - KNTT
Hoàn thành các sơ đồ tạo thành ion sau:
a) Li → Li+ + ?
b) Be → ? + 2e
c) Br + ? → Br-
d) O +2e → ?
-
Giải câu hỏi 2 trang 52 SGK Hóa học 10 Kết nối tri thức - KNTT
Viết cấu hình electron của các ion K+, Mg2+, F-, S2-. Mỗi cấu hình đó giống với cấu hình electron của nguyên tử khí hiếm nào?
-
Giải câu hỏi 3 trang 52 SGK Hóa học 10 Kết nối tri thức - KNTT
Vì sao một ion O2- kết hợp được với hai ion Li+?
-
Giải câu hỏi 4 trang 52 SGK Hóa học 10 Kết nối tri thức - KNTT
Cho các ion: Na+ , Mg2+, O2-, Cl-. Những ion nào có thể kết hợp với nhau tạo thành liên kết ion?
-
Giải câu hỏi 5 trang 52 SGK Hóa học 10 Kết nối tri thức - KNTT
Mô tả sự tạo thành liên kết ion trong:
a) Calcium oxide
b) Magnesium chloride.
-
Hoạt động trang 53 SGK Hóa học 10 Kết nối tri thức - KNTT
Lắp ráp mô hình tinh thể NaCl
Chuẩn bị: bộ mô hình tinh thể NaCl.
Tiến hành:
- Chọn hình cầu có màu sắc khác nhau đại diện cho ion Na+ và ion Cl-.
- Lắp các hình cầu và que nối theo mẫu (Hình 11.1b).
Quan sát mô hình và xác định số ion gần nhất bao quanh một ion trái dấu ở giữa mô hình.
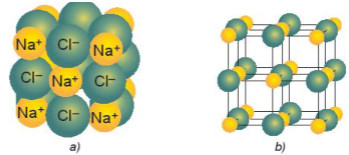
Hình 11.1. Sự sắp xếp các ion trong tinh thể sodium chloride
a) Mô hình đặc b) Mô hình rỗng
-
Hoạt động trang 54 SGK Hóa học 10 Kết nối tri thức - KNTT
Thử tính dẫn điện của hợp chất
Chuẩn bị: muối ăn dạng hạt, dung dịch muối ăn bão hòa, dung dịch nước đường, dụng cụ thử tính dẫn điện, cốc thủy tinh.
Tiến hành: Sử dụng dụng cụ thử tính dẫn điện như Hình 11.3, lần lượt cho chân kim loại của dụng cụ thử tính dẫn điện tiếp xúc với:
- Dung dịch nước đường
- Muối ăn khan.
- Dung dịch muối ăn bão hòa.
Nếu đèn sáng thì chất dẫn điện nếu đèn không sáng thì chất không dẫn điện.
Quan sát hiện tượng và cho biết trường hợp nào dẫn điện, trường hợp nào không dẫn điện. Giải thích.

-
Giải câu hỏi 6 trang 54 SGK Hóa học 10 Kết nối tri thức - KNTT
a) Vì sao muối ăn có nhiệt độ nóng chảy cao (8010C)?
b) Hợp chất ion dẫn điện trong trường hợp nào? Vì sao?
-
Giải bài 11.1 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Liên kết ion được tạo thành giữa hai nguyên tử bằng
A. một hay nhiều cặp electron dùng chung.
B. một hay nhiều cặp electron dùng chung chỉ do một nguyên tử đóng góp.
C. lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
D. một hay nhiều cặp electron dùng chung và các cặp electron này lệch về nguyên tử có độ âm điện lớn hơn.
-
Giải bài 11.2 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Liên kết ion là loại liên kết hoá học được hình thành nhờ lực hút tĩnh điện giữa các phần tử nào sau đây?
A. cation và anion.
B. các anion
C. cation và electron tự do.
D. electron và hạt nhân nguyên tử.
-
Giải bài 11.3 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Biểu diễn sự tạo thành ion nào sau đây đúng?
A. Na + le -> Na+.
B. Cl2 -> 2Cl- + 2e.
C. O2 + 2e -> 2O2-.
D. Al -> Al3+ + 3e.
-
Giải bài 11.4 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Số electron và số proton trong ion NH4+ là
A. 11 electron và 11 proton.
B. 10 electron và 11 proton.
C. 11 electron và 10 proton.
D 11 electron và 12 proton.
-
Giải bài 11.5 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Cặp nguyên tử nào sau đây không tạo hợp chất dạng X2+Y2- hoặc X2+Y2-?
A. Na và O.
B. K và S.
C. Ca và O.
D. Ca và Cl.
-
Giải bài 11.6 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Tính chất nào sau đây là tính chất của hợp chất ion?
A. Hợp chất ion có nhiệt độ nóng chảy thấp.
B. Hợp chất ion có nhiệt độ nóng chảy cao.
C. Hợp chất ion dễ hoả lỏng.
D. Hợp chất ion có nhiệt độ sôi không xác định.
-
Giải bài 11.7 trang 30 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho các phân tử sau: HCl, NaCl, CaCl2, AlCl3. Phân tử có liên kết mang nhiều tính chất ion nhất là
A. HCl.
B. NaCl.
C. CaCl2.
D. AlCl3.
-
Giải bài 11.8 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Dãy gồm các phân tử đều có liên kết ion là
A. Cl2, Br2, I2, HCl.
B. HCl, H2S, NaCl, N2O.
C. Na2O, KCl, BaCl2, Al2O3.
D. MgO, H2SO4, H3PO4, HCl.
-
Giải bài 11.9 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho các ion sau: K+; Be2+; Cr3+; F-; Se2- ;N3-. Viết phương trình biểu diễn sự hình thành mỗi ion trên.
-
Giải bài 11.10 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho các ion sau: 20Ca2+; 13Al3+; 9F-; 16S2-; 7N3-.
a) Viết cấu hình electron của mỗi ion.
b) Mỗi cấu hình đã viết giống với cấu hình electron của nguyên tử nào?
-
Giải bài 11.11 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Vì sao các hợp chất ion thường là chất rắn ở nhiệt độ phòng?
-
Giải bài 11.12 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho các chất sau: K2O, H2O, H2S, SO2, NaCl, K2S, CaF2, HCl. Trong phân tử chất nào có liên kết ion?
-
Giải bài 11.13 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Kể ra những hợp chất ion tạo thành từ các ion sau F-, K+, O2-, Ca2+.
-
Giải bài 11.14 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Dùng sơ đồ để biểu diễn sự hình thành liên kết trong mỗi hợp chất ion sau đây:
a) magnesium fluoride (MgF2);
b) potassium fluoride (KF);
c) sodium oxide (Na2O);
d) calcium oxide (CaO).
-
Giải bài 11.15 trang 31 SBT Hóa học 10 Kết nối tri thức - KNTT
Anion X- có cấu hình electron nguyên tử ở phân lớp ngoài cùng là 3p6.
a) Viết cấu hình electron của nguyên tử X. Cho biết X là nguyên tố kim loại hay phi kim.
b) Giải thích bản chất liên kết giữa X với barium.






