HŲ░ß╗øng dß║½n Giß║Żi b├Āi tß║Łp H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo B├Āi 5 B├Āi 5: Cß║źu tß║Īo bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc lß╗øp 10 CTST gi├║p c├Īc em hß╗Źc sinh nß║»m vß╗»ng phŲ░ŲĪng ph├Īp giß║Żi b├Āi tß║Łp v├Ā ├┤n luyß╗ćn tß╗æt kiß║┐n thß╗®c.
-
Giß║Żi c├óu hß╗Åi 1 trang 36 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.1, h├Ży m├┤ tß║Ż bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc cß╗¦a Mendeleev. Nhß║Łn x├®t vß╗ü c├Īch sß║»p xß║┐p c├Īc nguy├¬n tß╗æ h├│a hß╗Źc theo chiß╗üu tß╗½ tr├¬n xuß╗æng dŲ░ß╗øi trong c├╣ng mß╗Öt cß╗Öt
.jpg)
H├¼nh 5.1. Bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc cß╗¦a Mendeleev (1869)
-
Giß║Żi c├óu hß╗Åi 2 trang 36 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt hai nguy├¬n tß╗æ Te v├Ā I trong H├¼nh 5.1, em nhß║Łn thß║źy ─æiß╗üu g├¼ kh├Īc thŲ░ß╗Øng?
.jpg)
H├¼nh 5.1. Bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc cß╗¦a Mendeleev (1869)
-
Giß║Żi c├óu hß╗Åi 3 trang 36 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
H├Ży cho biß║┐t c├Īc dß║źu chß║źm hß╗Åi trong bß║Żng tuß║¦n ho├Ān ß╗¤ H├¼nh 5.1 c├│ h├Ām ├Į g├¼?
.jpg)
H├¼nh 5.1. Bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc cß╗¦a Mendeleev (1869)
-
Giß║Żi c├óu hß╗Åi 4 trang 36 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.2, h├Ży cho biß║┐t 3 nguy├¬n tß╗æ Sc, Ga v├Ā Ge nß║▒m ß╗¤ vß╗ŗ tr├Ł n├Āo trong bß║Żng tuß║¦n ho├Ān cß╗¦a Mendeleev (H├¼nh 5.1)
-
Giß║Żi c├óu hß╗Åi 5 trang 38 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.3, em h├Ży n├¬u c├Īc th├┤ng tin c├│ trong ├┤ nguy├¬n tß╗æ aluminium
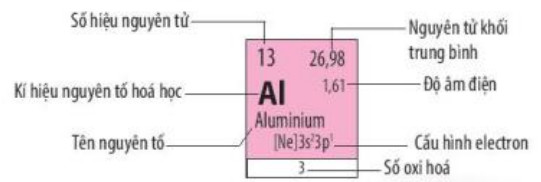
Hình 5.3. Ô nguyên tố aluminium
-
Luyß╗ćn tß║Łp 1 trang 38 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.3, cho biß║┐t sß╗æ electron lß╗øp ngo├Āi c├╣ng, sß╗æ proton cß╗¦a nguy├¬n tß╗Ł aluminium

Hình 5.3. Ô nguyên tố aluminium
-
Giß║Żi c├óu hß╗Åi 6 trang 38 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.4, h├Ży nhß║Łn x├®t vß╗ü sß╗æ lß╗øp electron trong nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ c├╣ng chu k├¼.
.jpg)
H├¼nh 5.4. C├Īc nguy├¬n tß╗æ thuß╗Öc chu k├¼ 2 v├Ā chu k├¼ 3
-
Luyß╗ćn tß║Łp 2 trang 38 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Dß╗▒a v├Āo cß║źu h├¼nh electron, em h├Ży cho biß║┐t nguy├¬n tß╗æ c├│ sß╗æ hiß╗ću nguy├¬n tß╗Ł l├Ā 20 thuß╗Öc chu k├¼ n├Āo trong bß║Żng tuß║¦n ho├Ān
-
Giß║Żi c├óu hß╗Åi 7 trang 38 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.2, nhß║Łn x├®t ─æß║Ęc ─æiß╗ām cß║źu h├¼nh electron nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ trong c├╣ng mß╗Öt nh├│m A
-
Giß║Żi c├óu hß╗Åi 8 trang 38 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt nh├│m VIIIB trong bß║Żng tuß║¦n ho├Ān, cho viß║┐t nh├│m n├Āy c├│ ─æß║Ęc ─æiß╗ām g├¼ kh├Īc biß╗ćt so vß╗øi c├Īc nh├│m c├▓n lß║Īi
-
Giß║Żi c├óu hß╗Åi 9 trang 39 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.5, nhß║Łn x├®t mß╗æi quan hß╗ć giß╗»a sß╗æ electron h├│a trß╗ŗ cß╗¦a nguy├¬n tß╗Ł vß╗øi sß╗æ thß╗® tß╗▒ nh├│m cß╗¦a nguy├¬n tß╗æ nh├│m A
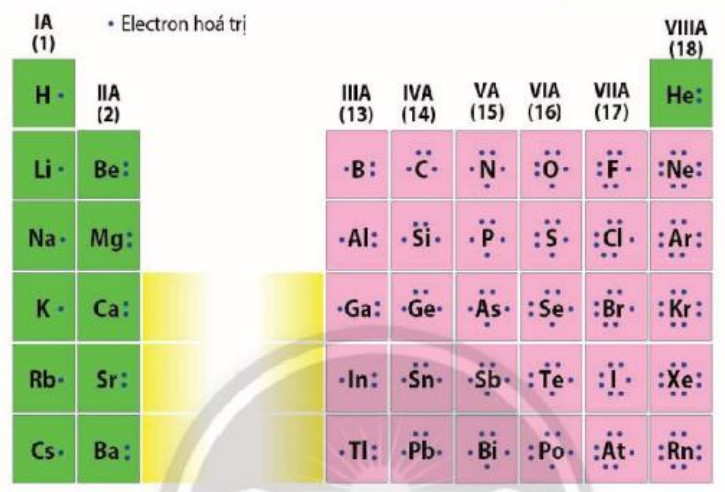
H├¼nh 5.5. Biß╗āu diß║┐n electron h├│a trß╗ŗ cß╗¦a c├Īc nguy├¬n tß╗æ nh├│m A
-
Giß║Żi c├óu hß╗Åi 10 trang 39 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.2, dß╗▒a v├Āo cß║źu h├¼nh electron nguy├¬n tß╗Ł, h├Ży nhß║Łn x├®t mß╗æi quan hß╗ć giß╗»a sß╗æ electron h├│a trß╗ŗ cß╗¦a nguy├¬n tß╗Ł c├Īc nguy├¬n tß╗æ vß╗øi sß╗æ thß╗® tß╗▒ nh├│m cß╗¦a nguy├¬n tß╗æ nh├│m B. N├¬u r├Ą c├Īc trŲ░ß╗Øng hß╗Żp ─æß║Ęc biß╗ćt.
-
Giß║Żi c├óu hß╗Åi 11 trang 39 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Dß╗▒a v├Āo cß║źu h├¼nh electron, cho biß║┐t nguy├¬n tß╗æ c├│ sß╗æ hiß╗ću nguy├¬n tß╗Ł l├Ā 6, 8, 18, 20 thuß╗Öc khß╗æi nguy├¬n tß╗æ n├Āo trong bß║Żng tuß║¦n ho├Ān. Ch├║ng l├Ā kim loß║Īi, phi kim hay kh├Ł hiß║┐m?
-
Luyß╗ćn tß║Łp trang 40 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Nitrogen l├Ā th├Ānh phß║¦n dinh dŲ░ß╗Īng cß║¦n thiß║┐t cho sß╗▒ sinh trŲ░ß╗¤ng, ph├Īt triß╗ān v├Ā sinh sß║Żn cß╗¦a thß╗▒c vß║Łt. Biß║┐t nitrogen c├│ sß╗æ hiß╗ću nguy├¬n tß╗Ł l├Ā 7.
a) Viß║┐t cß║źu h├¼nh electron cß╗¦a nitrogen
b) Nitrogen l├Ā nguy├¬n tß╗æ s, p, d hay f?
c) Nitrogen l├Ā kim loß║Īi, phi kim hay kh├Ł hiß║┐m?
-
Giß║Żi c├óu hß╗Åi 12 trang 40 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Quan s├Īt H├¼nh 5.2, nhß║Łn x├®t chiß╗üu t─āng ─æiß╗ćn t├Łch hß║Īt nh├ón nguy├¬n tß╗Ł c├Īc nguy├¬n tß╗æ trong chu k├¼ v├Ā nh├│m.
-
Vß║Łn dß╗źng trang 40 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Silicon l├Ā mß╗Öt nguy├¬n tß╗æ phß╗Ģ biß║┐n v├Ā c├│ nhiß╗üu ß╗®ng dß╗źng trong cuß╗Öc sß╗æng. Silicon si├¬u tinh khiß║┐t l├Ā chß║źt b├Īn dß║½n, ─æŲ░ß╗Żc d├╣ng trong k─® thuß║Łt v├┤ tuyß║┐n v├Ā ─æiß╗ćn tß╗Ł. Ngo├Āi ra, nguy├¬n tß╗æ n├Āy c├▓n ─æŲ░ß╗Żc sß╗Ł dß╗źng ─æß╗ā chß║┐ tß║Īo pin mß║Ęt trß╗Øi nhß║▒m mß╗źc ─æ├Łch chuyß╗ān ─æß╗Ģi n─āng lŲ░ß╗Żng ├Īnh s├Īng th├Ānh n─āng lŲ░ß╗Żng ─æiß╗ćn ─æß╗ā cung cß║źp cho c├Īc thiß║┐t bß╗ŗ tr├¬n t├Āu v┼® trß╗ź. X├Īc ─æß╗ŗnh vß╗ŗ tr├Ł cß╗¦a nguy├¬n tß╗æ silicon (Z = 14) trong bß║Żng tuß║¦n ho├Ān.
.jpg)
-
Giß║Żi b├Āi 1 trang 42 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Viß║┐t cß║źu h├¼nh electron nguy├¬n tß╗Ł v├Ā x├Īc ─æß╗ŗnh vß╗ŗ tr├Ł cß╗¦a c├Īc nguy├¬n tß╗æ sau trong bß║Żng tuß║¦n ho├Ān. Cho biß║┐t ch├║ng thuß╗Öc khß╗æi nguy├¬n tß╗æ n├Āo (s, p, d, f) v├Ā ch├║ng l├Ā kim loß║Īi, phi kim hay kh├Ł hiß║┐m:
a) Neon tß║Īo ra ├Īnh s├Īng m├Āu ─æß╗Å khi sß╗Ł dß╗źng trong c├Īc ß╗æng ph├│ng ─æiß╗ćn ch├ón kh├┤ng, ─æŲ░ß╗Żc sß╗Ł dß╗źng rß╗Öng r├Żi trong c├Īc biß╗ān quß║Żng c├Īo. Cho biß║┐t Ne c├│ sß╗æ hiß╗ću nguy├¬n tß╗Ł l├Ā 10.
b) Magnesium ─æŲ░ß╗Żc sß╗Ł dß╗źng ─æß╗ā l├Ām cho hß╗Żp kim bß╗ün nhß║╣, ─æß║Ęc biß╗ćt ─æŲ░ß╗Żc ß╗®ng dß╗źng cho ng├Ānh c├┤ng nghiß╗ćp h├Āng kh├┤ng. Cho biß║┐t Mg c├│ sß╗æ hiß╗ću nguy├¬n tß╗Ł l├Ā 12.
-
Giß║Żi b├Āi 2 trang 42 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
D├Ży n├Āo gß╗ōm c├Īc nguy├¬n tß╗æ c├│ t├Łnh chß║źt h├│a hß╗Źc tŲ░ŲĪng tß╗▒ nhau? V├¼ sao?
a) Oxygen (Z = 8), nitrogen (Z = 7), carbon (Z = 6)
b) Lithium (Z = 3), sodium (Z = 11), potassium (Z = 19)
c) Helium (Z = 2), neon (Z = 10), argon (Z = 18)
-
Giß║Żi b├Āi 3 trang 42 SGK H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Viß║┐t cß║źu h├¼nh electron nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ sau:
a) Nguyên tố thuộc chu kì 4, nhóm IIA
b) Nguy├¬n tß╗æ kh├Ł hiß║┐m thuß╗Öc chu k├¼ 3
-
Giß║Żi b├Āi 5.1 trang 19 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
X l├Ā nguy├¬n tß╗æ rß║źt cß║¦n thiß║┐t cho sß╗▒ chuyß╗ān h├│a cß╗¦a calcium, phosphorus, sodium, potassium, vitamin C v├Ā c├Īc vitamin nh├│m B. ß╗× trß║Īng th├Īi cŲĪ bß║Żn, cß║źu h├¼nh electron lß╗øp ngo├Āi c├╣ng cß╗¦a nguy├¬n tß╗Ł X l├Ā 3s2. Sß╗æ hiß╗ću nguy├¬n tß╗Ł cß╗¦a nguy├¬n tß╗æ X l├Ā
A. 12.
B. 13.
C. 11.
D. 14.
-
Giß║Żi b├Āi 5.2 trang 19 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Chu k├¼ l├Ā
A. d├Ży c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł cß╗¦a ch├║ng c├│ c├╣ng sß╗æ lß╗øp electron, ─æŲ░ß╗Żc xß║┐p theo chiß╗üu khß╗æi lŲ░ß╗Żng nguy├¬n tß╗Ł t─āng dß║¦n.
B. d├Ży c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł cß╗¦a ch├║ng c├│ c├╣ng sß╗æ lß╗øp electron, ─æŲ░ß╗Żc xß║┐p theo chiß╗üu sß╗æ khß╗æi t─āng dß║¦n.
C. d├Ży c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł cß╗¦a ch├║ng c├│ c├╣ng sß╗æ lß╗øp electron, ─æŲ░ß╗Żc xß║┐p theo chiß╗üu ─æiß╗ćn t├Łch hß║Īt nh├ón nguy├¬n tß╗Ł t─āng dß║¦n.
D. d├Ży c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł cß╗¦a ch├║ng c├│ c├╣ng sß╗æ lß╗øp electron, ─æŲ░ß╗Żc xß║┐p theo chiß╗üu sß╗æ neutron t─āng dß║¦n.
-
Giß║Żi b├Āi 5.3 trang 19 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Nh├│m nguy├¬n tß╗æ l├Ā
A tß║Łp hß╗Żp c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ cß║źu h├¼nh electron giß╗æng nhau, ─æŲ░ß╗Żc xß║┐p ß╗¤ c├╣ng mß╗Öt cß╗Öt.
B. tß║Łp hß╗Żp c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ cß║źu h├¼nh electron gß║¦n giß╗æng nhau, do ─æ├│ c├│ t├Łnh chß║źt h├│a hß╗Źc giß╗æng nhau v├Ā ─æŲ░ß╗Żc xß║┐p th├Ānh mß╗Öt cß╗Öt.
C. tß║Łp hß╗Żp c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ cß║źu h├¼nh electron tŲ░ŲĪng tß╗▒ nhau, do ─æ├│ c├│ t├Łnh chß║źt h├│a hß╗Źc gß║¦n giß╗æng nhau v├Ā ─æŲ░ß╗Żc xß║┐p th├Ānh mß╗Öt cß╗Öt.
D. tß║Łp hß╗Żp c├Īc nguy├¬n tß╗æ m├Ā nguy├¬n tß╗Ł c├│ t├Łnh chß║źt h├│a hß╗Źc giß╗æng nhau v├Ā ─æŲ░ß╗Żc xß║┐p c├╣ng mß╗Öt cß╗Öt.
-
Giß║Żi b├Āi 5.4 trang 20 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Trong bß║Żng tuß║¦n ho├Ān, c├Īc nguy├¬n tß╗æ ─æŲ░ß╗Żc sß║»p xß║┐p kh├┤ng theo nguy├¬n tß║»c n├Āo?
A. Theo chiß╗üu t─āng cß╗¦a ─æiß╗ćn t├Łch hß║Īt nh├ón.
B. C├Īc nguy├¬n tß╗æ c├│ c├╣ng sß╗æ lß╗øp electron trong nguy├¬n tß╗Ł ─æŲ░ß╗Żc xß║┐p th├Ānh mß╗Öt h├Āng.
C. C├Īc nguy├¬n tß╗æ c├│ c├╣ng sß╗æ electron ho├Ī trß╗ŗ trong nguy├¬n tß╗Ł ─æŲ░ß╗Żc xß║┐p th├Ānh mß╗Öt cß╗Öt.
D. Theo chiß╗üu t─āng khß╗æi lŲ░ß╗Żng nguy├¬n tß╗Ł.
-
Giß║Żi b├Āi 5.5 trang 20 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Sulfur dß║Īng kem b├┤i ─æŲ░ß╗Żc sß╗Ł dß╗źng ─æß╗ā ─æiß╗üu trß╗ŗ mß╗źn trß╗®ng c├Ī. Nguy├¬n tß╗Ł sulfur c├│ ph├ón lß╗øp electron ngo├Āi c├╣ng l├Ā 3p4. Ph├Īt biß╗āu n├Āo sau ─æ├óy l├Ā sai khi n├│i vß╗ü nguy├¬n tß╗Ł sulfur?
A. Lß╗øp ngo├Āi c├╣ng cß╗¦a sulfur c├│ 6 electron.
B. Hß║Īt nh├ón nguy├¬n tß╗Ł sulfur c├│ 16 electron.
C. Trong bß║Żng tuß║¦n ho├Ān sulfur nß║▒m ß╗¤ chu k├¼ 3.
D. Sulfur nß║▒m ß╗¤ nh├│m VIA.
-
Giß║Żi b├Āi 5.6 trang 20 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
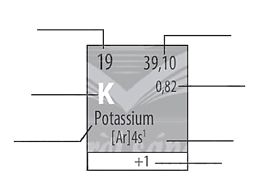
H├Ży cho biß║┐t ├Į ngh─®a cß╗¦a c├Īc th├┤ng tin c├│ trong ├┤ nguy├¬n tß╗æ sau:
-
Giß║Żi b├Āi 5.7 trang 20 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Sß╗Ł dß╗źng bß║Żng tuß║¦n ho├Ān c├Īc nguy├¬n tß╗æ h├│a hß╗Źc trong SGK (H├¼nh 5.2 trang 37), ho├Ān th├Ānh nhß╗»ng th├┤ng tin c├▓n thiß║┐u trong bß║Żng sau:
Hß╗Żp chß║źt
Khß╗æi lŲ░ß╗Żng Fe (g)
Khß╗æi lŲ░ß╗Żng O (g)
Tß╗ē lß╗ć khß╗æi lŲ░ß╗Żng
O : Fe
FeO
Fe2O3
Fe3O4
-
Giß║Żi b├Āi 5.8 trang 20 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
H├Ży giß║Żi th├Łch v├¼ sao chu k├¼ 3 chß╗ē c├│ 8 nguy├¬n tß╗æ.
-
Giß║Żi b├Āi 5.9 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
X├Īc ─æß╗ŗnh vß╗ŗ tr├Ł cß╗¦a nguy├¬n tß╗æ (├┤, chu k├¼ v├Ā nh├│m) cß╗¦a nguy├¬n tß╗æ c├│:
a. Sß╗æ hiß╗ću nguy├¬n tß╗Ł l├Ā 20, l├Ā nguy├¬n tß╗æ gi├║p xŲ░ŲĪng chß║»c khß╗Åe, ph├▓ng ngß╗½a nhß╗»ng bß╗ćnh lo├Żng xŲ░ŲĪng, giß║Żm t├¼nh trß║Īng ─æau nhß╗®c v├Ā kh├│ kh─ān trong vß║Łn ─æß╗Öng, l├Ām nhanh l├Ānh c├Īc vß║┐t nß╗®t g├Ży tr├¬n xŲ░ŲĪng.
b. 9 electron, ─æŲ░ß╗Żc sß╗Ł dß╗źng ─æß╗ā ─æiß╗üu chß║┐ mß╗Öt sß╗æ dß║½n xuß║źt hydrocarbon, l├Ām sß║Żn phß║®m trung gian ─æß╗ā sß║Żn xuß║źt ra chß║źt dß║╗o.
c. 28 proton, ─æŲ░ß╗Żc d├╣ng trong viß╗ćc chß║┐ tß║Īo hß╗Żp kim chß╗æng ─ān m├▓n.
d. Sß╗æ khß╗æi l├Ā 52 v├Ā 28 neutron, d├╣ng chß║┐ tß║Īo th├®p kh├┤ng gß╗ē.
-
Giß║Żi b├Āi 5.10 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Viß║┐t cß║źu h├¼nh electron nguy├¬n tß╗Ł cß╗¦a c├Īc nguy├¬n tß╗æ v├Ā x├Īc ─æß╗ŗnh t├¬n nguy├¬n tß╗æ:
a) Chu k├¼ 3, nh├│m IIIA, ─æŲ░ß╗Żc d├╣ng trong ng├Ānh c├┤ng nghiß╗ćp chß║┐ tß║Īo, cß╗ź thß╗ā l├Ā tß║Īo ra c├Īc chi tiß║┐t cho xe ├┤ t├┤, xe tß║Żi, t├Āu hoß║Ż, t├Āu biß╗ān v├Ā cß║Ż m├Īy bay.
b) Chu k├¼ 4, nh├│m IB, ─æŲ░ß╗Żc sß╗Ł dß╗źng rß║źt nhiß╗üu trong sß║Żn xuß║źt c├Īc nguy├¬n liß╗ću nhŲ░ d├óy ─æiß╗ćn, que h├Ān, tay cß║¦m, c├Īc ─æß╗ō d├╣ng nß╗Öi thß║źt trong nh├Ā, c├Īc tŲ░ß╗Żng ─æ├║c, nam ch├óm ─æiß╗ćn tß╗½, c├Īc ─æß╗Öng cŲĪ m├Īy m├│c,ŌĆ”
-
Giß║Żi b├Āi 5.11 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Mß╗Öt hß╗Żp chß║źt c├│ c├┤ng thß╗®c XY2, trong ─æ├│ X chiß║┐m 50% vß╗ü khß╗æi lŲ░ß╗Żng. Trong hß║Īt nh├ón cß╗¦a X v├Ā Y ─æß╗üu c├│ sß╗æ proton bß║▒ng sß╗æ neutron. Tß╗Ģng sß╗æ proton trong ph├ón tß╗Ł XY2 l├Ā 32. Hß╗Żp chß║źt n├Āy ─æŲ░ß╗Żc sß╗Ł dß╗źng nhŲ░ chß║źt trung gian ─æß╗ā sß║Żn xuß║źt sulfuric acid.
a. Viß║┐t cß║źu h├¼nh electron cß╗¦a X v├Ā Y
b. X├Īc ─æß╗ŗnh vß╗ŗ tr├Ł cß╗¦a X v├Ā Y trong bß║Żng tuß║¦n ho├Ān v├Ā c├┤ng thß╗®c ph├ón tß╗Ł hß╗Żp chß║źt XY2.
-
Giß║Żi b├Āi 5.12 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
Hai nguy├¬n tß╗æ X v├Ā Y ─æß╗®ng kß║┐ tiß║┐p nhau trong c├╣ng mß╗Öt chu k├¼, c├│ tß╗Ģng sß╗æ ─æiß╗ćn t├Łch hß║Īt nh├ón bß║▒ng 25.
a. H├Ży viß║┐t cß║źu h├¼nh electron cß╗¦a nguy├¬n tß╗Ł X, Y.
b. X├Īc ─æß╗ŗnh vß╗ŗ tr├Ł cß╗¦a X, Y trong bß║Żng tuß║¦n ho├Ān v├Ā t├¬n nguy├¬n tß╗æ X, Y.
-
Giß║Żi b├Āi 5.13 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
X, Y l├Ā hai nguy├¬n tß╗æ thuß╗Öc c├╣ng nh├│m A ß╗¤ hai chu k├¼ li├¬n tiß║┐p trong bß║Żng tuß║¦n ho├Ān, c├│ tß╗Ģng sß╗æ proton trong hai hß║Īt nh├ón l├Ā 32. Viß║┐t cß║źu h├¼nh electron cß╗¦a nguy├¬n tß╗Ł X v├Ā Y. X├Īc ─æß╗ŗnh t├¬n X, Y
-
Giß║Żi b├Āi 5.14 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
X v├Ā Y l├Ā hai nguy├¬n tß╗æ thuß╗Öc chu k├¼ nhß╗Å, thuß╗Öc hai nh├│m A kß║┐ tiß║┐p nhau trong bß║Żng tuß║¦n ho├Ān. ß╗× trß║Īng th├Īi ─æŲĪn chß║źt, X v├Ā Y phß║Żn ß╗®ng ─æŲ░ß╗Żc vß╗øi nhau. Tß╗Ģng sß╗æ proton trong hß║Īt nh├ón nguy├¬n tß╗Ł cß╗¦a X v├Ā Y l├Ā 23. Biß║┐t rß║▒ng X ─æß╗®ng sau Y trong bß║Żng tuß║¦n ho├Ān. X├Īc ─æß╗ŗnh t├¬n nguy├¬n tß╗æ X, Y.
-
Giß║Żi b├Āi 5.15 trang 21 SBT H├│a hß╗Źc 10 Ch├ón trß╗Øi s├Īng tß║Īo - CTST
H├▓a tan ho├Ān to├Ān 6,645 gam hß╗Śn hß╗Żp muß╗æi chloride cß╗¦a hai kim loß║Īi kiß╗üm thuß╗Öc hai chu k├¼ kß║┐ tiß║┐p nhau v├Āo nŲ░ß╗øc ─æŲ░ß╗Żc dung dß╗ŗch X. Cho to├Ān bß╗Ö dung dß╗ŗch X t├Īc dß╗źng ho├Ān to├Ān vß╗øi dung dß╗ŗch AgNO3 (dŲ░), thu ─æŲ░ß╗Żc 18,655 gam kß║┐t tß╗¦a. X├Īc ─æß╗ŗnh 2 kim loß║Īi kiß╗üm.