Đề thi HK2 môn Hóa 12 năm 2019 - Trường THPT Chuyên Quang Trung (có đáp án chi tiết) dưới đây được HOC247 biên soạn nhằm giúp các em tự luyện tập với các câu hỏi lý thuyết đa dạng, ôn tập lại các kiến thức cần nắm một cách hiệu quả, chuẩn bị thật tốt cho các kỳ thi sắp tới. Mời các em cùng tham khảo.
|
SỞ GD VÀ ĐT BÌNH PHƯỚC TRƯỜNG THPT CHUYÊN QUANG TRUNG |
ĐỀ THI HỌC KÌ 2 LỚP 12 NĂM 2019 MÔN HÓA HỌC 9 Thời gian: 50 phút |
Câu 1: Kim loại nào sau đây là kim loại kiềm thổ?
A. Na. B. Ca. C. Al. D. Fe.
Câu 2: Cấu hình electron lớp ngoài cùng của nguyên tử kim loại kiềm là
A. ns1. B. ns2. C. ns2np1. D. (n – 1)dxnsy.
Câu 3: Cách bảo quản thực phẩm (thịt, cá,…) bằng cách nào sau đây được coi là an toàn?
A. Dùng fomon và phân đạm. B. Dùng phân đạm và nước đá khô.
C. Dùng nước đá và nước đá khô. D. Dùng fomon và nước đá khô.
Câu 4: Isoamyl axetat là este có mùi chuối chín. Công thức phân tử este đó là
A. C4H8O2. B. C5H10O2. C. C7H14O2. D. C6H12O2.
Câu 5: Cho từ từ dung dịch NaOH vào dung dịch X, thu được kết tủa keo trắng tan trong dung dịch NaOH dư. Chất X là
A. FeCl3. B. KCl. C. AlCl3. D. MgCl2.
Câu 6: Dung dịch Gly-Ala phản ứng được với dung dịch nào sau đây?
A. NaCl. B. NaNO3. C. Na2SO4. D. NaOH.
Câu 7: Nguyên liệu chính dùng để sản xuất nhôm là
A. quặng manhetit. B. quặng boxit. C. quặng đolomit. D. quặng pirit.
Câu 8: Oxit nào sau đây là oxit lưỡng tính?
A. CrO. B. Cr2O3. C. FeO. D. MgO.
Câu 9: Poli(vinyl clorua) điều chế từ vinyl clorua bằng phản ứng
A. trao đổi. B. oxi hoá - khử. C. trùng hợp. D. trùng ngưng.
Câu 10: Trước đây, người ta thường dùng những tấm gương soi bằng Cu vì Cu là kim loại
A. có tính dẻo. B. có tính dẫn nhiệt tốt.
C. có khả năng phản xạ tốt ánh sáng. D. có tính khử yếu.
Câu 11: Trong các phản ứng sau, phản ứng nào không chứng minh được glucozơ chứa nhóm chức anđehit?
A. Oxi hoá glucozơ bằng AgNO3/NH3. B. Oxi hoà glucozơ bằng Cu(OH)2 đun nóng.
C. Lên men glucozơ bằng xúc tác enzim. D. Khử glucozơ bằng H2/Ni, t0.
Câu 12: Chất X là một bazơ mạnh, X được sử dụng để sản xuất clorua vôi. Chất X là
A. KOH. B. NaOH. C. Ba(OH)2. D. Ca(OH)2.
Câu 13: Thêm dung dịch NaOH dư vào dung dịch chứa 0,3 mol Fe(NO3)3. Lọc kết tủa, đem nung đến khối lượng không đổi thì khối lượng chất rắn thu được là
A. 24,0 gam. B. 96,0 gam. C. 32,1 gam. D. 48,0 gam.
Định hướng tư duy giải
m = 0,3 : 2.160 = 24 gam
Câu 14: Sục 8,96 lit khí CO2 (đktc) vào dung dịch chứa 0,25 mol Ca(OH)2. Khối lượng kết tủa thu được là
A. 25 gam. B. 10 gam. C. 12 gam. D. 40 gam.
Định hướng tư duy giải
m = (0,25.2 - 0,4) = 10 gam
Câu 15: Cho dãy các chất: HCHO, CH3COOH, CH3COOC2H5, HCOOH, C2H5OH, HCOOCH3. Số chất trong dãy tham gia phản ứng tráng gương là
A. 3. B. 2. C. 4. D. 5.
Câu 16: Lên men glucozơ thành ancol etylic. Toàn bộ khí CO2 sinh ra trong quá trình này được hấp thụ hết vào dung dịch Ca(OH)2 dư tạo ra 50 gam kết tủa, biết hiệu suất quá trình lên men đạt 80%. Khối lượng glucozơ cần dùng là
A. 33,7 gam. B. 56,25 gam. C. 20 gam. D. 90 gam.
Định hướng tư duy giải
m = 50 : 100 : 0,8 : 2.180 = 56,25 gam
Câu 17: Cho 9,85 gam hỗn hợp 2 amin đơn chức, bậc một tác dụng vừa đủ với dung dịch HCl thu được 18,975 g muối. Khối lượng của HCl cần dùng là
A. 9,521g. B. 9,125g. C. 9,215g. D. 9,512g.
Định hướng tư duy giải
mHCl = 18,975 - 9,85
Câu 18: Có 4 ống nghiệm chứa Cu(OH)2. Thêm vào các ống nghiệm lượng dư của 4 dung dịch etan-1,2điol, propan-1,3-điol, propan-1,2-điol,propan-1,2,3-triol. Hiện tượng xảy ra như hình sau:
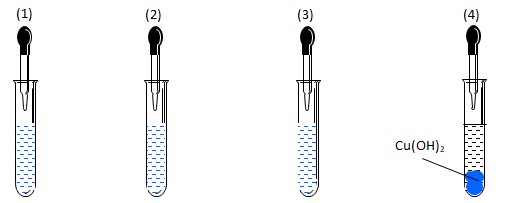
Dung dịch cho vào ống nghiệm 4 là
A. propan-1,3-điol. B. propan-1,2-điol. C. etan-1,2-điol. D. propan-1,2,3-triol.
Câu 19: Cho các phản ứng hóa học sau:
(1) (NH4)2SO4 + Ba(NO3)2 → (2) CuSO4 + Ba(NO3)2 →
(3) Na2SO4 + BaCl2 → (4) H2SO4 + BaCO3 →
(5) (NH4)2SO4 + Ba(OH)2 → (6) Fe2(SO4)3 + BaCl2 →
Các phản ứng đều có cùng một phương trình ion rút gọn là
A. (1), (2), (3), (6). B. (1), (3), (5), (6). C. (2), (3), (4), (6). D. (3), (4), (5), (6).
Câu 20: Thủy phân hoàn toàn đisaccarit A thu được hai monosaccarit X và Y. Hiđro hóa X hoặc Y đều thu được chất hữu cơ Z. A và Z lần lượt là
A. tinh bột và glucozơ. B. saccarozơ và sobitol.
C. saccarozơ và glucozơ. D. glucozơ và axit gluconic.
Câu 21: Trong các trường hợp sau, trường hợp nào không xảy ra ăn mòn điện hoá?
A. Nhúng thanh Cu trong dung dịch Fe2(SO4)3 có nhỏ một vài giọt dung dịch H2SO4.
B. Sự ăn mòn vỏ tàu trong nước biển.
C. Nhúng thanh Zn trong dung dịch H2SO4 có nhỏ vài giọt dung dịchCuSO4.
D. Sự gỉ của gang, thép trong tự nhiên.
Câu 22: Hợp chất thơm A có công thức phân tử C8H8O2 khi xà phòng hóa thu được 2 muối. Số đồng phân cấu tạo phù hợp của A là
A. 5. B. 3. C. 2. D. 4.
Câu 23: So sánh nào sau đây không đúng?
A. Fe(OH)2 và Cr(OH)2 đều là bazơ, là chất khử và kém bền nhiệt.
B. Al(OH)3 và Cr(OH)3 đều là hiđroxit lưỡng tính và có tính khử.
C. Al và Cr đều phản ứng với dung dịch HCl không theo cùng tỉ lệ số mol.
D. BaSO4 và BaCrO4 đều là muối trung hòa không tan trong nước.
Câu 24: Hai hợp chất hữu cơ X, Y có cùng công thức phân tử C3H6O2. Cả X và Y đều tác dụng với Na; X tác dụng được với NaHCO3, Y có khả năng tham gia phản ứng tráng bạc. Công thức của X và Y lần lượt là
A. C2H5COOH và HCOOC2H5. C. HCOOC2H5 và HOCH2CH2CHO.
B. HCOOC2H5 và HOCH2COCH3. D. C2H5COOH và CH3CH(OH)CHO.
Câu 25: Cho thêm m gam kali vào 300ml dung dịch chứa Ba(OH)2 0,1M và NaOH 0,1M thu được dung dịch X. Cho từ từ dung dịch X vào 200ml dung dịch Al2(SO4)3 0,1M thu được kết tủa Y. Để thu được lượng kết tủa Y lớn nhất thì giá trị của m là
A. 1,170. B. 1,248. C. 1,950. D. 1,560.
Định hướng tư duy giải
\({n_K} = {x^{mol}} \to {n_{ \downarrow \max }} = \frac{{0,03 + 0,03.2 + x}}{3} \to x = 0,04 \to m = 1,17{\rm{ gam}}\)
Câu 26: Khi xà phòng hoá 5,45 gam X có công thức phân tử C9H14O6 đã dùng 100 ml dung dịch NaOH 1M thu được ancol no Y và muối của một axit hữu cơ. Để trung hoà lượng NaOH dư sau phản ứng phải dùng hết 50 ml dung dịch HCl 0,5 M. Biết rằng 23 gam ancol Y khi hoá hơi có thể tích bằng thể tích của 8 gam O2 (trong cùng điều kiện). Công thức của X là
A. (C2H5COO)2C3H5(OH). B. (HCOO)3C6H11.
C. C2H5COOC2H4COOC2H4COOH. D. (CH3COO)3C3H5.
Định hướng tư duy giải
\({M_Y} = 92 \to \left\{ \begin{array}{l}
Y:{C_3}{H_5}{(OH)_3}\\
{n_{NaOHpu}} = 0,{075^{mol}}
\end{array} \right. \to X:{(C{H_3}COO)_3}{C_3}{H_5}\)
Câu 27: Cho sơ đồ các phản ứng sau:
X + NaOH (dư) → Y + Z + H2O. Y + HCl (dư ) → T + NaCl.
Z + CuO CH2O + Cu + H2O.
Biết Y là muối Na của axit glutamic. Công thức phân tử của X và T lần lượt là
A. C6H11O4N và C5H10O4NCl. B. C7H13O4N và C5H10O4NCl.
C. C6H11O4N và C5H9O4N. D. C7H13O4N và C5H9O4N.
Câu 28: Thực hiện các thí nghiệm sau:
(1) Cu vào dung dịch Fe2(SO4)3.
(2) Sục khí CO2 vào dung dịch Ca(OH)2.
(3) Sục hỗn hợp khí NO2 và O2 vào nước.
(4) Cho MnO2 vào dung dịch HCl đặc, nóng.
(5) Cho FeO vào dung dịch H2SO4 đặc, nóng.
(6) Cho Fe3O4 vào dung dịch HCl.
Số thí nghiệm có xảy ra phản ứng oxi hoá - khử là
A. 3. B. 2. C. 5. D. 4.
Câu 29: Tiến hành các thí nghiệm sau:
(1) Sục khí H2S vào dung dịch FeSO4.
(2) Sục khí H2S vào dung dịch Pb(NO3)2.
(3) Sục khí CO2 vào dung dịch NaAlO2.
(4) Sục khí CO2 dư vào dung dịch Ca(OH)2.
(5) Sục khí NH3 dư vào dung dịch Al2(SO4)3.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được kết tủa là
A. 2. B. 5. C. 3. D. 4.
Câu 30: Thực hiện phản ứng crackinh hoàn toàn m gam isobutan, thu được hỗn hợp A gồm hai hiđrocacbon. Cho hỗn hợp A qua dung dịch nước brom có hòa tan 11,2 gam brom. Brom bị mất màu hoàn toàn đồng thời có 2,912 lít khí (ở đktc) thoát ra khỏi bình brom, tỉ khối hơi của khí so với CO2 bằng
0,5. Giá trị của m là
A. 5,22. B. 6,96. C. 5,80. D. 4,64.
Định hướng tư duy giải
m = 0,07.42 + 0,13.44.0,5 = 5,8 gam
...
Trên đây là phần trích dẫn Đề thi HK2 môn Hóa 12 năm 2019 - Trường THPT Chuyên Quang Trung (có đáp án chi tiết), để xem toàn bộ nội dung chi tiết, mời các bạn cùng quý thầy cô vui lòng đăng nhập để tải về máy.
Chúc các em đạt điểm số thật cao trong kì thi sắp đến!






