Giải bài 7.5 trang 24 SBT Hóa học 10 Chân trời sáng tạo
Phosphorus được dùng vào mục đích quân sự như sản xuất bom, đạn cháy, đạn khói. Nguyên tố phosphorus ở ô số 15, chu kì 3, nhóm VA trong bảng tuần hoàn. Hãy cho biết:
- Cấu hình electron của phosphorus.
- Số electron lớp ngoài cùng của nguyên tử phosphorus
- Phosphorus là kim loại hay phi kim.
- Công thức oxide cao nhất của phosphorus.
- Công thức hợp chất khí của phosphorus với hydrogen.
- Công thức hydroxide cao nhất của phosphorus.
- Oxide và hydroxide cao nhất của phosphorus có tính acid hay base.
Hướng dẫn giải chi tiết bài 7.5
Phương pháp giải:
- Khi có cấu hình electron lớp ngoài cùng của nguyên tử
+ TH1: các lớp trước đó đã được lấp đầy electron
+ TH2: trước lớp ngoài cùng vẫn có lớp chưa được lấp đầy electron (do có phân lớp d hoặc phân lớp f). Áp dụng với nguyên tử có cấu hình electron lớp ngoài cùng từ 4s trở lên
- Từ cấu hình electron của nguyên tử
+ Số lớp electron = số chu kì
+ Số electron lớp ngoài cùng = số nhóm (đối với các nguyên tố nhóm A)
+ Ô số thứ tự = điện tích hạt nhân = số proton = số electron
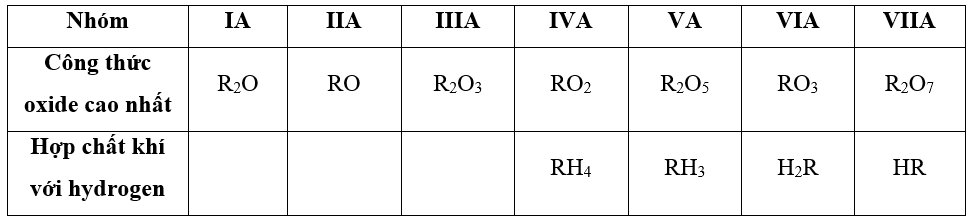
- Công thức oxide cao nhất và hợp chất khí với hydrogen của các nguyên tố từ IA đến VIIA
Lời giải chi tiết:
- Cấu hình electron của phosphorus: 1s22s22p63s23p3.
- Số electron lớp ngoài cùng của nguyên tử phosphorus: 5.
- Phosphorus là phi kim.
- Công thức oxide cao nhất của phosphorus: P2O5.
- Công thức hợp chất khí của phosphorus với hydrogen: PH3.
- Công thức hydroxide cao nhất của phosphorus: H3PO4.
- Oxide và hydroxide cao nhất của phosphorus có tính acid.
-- Mod Hóa Học 10 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.
Bài tập SGK khác
Giải bài 7.3 trang 24 SBT Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 7.4 trang 24 SBT Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 7.6 trang 25 SBT Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 7.7 trang 25 SBT Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 7.8 trang 25 SBT Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 7.9 trang 25 SBT Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 7.10 trang 25 SBT Hóa học 10 Chân trời sáng tạo - CTST




