Giải bài 7.8 trang 25 SBT Hóa học 10 Chân trời sáng tạo
Oxide cao nhất của nguyên tố R thuộc nhóm VIA có 60% oxygen về khối lượng, là một sản phẩm trung gian để sản xuất acid H2SO4 có tầm quan trọng bậc nhất trong công nghiệp. Hãy xác định nguyên tố R và viết công thức oxide cao nhất của nguyên tố R.
Hướng dẫn giải chi tiết bài 7.8
Phương pháp giải:
- Công thức oxide cao nhất và hợp chất khí với hydrogen của các nguyên tố từ IA đến VIIA
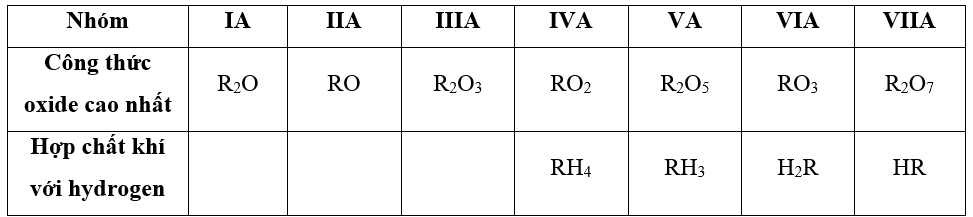
- Công thức thành phần phần trăm khối lượng của một nguyên tố trong hợp chất XaYb:
\(\% {m_X} = \frac{{a.{A_X}}}{{{A_{{X_a}{Y_b}}}}}.100\% = \frac{{a.{A_X}}}{{a.{A_X} + b.{A_Y}}}.100\% \)
Lời giải chi tiết:
Nguyên tố R thuộc nhóm VIA nên oxide cao nhất có dạng RO3.
Ta có:
\(\frac{{\% R}}{{\% O}} = \frac{R}{{16.3}} = \frac{{100 - 60}}{{60}} \Rightarrow R = 32.\)
Vậy R là sulfur (S), công thức oxide cao nhất là SO3.
-- Mod Hóa Học 10 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.





