Giải bài 15.2 trang 44 SBT Hóa học 10 Cánh Diều
Đường sucrose (C12H22O11) là một đường đôi. Trong môi trường acid ở dạ dày và nhiệt độ cơ thể, sucrose bị thủy phân thành đường glucose và fructose, sau đó bị oxi hóa bởi oxygen tạo thành CO2 và H2O. Sơ đồ thay đổi năng lượng hóa học của phản ứng được cho như hình dưới đây:
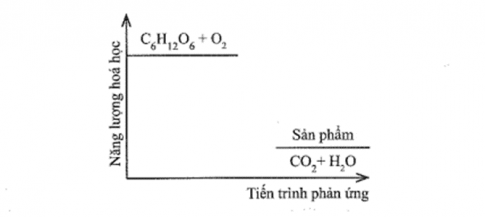
a) Dựa theo đồ thị, hãy cho biết phản ứng trong đó là tỏa nhiệt hay thu nhiệt. Vì sao?
b) Viết phương trình hoá học của phản ứng thuỷ phân đường sucrose. Phản ứng trong sơ đồ có phải là phản ứng oxi hoá - khử không? Nếu có, hãy chỉ ra chất oxi hoá và chất khử trong phản ứng và cân bằng phương trình hoá học của phản ứng theo phương pháp thăng bằng electron.
c) Khi 1 mol đường sucrose bị đốt cháy hoàn toàn với một lượng vừa đủ oxygen ở điều kiện chuẩn toả ra một lượng nhiệt là 5645 kJ. Xác định biến thiên enthalpy chuẩn của phản ứng oxi hoá sucrose.
d) Nếu 5,00 gam đường sucrose được đốt cháy hoàn toàn ở cùng điều kiện như trên thì biến thiên enthalpy quá trình bằng bao nhiêu?
e) Vì sao để duy trì một cơ thể khoẻ mạnh, cần một chế độ dinh dưỡng đầy đủ và luyện tập thể dục thể thao hợp lí?
Lời giải chi tiết:
Hướng dẫn giải chi tiết bài 15.2
Phương pháp giải:
- Dựa vào đồ thị: Biến thiên enthalpy âm → phản ứng tỏa nhiệt
- Phản ứng oxi hoá - khử có sự thay đổi số oxi hoá, tức là có các quá trình nhường và nhận electron. Ta có thể cân bằng các phản ứng oxi hoá - khử theo nguyên tắc trong một phản ứng, tổng số electron nhường phải bằng tổng số electron nhận.
Lời giải chi tiết:
a) Năng lượng của sản phẩm < năng lượng chất tham gia → Biến thiên enthalpy âm → Phản ứng tỏa nhiệt
b) - Phản ứng thủy phân đường sucrose trong môi trường acid và đun nóng:
C12H22O11 + H2O → C6H12O6 (glucose) + C6H12O6 (fructose)
- Phản ứng trong sơ đồ là phản ứng oxi hóa - khử với O2 là chất oxi hóa, đường glucose và fructose là chất khử:
+ Bước 1: \(\overset{0}{\mathop{{{C}_{6}}}}\,{{H}_{12}}{{O}_{6}}+\overset{0}{\mathop{{{O}_{2}}}}\,\xrightarrow{{{t}^{o}}}\overset{+4}{\mathop{C}}\,\overset{-2}{\mathop{{{O}_{2}}}}\,+{{H}_{2}}O\)
→ C6H12O6 là chất khử, O2 là chất oxi hóa
+ Bước 2:
+ Quá trình oxi hóa: \(6\overset{0}{\mathop{C}}\,\to 6\overset{+4}{\mathop{C}}\,+6.4e\)
+ Quá trình khử: \(\overset{0}{\mathop{{{O}_{2}}}}\,+4e\to 2\overset{-2}{\mathop{{{O}_{2}}}}\,\)
- Bước 3:
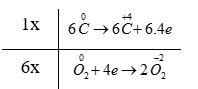
- Bước 4: C6H12O6 + 6O2 \(\xrightarrow{{{t}^{o}}}\) 6CO2 + 6H2O
c) - Phản ứng đốt cháy đường sucrose: C12H22O11 + 12O2 \(\xrightarrow{{{t}^{o}}}\) 12CO2 + 11H2O
- Phản ứng tỏa nhiệt → \({{\Delta }_{r}}H_{298}^{0}=-5645kJ\)
d) Nếu 5,00 gam đường sucrose được đốt cháy hoàn toàn ở cùng điều kiện như trên thì biến thiên enthalpy quá trình bằng: \(\frac{5}{{342}}.( - 5645) = - 82,5kJ\)
e) - Cơ thể cần năng lượng để hoạt động nên phải có chế độ dinh dưỡng đầy đủ.
- Luyện tập thể dục, thể thao hợp lý giúp tăng cường sức khỏe và đốt cháy năng lượng dư thừa trong cơ thể
-- Mod Hóa Học 10 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.
Bài tập SGK khác
Giải bài 3 trang 87 SGK Hóa học 10 Cánh Diều - CD
Giải bài 15.1 trang 44 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.3 trang 45 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.4 trang 45 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.5 trang 46 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.6 trang 46 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.7 trang 46 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.8 trang 47 SBT Hóa học 10 Cánh Diều - CD
Giải bài 15.9 trang 47 SBT Hóa học 10 Cánh Diều - CD




