DŲ░ß╗øi ─æ├óy l├Ā HŲ░ß╗øng dß║½n giß║Żi H├│a 11 SGK n├óng cao ChŲ░ŲĪng 9 B├Āi 61 Axit cacboxylic - T├Łnh chß║źt h├│a hß╗Źc, ─æiß╗üu chß║┐ v├Ā ß╗®ng dß╗źng ─æŲ░ß╗Żc hoc247 bi├¬n soß║Īn v├Ā tß╗Ģng hß╗Żp, nß╗Öi dung b├Īm s├Īt theo chŲ░ŲĪng tr├¼nh SGK H├│a hß╗Źc 11 n├óng cao gi├║p c├Īc em hß╗Źc sinh nß║»m vß╗»ng phŲ░ŲĪng ph├Īp giß║Żi b├Āi tß║Łp v├Ā ├┤n tß║Łp kiß║┐n thß╗®c hiß╗ću quß║Ż hŲĪn.
B├Āi 1 trang 256 SGK H├│a 11 n├óng cao
B├Āi 2 trang 256 SGK H├│a 11 n├óng cao
B├Āi 3 trang 256 SGK H├│a 11 n├óng cao
B├Āi 4 trang 256 SGK H├│a 11 n├óng cao
B├Āi 5 trang 257 SGK H├│a 11 n├óng cao
B├Āi 6 trang 257 SGK H├│a 11 n├óng cao
B├Āi 7 trang 257 SGK H├│a 11 n├óng cao
B├Āi 1 trang 256 SGK H├│a 11 n├óng cao
Viß║┐t phŲ░ŲĪng tr├¼nh ho├Ī hß╗Źc cß╗¦a c├Īc phß║Żn ß╗®ng ─æß╗ā minh hoß║Ī:
a) Axit axetic c├│ ─æß║¦y ─æß╗¦ t├Łnh chß║źt cß╗¦a mß╗Öt axit.
b) Axit axetic l├Ā mß╗Öt axit yß║┐u nhŲ░ng vß║½n mß║Īnh hŲĪn axit cacbonic, c├▓n phenol l├Ā mß╗Öt axit yß║┐u hŲĪn axit cacbonic.
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
CH3COOH c├│ t├Łnh chß║źt ─æß║¦y ─æß╗¦ cß╗¦a mß╗Öt axit.
CH3COOH + H2O Ōćö CH3COO- + H3O+. L├Ām quß╗│ t├Łm h├│a ─æß╗Å.
2CH3COOH + 2Na ŌåÆ 2CH3COONa + H2
CH3COOH + NaOH ŌåÆ CH3COONa + H2O
2CH3-COOH + CaO ŌåÆ (CH3COO)2Ca + H2O
2CH3COOH + CaCO3 ŌåÆ (CH3COO)2Ca + CO2 + H2O
Câu b:
2CH3-COOH + Na2CO3 ŌåÆ 2CH3-COONa + CO2 + H2O
C6H5ONa + CO2 + H2O ŌåÆ C6H5OH + NaHCO3
B├Āi 2 trang 256 SGK H├│a 11 n├óng cao
H├Ży ─æiß╗ün chß╗» ─É (─æ├║ng) hoß║Ęc chß╗» S (sai) v├Āo c├Īc dß║źu [... ] ß╗¤ mß╗Śi c├óu sau:
a) Giß║źm ─ān l├Ām ─æß╗Å quß╗│ t├Łm. [... ]
b) NŲ░ß╗øc ├®p tß╗½ quß║Ż chanh kh├┤ng ho├Ā tan ─æŲ░ß╗Żc CaCO3. [ ...]
c) D├╣ng axit axetic tß║®y sß║Īch ─æŲ░ß╗Żc cß║Ęn b├Īm ß╗¤ trong ph├Łch nŲ░ß╗øc n├│ng. [ ...]
d) Phß║Żn ß╗®ng cß╗¦a axit axetic vß╗øi etanol l├Ā phß║Żn ß╗®ng trung ho├Ā. [ ...]
HŲ░ß╗øng dß║½n giß║Żi:
a) ─É
b) S
c) ─É
d) S
B├Āi 3 trang 256 SGK H├│a 11 n├óng cao
H├Ży sß║»p xß║┐p c├Īc axit trong c├Īc d├Ży sau theo thß╗® tß╗▒ t─āng dß║¦n lß╗▒c axit:
a) CH3 COOH,Cl3CCOOH,Cl2CHCOOH,ClCH2COOH
b) ClCH2CH2COOH,CH3 CH(Cl)CH2COOH,CH3 CH2CH(Cl)COOH,CH3CH2CH2COOH
HŲ░ß╗øng dß║½n giß║Żi:
Hß╗Źc sinh xem phß║¦n kiß║┐n thß╗®c bß╗Ģ sung chŲ░ŲĪng IX.
Lß╗▒c axit theo thß╗® tß╗▒ t─āng dß║¦n tr├Īi tß╗½ qua phß║Żi.
Câu a:
CH3COOH < ClCH2-COOH < Cl2CH-COOH < Cl3C-COOH
Câu b:
CH3(CH2)2COOH < Cl(CH2)3COOH < CH3CHClCOOH < CH3CH2CHClCOOH
B├Āi 4 trang 256 SGK H├│a 11 n├óng cao
Hai b├¼nh nhŲ░ nhau, b├¼nh A chß╗®a 0,50 l├Łt axit clohi─æric 2M, b├¼nh B chß╗®a 0,50 l├Łt axit axetic 2,0M ─æŲ░ß╗Żc bß╗ŗt k├Łn bß╗¤i 2 b├│ng cao su nhŲ░ nhau. Hai mß║®u Mg khß╗æi lŲ░ß╗Żng nhŲ░ nhau ─æŲ░ß╗Żc thß║Ż xuß╗æng c├╣ng mß╗Öt l├║c. Kß║┐t quß║Ż sau 1 ph├║t v├Ā sau 10 ph├║t (phß║Żn ß╗®ng ─æ├Ż kß║┐t th├║c) ─æŲ░ß╗Żc thß╗ā hiß╗ćn nhŲ░ ß╗¤ h├¼nh dŲ░ß╗øi ─æ├óy. H├Ży nhß║Łn x├®t v├Ā giß║Żi th├Łch.
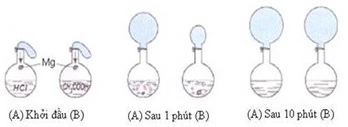
HŲ░ß╗øng dß║½n giß║Żi:
Mg + 2HCl ŌåÆ MgCl2 + H2
Mg + 2CH3COOH ŌåÆ (CH3COO)2Mg + H2
nCH3COOH = nHCl = 0,5.2 = 1 mol
HCl l├Ā chß║źt ─æiß╗ćn li mß║Īnh n├¬n ph├ón li ho├Ān to├Ān ŌćÆ nß╗ōng ─æß╗Ö H+ lß╗øn ŌćÆ H2 tho├Īt ra mß║Īnh hŲĪn. CH3COOH l├Ā chß║źt ─æiß╗ćn li yß║┐u ŌćÆ nß╗ōng ─æß╗Ö H+ nhß╗Å ŌćÆ H2 tho├Īt ra yß║┐u hŲĪn.
Sau 1 ph├║t thß║źy kh├Ł H2 ß╗¤ HCl nhiß╗üu hŲĪn so vß╗øi CH3COOH (Mg phß║Żn ß╗®ng vß╗øi HCl nhanh hŲĪn CH3COOH). Sau phß║Żn ß╗®ng kß║┐t th├║c 10 ph├║t kh├Ł H2 bay ra ß╗¤ 2 b├¼nh nhŲ░ nhau v├¼ nH2 = 0,5 mol (bß║▒ng nhau).
B├Āi 5 trang 257 SGK H├│a 11 n├óng cao
Viß║┐t phŲ░ŲĪng tr├¼nh ho├Ī hß╗Źc cß╗¦a phß║Żn ß╗®ng khi cho axit acrylic t├Īc dß╗źng lß║¦n lŲ░ß╗Żt vß╗øi c├Īc chß║źt sau:
a) C6H5ONa
b) NaHCO3
c) H2 (Ni,to)
d) Br2/CCl4
e) P2O5
g) tr├╣ng hß╗Żp
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
CH2=CH-COOH + C6H5ONa ŌåÆ CH2=CH-COONa + C6H5OH
Câu b:
CH2=CH-COOH + NaHCO3 ŌåÆ CH2=CH-COONa + CO2 + H2O
Câu c:
CH2=CH-COOH + H2 ŌåÆ CH3-CH2-COOH (xt: Ni, to)
Câu d:
CH2=CH-COOH + Br2 ŌåÆ CH2Br- CHBr-COOH (xt: CCl4)
Câu e:
CH2=CH-COOH ŌåÆ (CH2=CH-CO)2O + H2O (xt: P2O5)
B├Āi 6 trang 257 SGK H├│a 11 n├óng cao
Ho├Ān th├Ānh c├Īc sŲĪ ─æß╗ō phß║Żn ß╗®ng sau (c├Īc chß╗» c├Īi chß╗ē sß║Żn phß║®m hß╗»u cŲĪ ch├Łnh):
.png)
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
CH3CHO + HCN ŌåÆ CH3CH(CN)OH
CH3CH(CN)OH + 2H2O ŌåÆ CH3CH(OH)COOH + NH3
Câu b:
CH3CH2Br + Mg ŌåÆ CH3CH2-Mg-Br
CH3CH2-Mg-Br + CO2 ŌåÆ CH3CH2COO-Mg-Br
CH3CH2COO-Mg-Br + HCl ŌåÆ CH3CH2COOH + MgClBr
Câu c:
.png)
B├Āi 7 trang 257 SGK H├│a 11 n├óng cao
H├Ży ph├ón biß╗ćt c├Īc chß║źt trong c├Īc nh├│m sau:
a) Etanol, fomalin, axeton, axit axetic.
b) Phenol, p ŌĆō nitrobenzan─æehit, axit benzoic.
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
D├╣ng quß╗│ t├Łm nhß║Ł biß║┐t ─æŲ░ß╗Żc axit axetic v├¼ quß╗│ t├Łm h├│a ─æß╗Å.
D├╣ng phß║Żn ß╗®ng tr├Īng gŲ░ŲĪng nhß║Łn biß║┐t ─æŲ░ß╗Żc fomalin v├¼ tß║Īo kß║┐t tß╗¦a Ag.
HCHO + 4[Ag(NH3)2](OH) ŌåÆ (NH4)2CO3 + 4Ag + 6NH3 + 2H2O
D├╣ng Na nhß║Łn biß║┐t ─æŲ░ß╗Żc C2H5OH v├¼ sß╗¦i bß╗Źt kh├Ł H2. Mß║½u c├▓n lß║Īi l├Ā axeton.
Câu b:
D├╣ng quß╗│ t├Łm nhß║Łn biß║┐t ─æŲ░ß╗Żc axit bezoic v├¼ l├Ām quß╗│ t├Łm h├│a ─æß╗Å.
D├╣ng phß║Żn ß╗®ng tr├Īng gŲ░ŲĪng nhß║Łn biß║┐t ─æŲ░ß╗Żc p ŌĆō nitrobenzen─æehit v├¼ tß║Īo ra kß║┐t tß╗¦a Ag. Mß║½u c├▓n lß║Īi l├Ā phenol.
p-NO2-C4H6CHO + 2[Ag(NH3)2]OH ŌåÆ P-NO2-C4H6COONH4 + 2Ag + 3NH3 + H2O
B├Āi 8 trang 257 SGK H├│a 11 n├óng cao
─Éß╗ā trung ho├Ā 40,0ml giß║źm cß║¦n d├╣ng 25,0ml dung dß╗ŗch NaOH 1,00M. Coi khß╗æi lŲ░ß╗Żng ri├¬ng cß╗¦a giß║źm kh├┤ng kh├Īc khß╗æi lŲ░ß╗Żng ri├¬ng cß╗¦a nŲ░ß╗øc. H├Ży t├Łnh nß╗ōng ─æß╗Ö % cß╗¦a axit axetic trong mß║½u giß║źm n├│i tr├¬n.
HŲ░ß╗øng dß║½n giß║Żi:
nNaOH = 0,025 .1 = 0,025 mol
CH3COOH + NaOH ŌåÆ CH3COONa + H2O
nCH3COOH = nNaOH = 0,025 mol
mCH3COOH = 0,025 . 60 = 1,5 g
mdd CH3COOH = D.V = 1.40 = 40 g
\(C\% (C{H_3}COOH) = \frac{{1,5}}{{40}}.100\% = 3,75\% \)
B├Āi 9 trang 257 SGK H├│a 11 n├óng cao
Th├¬m nŲ░ß╗øc v├Āo 10 ml axit axetic bß║▒ng (axit 100%, D = 1,05 g/cm3) ─æß║┐n thß╗ā t├Łch 1,75 l├Łt ß╗¤ 25oC rß╗ōi d├╣ng m├Īy ─æo th├¼ thß║źy pH = 2,9.
a) T├Łnh nß╗ōng ─æß╗Ö mol cß╗¦a dung dß╗ŗch thu ─æŲ░ß╗Żc.
b) T├Łnh ─æß╗Ö ─æiß╗ćn li ╬▒ cß╗¦a axit axetic ß╗¤ dung dß╗ŗch n├│i tr├¬n.
c) T├Łnh gß║¦n ─æ├║ng hß║▒ng sß╗æ c├ón bß║▒ng cß╗¦a axit axetic ß╗¤ 25oC.
HŲ░ß╗øng dß║½n giß║Żi:
Câu a:
Số mol CH3COOH:
\(n = \frac{{C\% .D.V}}{{100.M}} = 0,175mol\)
Nß╗ōng ─æß╗Ö mol/lit cß╗¦a CH3COOH trong dung dß╗ŗch: CM = 0,175/1,75 = 0,1 M
Câu b:
pH=2,9 ŌćÆ [H+]=10-2,9 M
CH3COOH Ōćö CH3COO- + H+
TrŲ░ß╗øc ─æiß╗ćn li 0,1 0 0
─Éiß╗ćn li 0,1\(\alpha \) 0,1\(\alpha \) 0,1\(\alpha \)
Sau ─æiß╗ćn li (0,1 - 0,1\(\alpha \) ) 0,1\(\alpha \) 0,1\(\alpha \)
Ta c├│: 0,1\(\alpha \) = 10-2,9 Ōćö \(\alpha \) = 10-1,9 = 0,0126
Câu c:
\({K_a} = \frac{{[C{H_3}CO{O^ - }][{H^ + }]}}{{[C{H_3}COOH]}} = \frac{{0,1\alpha .0,1\alpha }}{{0,1.(1 - \alpha )}}\)
V├¼ \(\alpha \) << 1 ŌćÆ 0,1.(1- \(\alpha \)) = 0,1
\( \to {K_a} = 0,1.{\alpha ^2} = 0,{1.10^{ - 3,8}} = {10^{ - 4,8}} = 1,{58.10^{ - 5}}\)
Tr├¬n ─æ├óy l├Ā nß╗Öi dung chi tiß║┐t Giß║Żi b├Āi tß║Łp n├óng cao H├│a 11 ChŲ░ŲĪng ChŲ░ŲĪng 9 B├Āi 61, vß╗øi hŲ░ß╗øng dß║½n giß║Żi chi tiß║┐t, r├Ą r├Āng, tr├¼nh b├Āy khoa hß╗Źc. Hoc247 hy vß╗Źng ─æ├óy sß║Į l├Ā t├Āi liß╗ću hß╗»u ├Łch gi├║p c├Īc bß║Īn hß╗Źc sinh lß╗øp 11 hß╗Źc tß║Łp thß║Łt tß╗æt
T├Āi liß╗ću li├¬n quan
TŲ░ liß╗ću nß╗Ģi bß║Łt tuß║¦n
- Xem thêm










