Dưới đây là lý thuyết và bài tập minh họa Bài 10: Công thức phân tử hợp chất hữu cơ môn Hóa học lớp 11 Cánh diều. Bài giảng đã được HOC247 biên soạn ngắn gọn, đầy đủ, dễ hiểu về công thức phân tử hợp chất hữu cơ, cách lập công thức phân tử của hợp chất hữu cơ và sơ lược về phổ khối lượng MS.
Hi vọng bài giảng dưới đây sẽ giúp các em dễ dàng nắm được nội dung chính của bài.
Tóm tắt lý thuyết
1.1. Thành phần nguyên tố và công thức phân tử
|
Công thức phân tử cho biết thành phần nguyên tố và số lượng nguyên tử của mỗi nguyên tố trong phân tử. |
- Thành phần các nguyên tử có trong phân tử chất hữu cơ cho biết những nguyên tố hoá học tạo nên hợp chất đó. Số lượng các nguyên tử cho biết các nguyên tố kết hợp với nhau theo tỉ lệ nào.
Ví dụ: Khi butane và propane là khí hoá lỏng được nên trong bình gas, được các gia đình sử dụng để đun, nấu có công thức phân tử là C3H4 và C4H10.
- Công thức đơn giản nhất (còn được gọi là công thức thực nghiệm) cho biết tỉ lệ số nguyên tử của các nguyên tố có trong phân tử hợp chất hữu cơ (tỉ lệ các số nguyên tối giản).
Ví dụ: Hợp chất glucose có nhiều trong quả nho chín có công thức phân tử là C6H12O6, thì công thức đơn giản nhất là CH2O.
- Một hợp chất hữu cơ có công thức phân tử là CxHyOz.
- Thiết lập công thức đơn giản nhất bằng cách lập tỉ lệ x : y : z ở dạng số nguyên tối giản p : q : r
- Phân tích định lượng, ta được tỉ lệ phần trăm các nguyên tố trong phân tử.
\(x:y:z = \frac{{\% C}}{{12,0}}{\rm{: }}\frac{{\% H}}{{1,0}}{\rm{: }}\frac{{\% O}}{{16,0}}{\rm{ }} = p:q:r\)
- Từ đó thiết lập được công thức đơn giản nhất: CpHqOr.
- Trong đó: p, q, r là các số nguyên tối giản; x, y, z, n là số nguyên dương.
- %C, %H, %O, lần lượt là % khối lượng của các nguyên tố C, H, O, N trong hợp chất hữu cơ.
- Khi biết phân tử khối, xác định được giá trị n, từ đó suy ra công thức phân tử.
– Công thức phân tử cho biết số nguyên tử của các nguyên tố có trong phân tử.
- Mối quan hệ giữa công thức phân tử và công thức đơn giản nhất:
CxHyOz = (CpHqOr)n
1.2. Phương pháp xác định phân tử khối của hợp chất hữu cơ - Phổ khối lượng (MS)
– Hiện nay, người ta thường sử dụng phổ khối lượng để xác định phân tử khối của hợp chất hữu cơ.
– Trên phổ khối lượng, mỗi tín hiệu (peak) tương ứng với một phân mảnh ion khi các phân tử hợp chất hữu cơ bị ion hoá trong thiết bị phân tích phổ.
– Mỗi peak được xác định bởi giá trị m/z và cường độ tương đối (%).
– Có thể dự đoán phân tử khối của hợp chất hữu cơ đơn giản bằng tín hiệu của mảnh ion phân tử (kí hiệu là [M+]).
– Mảnh ion phân tử này thường ứng với tín hiệu có giá trị m/z lớn nhất.
– Trong thiết bị đo phổ khối lượng, hợp chất hữu cơ thường bị bắn phá bởi các electron có năng lượng cao và bị chuyển thành mảnh ion phân tử.
– Quá trình này được gọi là quá trình ion hoá. Ion phân tử có thể tiếp tục bị phân mảnh để trở thành những phân mảnh ion có khối lượng nhỏ hơn.
– m là khối lượng của ion, z là điện tích của ion. Đa số các ion đều mang điện tích dương +1 nên m/z tương đương với m. Do đó, máy được gọi là máy phân tích khối phố.
%20v%C3%A0%20phenol%20(b.png)
Hình 10.1. Phổ khối lượng của naphtalene (a) và phenol (b)
| Phổ khối lượng có thể cho thông tin về phân tử khối của hợp chất hữu cơ thông qua mảnh ion phân tử thường ứng với tín hiệu có giá trị m/z lớn nhất. |
Bài tập minh họa
Bài 1. Phân tích chất hữu cơ X chứa C, H, O ta có: mC : mH : mO = 2,24 : 0,357 : 2. Hãy xác định công thức đơn giản nhất của X.
Hướng dẫn giải
Gọi CTPT X là: CxHyOz
\(x:y:z=\frac{{{m}_{C}}}{12}:\frac{{{m}_{H}}}{1}:\frac{{{m}_{O}}}{16}=\text{ }0,187\text{ }:\text{ }0,375\text{ }:\text{ }0,125\text{ }=\text{ }3\text{ }:\text{ }6\text{ }:\text{ }2\)
\(\Rightarrow\) CTĐG: C3H6O2
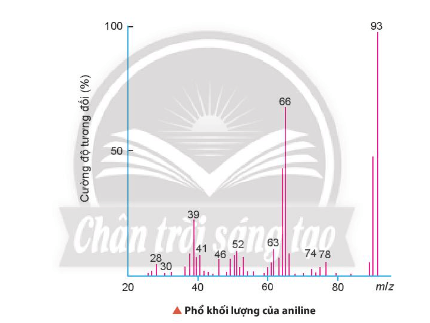
Bài 2. Aniline là hợp chất quan trọng trong công nghiệp phẩm nhuộm và sản xuất polymer. Kết quả phân tích nguyên tố của aniline như sau: 77,42% C; 7,53% H về khối lượng, còn lại là nitrogen. Phân tử khối của aniline được xác định trên phổ khối lượng tương ứng với peak có cường độ tương đối mạnh nhất. Lập công thức phân tử của aniline.
Hướng dẫn giải
%mN = 100% - 77,42% - 7,53% = 15,05%.
- Đặt công thức phân tử của aniline là CxHyNz.
- Dựa vào phổ khối lượng của aniline xác định được Maniline = 93.
Vậy:
\(\begin{align} & x=\frac{%{{m}_{C}}}{12}.\frac{M}{100}=\frac{77,42}{12}.\frac{93}{100}=2 \\ & y=\frac{%{{m}_{H}}}{1}.\frac{M}{100}=\frac{7,53}{1}.\frac{93}{100}=6 \\ & z=\frac{%{{m}_{N}}}{14}.\frac{M}{100}=\frac{15,05}{14}.\frac{93}{100}=1 \\ \end{align} \)
⇒ Công thức phân tử của aniline là: C6H7N.
Luyện tập Bài 10 Hóa 11 Cánh Diều
Học xong bài học này, em có thể:
Học xong bài học này, em có thể:
– Sử dụng được kết quả phổ khối lượng (MS) để xác định phân tử khối của hợp chất hữu cơ.
– Nêu được khái niệm về công thức phân tử hợp chất hữu cơ.
– Lập được công thức phân tử hợp chất hữu cơ từ dữ liệu phân tích nguyên tố và phân tử khối.
3.1. Trắc nghiệm Bài 10 Hóa 11 Cánh Diều
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 11 CD Bài 10 cực hay có đáp án và lời giải chi tiết.
-
- A. Số lượng các nguyên tố trong hợp chất.
- B. Tỉ lệ giữa các nguyên tố trong hợp chất.
- C. Cấu trúc phân tử hợp chất hữu cơ.
- D. Tất cả đều sai.
-
- A. Số lượng các nguyên tố trong hợp chất.
- B. Tỉ lệ giữa các nguyên tố trong hợp chất
- C. Hàm lượng mỗi nguyên tố trong hợp chất.
- D. Cấu trúc phân tử hợp chất hữu cơ.
-
- A. 2 : 4 : 2
- B. 3 : 2 : 1
- C. 3 : 4 : 1
- D. 1 : 2 : 2
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK Bài 10 Hóa 11 Cánh Diều
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 11 CD Bài 10 để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Mở đầu trang 63 SGK Hóa học 11 Cánh diều – CD
Vận dụng 1 trang 64 SGK Hóa học 11 Cánh diều – CD
Giải Câu hỏi 1 trang 64 SGK Hóa học 11 Cánh diều – CD
Vận dụng 2 trang 64 SGK Hóa học 11 Cánh diều – CD
Giải Câu hỏi 2 trang 65 SGK Hóa học 11 Cánh diều – CD
Giải Bài 1 trang 66 SGK Hóa học 11 Cánh diều – CD
Giải Bài 2 trang 66 SGK Hóa học 11 Cánh diều – CD
Giải Bài 3 trang 66 SGK Hóa học 11 Cánh diều – CD
Giải Bài 4 trang 66 SGK Hóa học 11 Cánh diều – CD
Giải Bài 5 trang 66 SGK Hóa học 11 Cánh diều – CD
Hỏi đáp Bài 10 Hóa 11 Cánh Diều
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học HOC247 sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!









