Giải bài 18.13 trang 65 SBT Hóa học 10 Cánh Diều
a) X là các nguyên tố bền thuộc nhóm halogen. Hãy điền công thức hóa học của nguyên tố, chất, ion theo thứ tự với các tính chất tương ứng theo bảng sau:

b) Viết các phản ứng chứng minh sự thay đổi tính khử của các ion X- theo xu hướng trong bảng tuần hoàn đã được hoàn thành ở câu a.
c) Tìm hiểu và giải thích vì sao tính acid của các hợp chất HX lại được thay đổi theo thứ tự như câu a.
Hướng dẫn giải chi tiết bài 18.13
Phương pháp giải:
Đi từ florine đến iodine độ âm điện giảm dần, tính oxi hoá giảm dần, tính khử và tính acid tăng dần.
Lời giải chi tiết:
a)
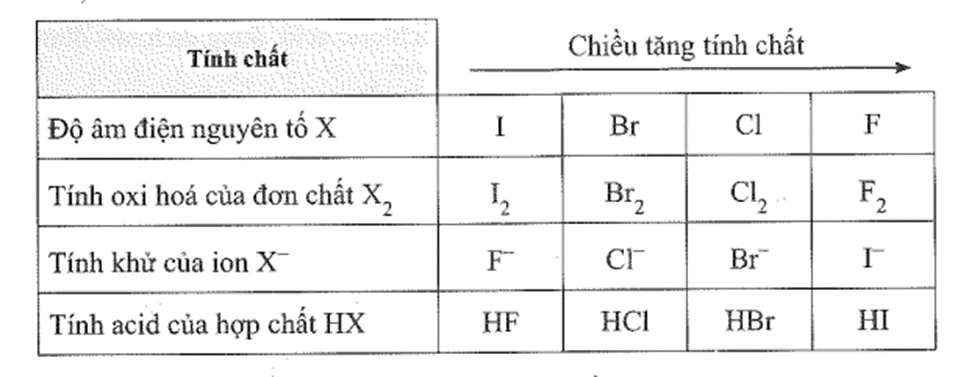
b) Phản ứng chứng minh tính khử của các ion tăng dần theo thứ tự: F-, Br-, Cl-, I-:
Phản ứng với sulfuric acid đặc trong cùng điều kiện:
NaF(s) + H2SO4(l) → NaHSO4(s) + HF(g)
NaCl(s) + H2SO4(l) → NaHSO4(s) + HCl(g)
2NaBr(s) + 3H2SO4(l) → 2NaHSO4(s) + Br2(g) + SO2(g) + 2H2O(g)
8NaI(s) + 9H2SO4(l) → 8NaHSO4(s) + H2S(g) + 4I2(g) + 4H2O(g)
Dễ thấy F- và Cl- không thể hiện tính khử; Br- khử lưu huỳnh (sulfur) có số oxi hóa +6 về số oxi hóa +4; I- có thể khử lưu huỳnh (sulfur) có số oxi hóa +6 xuống số oxi hóa thấp hơn là -2.
Vậy tính khử I- > Br-> Cl-, F- (1).
Mặt khác, Cl- trong HCl đặc có thể khử MnO2 theo phản ứng sau:
MnO2(s) + 4HCl(aq) → MnCl2(aq) + Cl2(g) + 2H2O(l)
Phản ứng này dùng để điều chế Cl2 trong phòng thí nghiệm, trong khi đó F- trong điều kiện tương tự thì không xảy ra phản ứng. Ngoài ra, F- gần như không thể bị oxi hóa bởi các hóa chất khác trong điều kiện thông thường.
Vậy tính khử Cl- > F- (2)
Từ (1) và (2) suy ra điều cần chứng minh.
c) Nguyên nhân chủ yếu làm tăng độ mạnh của các acid theo dãy HF, HCl, HBr, HI là do sự giảm độ bền liên kết theo thứ tự: H – F > H – Cl > H – Br > H – I.
-- Mod Hóa Học 10 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.





