Giải bài 14.11 trang 37 SBT Hóa học 10 Kết nối tri thức
Dùng công thức Lewis để biểu diễn phân tử SO3 sao cho phù hợp với quy tắc octet. Chỉ rõ các liên kết trong phân tử thuộc loại liên kết nào.
Hướng dẫn giải chi tiết bài 14.11
Phương pháp giải:
- Quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm Helium)
- Các bước thực hiện:
+ Bước 1: Viết cấu hình electron của các nguyên tử
+ Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử
+ Bước 3: Viết sự hình thành liên kết trong các phân tử
Lời giải chi tiết:
16S: \(1{s^2}2{s^2}2{p^6}3{s^2}3{p^4}\)
8O: \(1{s^2}2{s^2}2{p^4}\)
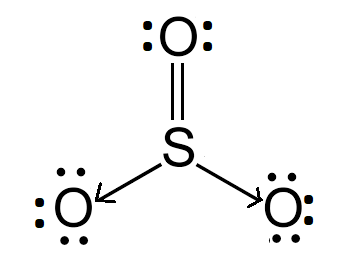
Nguyên tử trung tâm S có 6 electron lớp ngoài cùng và nguyên tử O cũng có 6 electron lớp ngoài cùng. Khi tạo thành phân tử SO3 nguyên tử S và 2 nguyên tử O dùng chung 2 cặp electron để tạo 2 liên kết cộng hoá trị kép phân cực. Để thoả mãn quy tắc octet, liên kết cộng hoá trị giữa nguyên tử S và 2 nguyên tử O còn lại được thực hiện bằng sự cho - nhận 2 cặp electron của nguyên tử S. Kết quả. trong phân tử SO3 các nguyên tử S và O đều có 8 eleetron lớp ngoài cùng thoã mãn quy tắc octet.
Công thức Lewis:
-- Mod Hóa Học 10 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.
Bài tập SGK khác
Giải bài 14.9 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.10 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.12 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.13 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.14 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.15 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.16 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.17 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT




