Giải bài 14.14 trang 38 SBT Hóa học 10 Kết nối tri thức
Dựa vào giá trị của độ âm điện ở Bảng 6.2 trong sách giáo khoa Hóa học 10, hãy nêu bản chất liên kết trong các phân tử và ion sau: HClO, KHS, HCO3-, K2SO4.
Hướng dẫn giải chi tiết bài 14.14
Phương pháp giải:
Dựa vào hiệu độ âm điện:
|
Hiệu độ âm điện (\(\Delta \chi \)) |
Loại liên kết |
|
\(0 \le \Delta \chi < 0,4\) |
Cộng hóa trị không phân cực |
|
\(0,4 \le \Delta \chi < 1,7\) |
Cộng hóa trị phân cực |
|
\(\Delta \chi \ge 1,7\) |
Ion |
Lời giải chi tiết:
Bản chất các liên kết phụ thuộc vào hiệu độ âm điện giữa hai nguyên tử của hai nguyên tố tạo liên kết. Viết công thức cấu tạo các phân tử và tính hiệu độ âm điện để suy ra bản chất liên kết.
H-Cl=O có hiệu độ âm điện H-Cl là 0,96 ⇒ Liên kết cộng hóa trị phân cực
Cl-O là 0,28 ⇒ Liên kết cộng hóa trị không phân cực.
K+ và [S-H]- có hiệu độ âm điện K và S là 1,76 ⇒ liên kết ion;
S-H là 0,38 ⇒ liên kết cộng hóa trị phân cực.
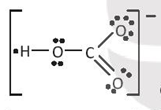
có hiệu độ âm điện H và O là 1,24 ⇒ liên kết cộng hóa trị phân cực;
C-O có hiệu độ âm điện là 0,89 ⇒ liên kết cộng hóa trị phân cực.
* K+ và 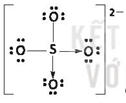 có hiệu độ âm điện K-O là 2,62 ⇒ liên kết ion;
có hiệu độ âm điện K-O là 2,62 ⇒ liên kết ion;
S-O là 1,54 ⇒ liên kết cộng hóa trị phân cực.
-- Mod Hóa Học 10 HỌC247
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.
Bài tập SGK khác
Giải bài 14.12 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.13 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.15 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.16 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.17 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT




