HŲ░ß╗øng dß║½n Giß║Żi b├Āi tß║Łp H├│a hß╗Źc 11 KNTT B├Āi 20 Alcohol m├┤n Ho├Ī hß╗Źc lß╗øp 11 gi├║p c├Īc em hß╗Źc sinh nß║»m vß╗»ng phŲ░ŲĪng ph├Īp giß║Żi b├Āi tß║Łp v├Ā ├┤n luyß╗ćn tß╗æt kiß║┐n thß╗®c.
-
Mß╗¤ ─æß║¦u trang 119 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Tß╗½ xa xŲ░a con ngŲ░ß╗Øi ─æ├Ż biß║┐t l├¬n men c├Īc loß║Īi ng┼® cß╗æc, hoa quß║Ż ─æß╗ā tß║Īo ra c├Īc ─æß╗ō uß╗æng c├│ cß╗ōn (c├│ chß╗®a ethanol ŌĆō mß╗Öt alcohol quen thuß╗Öc). Ng├Āy nay, alcohol ─æŲ░ß╗Żc sß╗Ł dß╗źng phß╗Ģ biß║┐n trong nhiß╗üu l─®nh vß╗▒c kh├Īc nhau nhŲ░ l├Ām dung m├┤i, nguy├¬n liß╗ću ho├Ī hß╗Źc, nhi├¬n liß╗ću, x─āng sinh hß╗Źc, ŌĆ” Vß║Ły alcohol l├Ā g├¼ v├Ā c├│ nhß╗»ng t├Łnh chß║źt ─æß║Ęc trŲ░ng n├Āo?
-
Giß║Żi C├óu hß╗Åi 1 trang 120 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Viß║┐t c├Īc ─æß╗ōng ph├ón cß║źu tß║Īo cß╗¦a alcohol c├│ c├┤ng thß╗®c C4H9OH v├Ā x├Īc ─æß╗ŗnh bß║Łc cß╗¦a c├Īc alcohol ─æ├│.
-
Giß║Żi C├óu hß╗Åi 2 trang 121 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
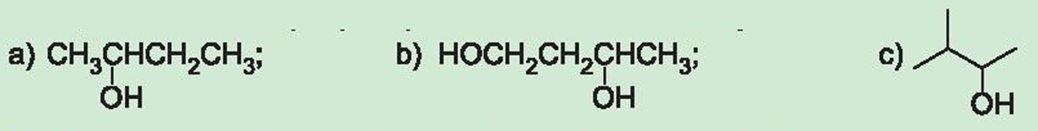
Gß╗Źi t├¬n theo danh ph├Īp thay thß║┐ c├Īc alcohol dŲ░ß╗øi ─æ├óy:
-
Giß║Żi C├óu hß╗Åi 3 trang 121 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Viß║┐t c├┤ng thß╗®c cß║źu tß║Īo cß╗¦a c├Īc alcohol c├│ t├¬n gß╗Źi dŲ░ß╗øi ─æ├óy:
a) pentan ŌĆō 1 ŌĆō ol;
b) but ŌĆō 3 ŌĆō en ŌĆō 1 ŌĆō ol;
c) 2 ŌĆō methylpropan ŌĆō 2 ŌĆō ol;
d) butane ŌĆō 2,3 ŌĆō diol.
-
Hoß║Īt ─æß╗Öng trang 122 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
C├Īc hß╗Żp chß║źt propane, dimethyl ether v├Ā ethanol c├│ ph├ón tß╗Ł khß╗æi tŲ░ŲĪng ─æŲ░ŲĪng nhau v├Ā c├│ mß╗Öt sß╗æ t├Łnh chß║źt nhŲ░ sau:
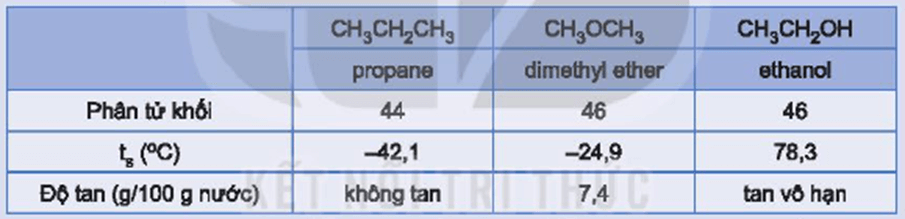
H├Ży giß║Żi th├Łch tß║Īi sao ethanol c├│ nhiß╗ćt ─æß╗Ö s├┤i cao hŲĪn v├Ā tan trong nŲ░ß╗øc tß╗æt hŲĪn so vß╗øi hai chß║źt c├▓n lß║Īi.
-
Giß║Żi C├óu hß╗Åi 4 trang 123 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Tß╗½ sß╗æ liß╗ću ß╗¤ Bß║Żng 20.3, em h├Ży giß║Żi th├Łch tß║Īi sao trong d├Ży alcohol no, ─æŲĪn chß╗®c, mß║Īch hß╗¤, nhiß╗ćt ─æß╗Ö s├┤i cß╗¦a c├Īc alcohol t─āng dß║¦n tß╗½ C1 ─æß║┐n C5 c├▓n ─æß╗Ö tan trong nŲ░ß╗øc giß║Żm dß║¦n tß╗½ C3 ─æß║┐n C5.
-
Giß║Żi C├óu hß╗Åi 5 trang 124 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
─Éun n├│ng butan ŌĆō 2 ŌĆō ol vß╗øi sulfuric acid ─æß║Ęc thu ─æŲ░ß╗Żc c├Īc alkene n├Āo? Sß║Żn phß║®m n├Āo l├Ā sß║Żn phß║®m ch├Łnh.
-
Giß║Żi C├óu hß╗Åi 6 trang 124 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Viß║┐t c├┤ng thß╗®c cß║źu tß║Īo sß║Żn phß║®m cß╗¦a phß║Żn ß╗®ng khi oxi ho├Ī c├Īc alcohol sau bß║▒ng CuO ─æun n├│ng:

-
Th├Ł nghiß╗ćm trang 124 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Nghi├¬n cß╗®u vß╗ü phß║Żn ß╗®ng ch├Īy cß╗¦a alcohol
Chuß║®n bß╗ŗ: cß╗ōn 90o (cß╗ōn y tß║┐), b├Īt sß╗®, que ─æ├│m d├Āi khoß║Żng 20 cm.
Tiß║┐n h├Ānh: Lß║źy khoß║Żng 1 mL ethanol (ch├║ ├Į kh├┤ng lß║źy nhiß╗üu hŲĪn) cho v├Āo b├Īt sß╗®. ─Éß╗æt ch├Īy que ─æ├│m v├Ā ─æŲ░a ngß╗Źn lß╗Ła v├Āo gß║¦n miß╗ćng b├Īt sß╗® ─æß╗ā ─æß╗æt ch├Īy ethanol.
LŲ░u ├Į: Cß║®n thß║Łn bß╗Ång khi thß╗▒c hiß╗ćn th├Ł nghiß╗ćm ─æß╗æt ch├Īy cß╗ōn.
Quan s├Īt hiß╗ćn tŲ░ß╗Żng v├Ā viß║┐t phŲ░ŲĪng tr├¼nh ho├Ī hß╗Źc cß╗¦a phß║Żn ß╗®ng xß║Ży ra.
-
Th├Ł nghiß╗ćm trang 125 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Copper(II) hydroxide t├Īc dß╗źng vß╗øi alcohol ─æa chß╗®c
Chuß║®n bß╗ŗ: dung dß╗ŗch CuSO4 2%, dung dß╗ŗch NaOH 10%, ethanol, glycerol; 2 ß╗æng nghiß╗ćm.
Tiß║┐n h├Ānh:
- Cho v├Āo 2 ß╗æng nghiß╗ćm, mß╗Śi ß╗æng khoß║Żng 1 mL dung dß╗ŗch CuSO4 2% v├Ā 1 mL dung dß╗ŗch NaOH 10%.
- Lß║»c nhß║╣ 2 ß╗æng nghiß╗ćm rß╗ōi nhß╗Å v├Āo tß╗½ng ß╗æng:
ß╗Éng nghiß╗ćm (1): 5 giß╗Źt ethanol.
ß╗Éng nghiß╗ćm (2): 5 giß╗Źt glycerol.
- Lß║»c ─æß╗üu cß║Ż 2 ß╗æng nghiß╗ćm.
Quan s├Īt hiß╗ćn tŲ░ß╗Żng xß║Ży ra ß╗¤ tß╗½ng ß╗æng nghiß╗ćm, giß║Żi th├Łch v├Ā viß║┐t phŲ░ŲĪng tr├¼nh ho├Ī hß╗Źc.
-
Giß║Żi C├óu hß╗Åi 7 trang 125 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Viß║┐t phŲ░ŲĪng tr├¼nh ho├Ī hß╗Źc cß╗¦a phß║Żn ß╗®ng giß╗»a methanol vß╗øi sodium.
-
Giß║Żi C├óu hß╗Åi 8 trang 125 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
N├¬u phŲ░ŲĪng ph├Īp ho├Ī hß╗Źc ─æß╗ā ph├ón biß╗ćt methanol v├Ā ethylene glycol.
-
Giß║Żi C├óu hß╗Åi 9 trang 127 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Mß╗Öt ─æŲĪn vß╗ŗ cß╗ōn tŲ░ŲĪng ─æŲ░ŲĪng 10 mL (hoß║Ęc 7,89 gam) ethanol nguy├¬n chß║źt. Theo khuyß║┐n c├Īo cß╗¦a ng├Ānh y tß║┐, ─æß╗ā ─æß║Żm bß║Żo sß╗®c khoß║╗ mß╗Śi ngŲ░ß╗Øi trŲ░ß╗¤ng th├Ānh kh├┤ng n├¬n uß╗æng qu├Ī 2 ─æŲĪn vß╗ŗ cß╗ōn mß╗Śi ng├Āy. Vß║Ły mß╗Śi ngŲ░ß╗Øi trŲ░ß╗¤ng th├Ānh kh├┤ng n├¬n uß╗æng qu├Ī bao nhi├¬u mL rŲ░ß╗Żu 40o mß╗Öt ng├Āy?
-
Giß║Żi C├óu hß╗Åi 10 trang 127 SGK H├│a hß╗Źc 11 Kß║┐t nß╗æi tri thß╗®c ŌĆō KNTT
Viß║┐t phŲ░ŲĪng tr├¼nh ho├Ī hß╗Źc cß╗¦a c├Īc phß║Żn ß╗®ng trong sŲĪ ─æß╗ō ─æiß╗üu chß║┐ glycerol tß╗½ propylene.





