Hướng dẫn Giải bài tập Hóa học 11 CTST Bài 15 Dẫn xuất halogen môn Hóa học lớp 11 giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức.
-
Mở đầu trang 92 SGK Hóa học 11 Chân trời sáng tạo – CTST
Trong y khoa, gây mê là phương pháp làm bệnh nhân mất ý thức, phục hồi được sau một thời gian, không đau và đảm bảo an toàn trong suốt quá trình phẫu thuật. Halothane được dùng làm thuốc gây mê, phù hợp cho nhiều độ tuổi, ít ảnh hưởng đến sức khoẻ của bệnh nhân trong và sau phẫu thuật. Công thức cấu tạo của phân tử halothane là:
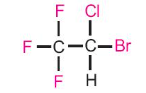
Halothane là dẫn xuất halogen của hydrocarbon, có tính chất đặc trưng và ứng dụng thực tiễn. Dẫn xuất halogen của hydrocarbon là gì? Có những tính chất và ứng dụng trong lĩnh vực nào?
-
Thảo luận 1 trang 93 SGK Hóa học 11 Chân trời sáng tạo – CTST
Em hãy cho biết thành phần các nguyên tố có trong dẫn xuất halogen của hydrocarbon.
-
Hoạt động trang 93 SGK Hoá học 11 Chân trời sáng tạo – CTST
Cho các chất sau: CH3Br, Cl2O7, F2C=CF2, CH2Cl2, HCl, COCl2 (phosgene). Chất nào là dẫn xuất halogen của hydrocarbon?
-
Thảo luận 2 trang 93 SGK Hóa học 11 Chân trời sáng tạo – CTST
Quan sát Ví dụ 1 và Ví dụ 2, cho biết cách đánh số thứ tự mạch carbon trong dẫn xuất halogen và dẫn xuất halogen có các loại đồng phân cấu tạo nào.
-
Hoạt động trang 94 SGK Hoá học 11 Chân trời sáng tạo – CTST
Viết công thức cấu tạo và gọi tên thay thế của các đồng phân dẫn xuất halogen có công thức phân tử C3H7Cl.
-
Thảo luận 3 trang 94 SGK Hóa học 11 Chân trời sáng tạo – CTST
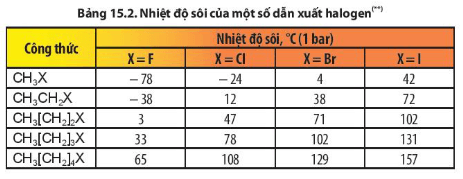
Dựa vào Bảng 15.2, cho biết xu hướng biến đổi nhiệt độ sôi của các dẫn xuất halogen theo chiều tăng độ dài mạch carbon (cùng loại halogen) và theo chiều tăng nguyên tử khối của halogen từ F, Cl, Br, I (cùng gốc alkyl).
-
Hoạt động trang 95 SGK Hoá học 11 Chân trời sáng tạo – CTST
Cho các chất ethanol (C2H5OH) và dichloromethane (CH2Cl2) vào 2 ống nghiệm chứa dung dịch CuSO4 loãng, lắc hỗn hợp và để yên như hình bên. Cho biết ống nghiệm nào chứa dichloromethane.

-
Thảo luận 4 trang 95 SGK Hóa học 11 Chân trời sáng tạo – CTST
Trong thí nghiệm thuỷ phân bromoethane, giải thích tại sao cần phải rửa ion Br-.
-
Thảo luận 5 trang 95 SGK Hóa học 11 Chân trời sáng tạo – CTST
Hãy cho biết mục đích của việc acid hoá dung dịch sau thuỷ phân bằng dung dịch HNO3. Có thể thay dung dịch HNO3 bằng dung dịch H2SO4 hoặc dung dịch HCl được không?
-
Thảo luận 6 trang 95 SGK Hóa học 11 Chân trời sáng tạo – CTST
Giải thích kết quả của thí nghiệm ở Bước 4.
-
Thảo luận 7 trang 96 SGK Hóa học 11 Chân trời sáng tạo – CTST
Trong phản ứng tách hydrogen halide, cho biết nguyên tử hydrogen ở nguyên tử carbon nào được tách cùng với nguyên tử halogen ra khỏi dẫn xuất.
-
Hoạt động trang 96 SGK Hoá học 11 Chân trời sáng tạo – CTST
Hoàn thành phương trình hóa học
a) CH3Cl + KOH →
b) CH3CH2Br + NaOH →
c) CH2=CHCH2Cl + NaOH →
d) CH3CH2Br \(\xrightarrow{+KOH,ethanol,{{t}^{o}}}\)
e)
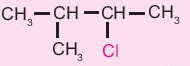 \(\xrightarrow{+KOH,ethanol,{{t}^{o}}}\)
\(\xrightarrow{+KOH,ethanol,{{t}^{o}}}\) -
Thảo luận 8 trang 97 SGK Hóa học 11 Chân trời sáng tạo – CTST
Hiện nay, vì yếu tố lợi nhuận mà vấn đề lạm dụng thuốc bảo vệ thực vật, thuốc kích thích tăng trưởng gây tác hại nghiêm trọng đến sức khoẻ người tiêu dùng. Hãy đưa ra hướng giải quyết về tình trạng trên.

-
Giải Bài 1 trang 98 SGK Hóa học 11 Chân trời sáng tạo – CTST
Gọi tên các dẫn xuất halogen:
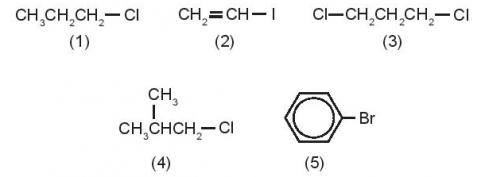
-
Giải Bài 2 trang 98 SGK Hóa học 11 Chân trời sáng tạo – CTST
Cho sơ đồ biến đổi của 1-chloropropane như sau:
CH3CH=CH2 \(\xleftarrow{\left( 1 \right)}\) CH3CH2CH2Cl \(\xrightarrow{\left( 2 \right)}\) CH3CH2CH2OH
a) Gọi tên loại phản ứng (1), (2) và hoàn thành các phương trình hoá học.
b) Thực hiện 2 phản ứng theo sơ đổ trên khi thay hợp chất CH3CH2CH2Cl bằng 2-bromobutane. Xác định sản phẩm hữu cơ chính (nếu có) trong các phản ứng.
-
Giải Bài 3 trang 98 SGK Hóa học 11 Chân trời sáng tạo – CTST
CFC là hợp chất khó cháy, không độc và trơ về mặt hoá học. Trước đây CFC chủ yếu được sử dụng trong công nghiệp nhiệt lạnh. CFC không gây hại ở điều kiện thường, nhưng trên khí quyển của Trái Đất, chúng tồn tại trong khoảng 100 năm và khuếch tán lên tầng bình lưu. Dưới tác dụng của tia UV từ Mặt Trời, liên kết C – Cl của CFC bị phá vỡ, tạo ra gốc Cl tự do. Theo ước tính, mỗi năm gốc Cl tự do phá huỷ 1 triệu phân tử ozone. Việc không sử dụng CFC đã giúp lỗ hổng tầng ozone được thu hẹp. Ngày nay người ta đã sử dụng hợp chất nào để thay thế CFC trong công nghiệp làm lạnh để tránh việc phá huỷ tầng ozone?





