Hướng dẫn Giải bài tập Hóa học 11 CD Bài 19 Carboxylic acid môn Hóa học lớp 11 giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức.
-
Mở đầu trang 132 SGK Hóa học 11 Cánh diều – CD
Hãy viết công thức cấu tạo của acetic acid. Cho biết một số tính chất hoá học và ứng dụng của acetic acid mà em biết.
-
Luyện tập 1 trang 133 SGK Hóa học 11 Cánh diều – CD
Hãy chỉ ra hợp chất carboxylic acid trong số các chất dưới đây:
CH3 – COOH (A)
CH3 – CHO (B)
HOOC – COOH (C)
CH3 – CO – CH3 (D)
CH2 = CH – COOH (E)
-
Luyện tập 2 trang 133 SGK Hóa học 11 Cánh diều – CD
Viết công thức cấu tạo, gọi tên thay thế của các carboxylic acid có cùng công thức C5H10O2.
-
Giải Câu hỏi 1 trang 134 SGK Hóa học 11 Cánh diều – CD
Căn cứ các dữ liệu về nhiệt độ sôi và nhiệt độ nóng chảy, hãy chỉ ra các carboxylic acid nào ở thể lỏng, rắn ở điều kiện thường.
-
Luyện tập 3 trang 134 SGK Hóa học 11 Cánh diều – CD
Cho các chất có công thức sau: HCOOH (A), C2H6 (B), CH3CH = O (C), C2H5OH (D), CH3COOH (E). Hãy sắp xếp các chất trên theo chiều tăng dần nhiệt độ sôi của chúng và giải thích.
-
Giải Câu hỏi 2 trang 134 SGK Hóa học 11 Cánh diều – CD
Vì sao acetic acid có thể tan vô hạn trong nước?
-
Giải Câu hỏi 3 trang 135 SGK Hóa học 11 Cánh diều – CD
Từ đặc điểm cấu tạo của nhóm carboxyl, hãy dự đoán tính chất đặc trưng của các hợp chất carboxylic acid.
-
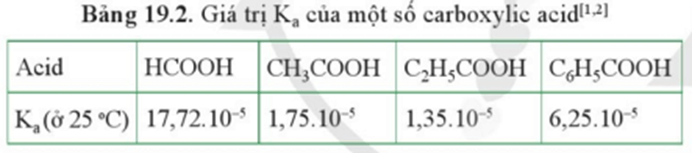
Giải Câu hỏi 4 trang 135 SGK Hóa học 11 Cánh diều – CD
Từ các giá trị Ka cho trong Bảng 19.2, hãy cho biết carboxylic acid no, đơn chức, mạch hở nào có tính acid mạnh nhất.
-
Thí nghiệm 1 trang 135 SGK Hóa học 11 Cánh diều – CD
Khả năng đổi màu quỳ tím của acetic acid
Nhúng đầu đũa thuỷ tinh vào dung dịch acetic acid 5%, sau đó chấm vào giấy quỳ tím. Quan sát và nhận xét sự thay đổi màu của giấy quỳ tím.
-
Thí nghiệm 2 trang 136 SGK Hóa học 11 Cánh diều – CD
Phản ứng của acetic acid với magnesium
Chuẩn bị: Dung dịch CH3COOH 1 M, phoi bào magnesium; ống nghiệm.
Tiến hành: Cho 1 – 2 mL dung dịch acetic acid 1M vào ống nghiệm, sau đó thêm vào vài mẩu magnesium.
Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích.
-
Luyện tập 4 trang 136 SGK Hóa học 11 Cánh diều – CD
Viết phương trình hoá học của phản ứng xảy ra giữa propionic acid với:
a) Zn.
b) CuO.
c) Cu(OH)2.
d) CaCO3.
-
Luyện tập 5 trang 136 SGK Hóa học 11 Cánh diều – CD
Trình bày cách phân biệt các dung dịch sau: acetic acid, acrylic acid, acetaldehyde.
-
Vận dụng trang 136 SGK Hóa học 11 Cánh diều – CD
Ấm (siêu) đun nước lâu ngày thường có một lớp cặn bám dưới đáy. Hãy đề xuất một phương pháp đơn giản để loại lớp cặn đó.
-
Thí nghiệm 3 trang 136 SGK Hóa học 11 Cánh diều – CD
Phản ứng của acetic acid với sodium carbonate
Chuẩn bị: Dung dịch CH3COOH 1 M, dung dịch Na2CO3 1M; ống nghiệm, diêm.
Tiến hành: Cho 1 – 2 mL dung dịch sodium carbonate 1 M vào ống nghiệm. Nhỏ tiếp vào ống nghiệm 1 – 2 mL dung dịch acetic acid 1 M. Đưa que diêm đang cháy vào miệng ống nghiệm.
Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích.
-
Luyện tập 6 trang 136 SGK Hóa học 11 Cánh diều – CD
Do phản ứng ester hoá là phản ứng thuận nghịch nên hiệu suất của phản ứng thường không cao. Đề xuất các biện pháp để nâng cao hiệu suất của phản ứng ester hoá.
-
Luyện tập 7 trang 137 SGK Hóa học 11 Cánh diều – CD
Trong thí nghiệm điều chế ethyl acetate, vì sao không đun sôi hỗn hợp phản ứng? Vai trò của dung dịch sodium chloride bão hoà là gì?
-
Thí nghiệm 4 trang 137 SGK Hóa học 11 Cánh diều – CD
Phản ứng điều chế ethyl acetate
Chuẩn bị: Cồn 96°, acetic acid nguyên chất, dung dịch H2SO4 đặc, dung dịch NaCl bão hoà, ống nghiệm.
Tiến hành: Cho 1 mL cồn 96° vào trong ống nghiệm. Cho tiếp vào trong ống nghiệm 1 mL acetic acid nguyên chất. Thêm vào ống nghiệm 1 – 2 giọt dung dịch sulfuric acid đậm đặc và lắc đều, dùng bông sạch nút miệng ống nghiệm. Sau đó, đun cách thuỷ trong cốc thuỷ tinh ở nhiệt độ 65 – 70 °C trong khoảng thời gian 5 – 7 phút. Làm lạnh ống nghiệm rồi cho thêm vào 2 mL dung dịch sodium chloride bão hoà. Để yên ống nghiệm.
Yêu cầu: Quan sát, mô tả hiện tượng và giải thích.
Chú ý an toàn: Cẩn thận khi làm việc với dung dịch H2SO4 đặc.
-
Giải Bài 1 trang 139 SGK Hóa học 11 Cánh diều – CD
Hợp chất X có công thức cấu tạo: (CH3)2CHCH2COOH. Tên của X là
A. 2 – methylpropanoic acid.
B. 2 – methylbutanoic acid.
C. 3 – methylbutanoic acid.
D. 3 – methylbutan – 1 – oic acid.
-
Giải Bài 2 trang 139 SGK Hóa học 11 Cánh diều – CD
Chất nào sau đây có nhiệt độ sôi cao nhất?
A. Propan – 1 – ol.
B. Acetaldehyde.
C. Formic acid.
D. Acetic acid.
-
Giải Bài 3 trang 139 SGK Hóa học 11 Cánh diều – CD
Trình bày phương pháp hoá học để phân biệt các dung dịch sau: ethanol, glycerol, acetaldehyde và acetic acid.
-
Giải Bài 4 trang 139 SGK Hóa học 11 Cánh diều – CD
Đun nóng 12 gam acetic acid với 13,8 gam ethanol (có dung dịch H2SO4 đặc làm xúc tác) thu được 11 gam ester. Tính hiệu suất của phản ứng ester hoá.
-
Giải Bài 5 trang 139 SGK Hóa học 11 Cánh diều – CD
Giấm được sử dụng khá phổ biến để chế biến thức ăn. Bạn Mai muốn xác định nồng độ acetic acid có trong giấm ăn bằng cách sử dụng dung dịch sodium hydroxyde 0,1M để chuẩn độ. Bạn lấy mẫu giấm ăn đó để làm thí nghiệm và kết quả chuẩn độ 3 lần như bảng sau:
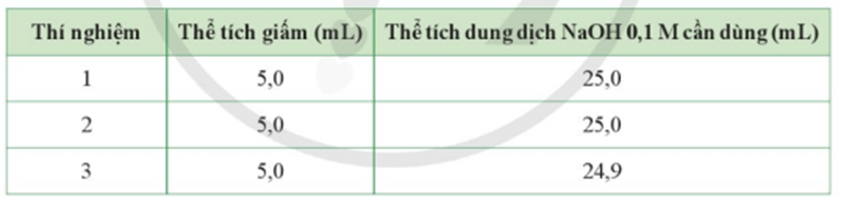
Hãy giúp bạn Mai xác định nồng độ mol của acetic acid trong giấm.
-
Giải Bài 6 trang 139 SGK Hóa học 11 Cánh diều – CD
Hợp chất X được dùng nhiều để tổng hợp polymer. Kết quả phân tích nguyên tố cho thấy X có %C = 50%, %H = 5,56% (về khối lượng), còn lại là O. Trên phổ đồ MS của X thấy xuất hiện peak của ion phân tử [M+] có giá trị m/z = 72. Trên phổ IR của X thấy xuất hiện một peak rộng từ 2 500 – 3 200 cm-1, một peak ở 1 707 cm-1. Lập luận và dự đoán công thức cấu tạo của X.





