Hoạt động trang 58 SGK Hoá học 11 Chân trời sáng tạo
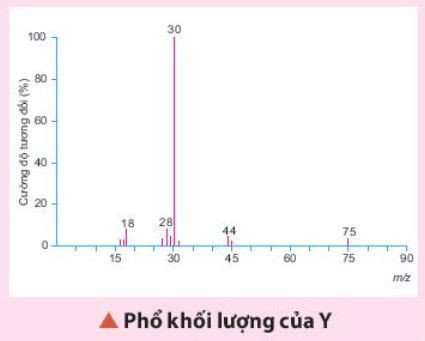
Một hợp chất hữu cơ Y có 32% C; 6,67% H; 18,67% N về khối lượng còn lại là O. Phân tử khối của hợp chất này được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất. Lập công thức phân tử của Y.
Hướng dẫn giải chi tiết Hoạt động trang 58
Phương pháp giải
HS dựa vào phân tử khối của X được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất, xác định công thức phân tử hợp chất hữu cơ bằng công thức.
\(\begin{align} & {{C}_{x}}{{H}_{y}}{{O}_{z}}{{N}_{t}} \\ & x=\frac{%{{m}_{C}}}{12}.\frac{M}{100} \\ & y=\frac{%{{m}_{H}}}{1}.\frac{M}{100} \\ & z=\frac{%{{m}_{O}}}{16}.\frac{M}{100} \\ & t=\frac{%{{m}_{N}}}{14}.\frac{M}{100} \\ \end{align} \)
Lời giải chi tiết
%mO = 100% - 32% - 6,67% - 18,67% = 42,66%.
Đặt công thức phân tử của Y là CxHyOzNt.
Từ phổ khối lượng của Y xác định được: MY = 75.
Vậy:
\(\begin{align} & x=\frac{\%{{m}_{C}}}{12}.\frac{M}{100}=\frac{32}{12}.\frac{75}{100}=2 \\ & y=\frac{\%{{m}_{H}}}{1}.\frac{M}{100}=\frac{6,67}{1}.\frac{75}{100}=5 \\ & z=\frac{\%{{m}_{O}}}{16}.\frac{M}{100}=\frac{42,66}{16}.\frac{75}{100}=2 \\ & t=\frac{\%{{m}_{N}}}{14}.\frac{M}{100}=\frac{18,67}{14}.\frac{75}{100}=1 \\ \end{align} \)
Công thức phân tử của Y: C2H5O2N.
-- Mod Hóa Học 11 HỌC247
-


Oxi hóa hoàn toàn 4,92g một hợp chất A chứa C, H, O, N và O rồi cho sản phẩm lần lượt qua bình chứa H2SO4 đậm đặc, bình chứa KOH thì thấy khối lượng bình chứa H2SO4 đặc tăng thêm 1,81mg, bình chứa KOH tăng thêm 10,56g.
bởi Trinh Hung
 29/06/2023
29/06/2023
Ở thí nghiệm khác, khi nung 6,15g hợp chất A với CuO thì thu được 0,55l (đktc) khí N2. Hàm lượng phần trăm của Oxi trong A là bao nhiêu?
A. 26,215%
B. 58,54%
C.11,18%
C.4,065%
Theo dõi (0) 1 Trả lời
Bài tập SGK khác
Thảo luận 1 trang 57 SGK Hóa học 11 Chân trời sáng tạo – CTST
Thảo luận 2 trang 58 SGK Hóa học 11 Chân trời sáng tạo – CTST
Giải Bài 1 trang 59 SGK Hóa học 11 Chân trời sáng tạo – CTST
Giải Bài 2 trang 60 SGK Hóa học 11 Chân trời sáng tạo – CTST
Giải Bài 3 trang 60 SGK Hóa học 11 Chân trời sáng tạo – CTST




