HOC247 đã tổng hợp, biên soạn các kiến thức trọng tâm trong Chương trình giữa HK1 môn KHTN 8 Kết nối tri thức thông qua nội dung Đề thi giữa HK1 môn KHTN 8 KNTT năm học 2023-2024 Trường THCS Nguyễn Tri Phương. Thêm vào đó, tương ứng với mỗi phần, HOC247 cung cấp hệ thống câu hỏi trắc nghiệm giúp các em có thể tự kiểm tra mức độ ghi nhớ bài của mình. Chúc các em học sinh đạt kết quả cao trong kì thi giữa HK1 sắp tới!
1. Đề thi
|
SỞ GDĐT TRƯỜNG THCS NGUYỄN TRI PHƯƠNG
|
ĐỀ THI GIỮA HK1 NĂM HỌC 2023-2024 Môn: KHTN 8 Thời gian làm bài:45 phút; không kể thời gian giao đề |
Phần I. Trắc nghiệm (6 điểm)
Hãy khoanh tròn chữ cái đứng trước câu trả lời mà em cho là đúng nhất. Mỗi câu trả lời đúng được 0,25 điểm.
Câu 1: Cầu chì (fuse) được sử dụng để
A. đo dòng điện, điện áp, công suất và năng lượng điện cung cấp cho mạch điện.
B. nhằm phòng tránh các hiện tượng quá tải trên đường dây gây cháy nổ.
C. chuyển đổi điện áp xoay chiều thành điện áp một chiều.
D. đo cường độ dòng điện trong mạch điện.
Câu 2: Dụng cụ nào dùng để đựng trộn các hóa chất rắn với nhau hoặc nung các chất ở nhiệt độ cao?
A. Cốc.
B. Bình tam giác.
C. Ống nghiệm.
D. Bát sứ.
Câu 3: Khi đun nóng hoá chất trong ống nghiệm, cách làm nào sau đây là sai?
A. Kẹp ống nghiệm bằng kẹp ở khoảng 1/3 ống nghiệm tính từ miệng ống.
B. Miệng ống nghiệm nghiêng về phía không có người.
C. Để đáy ống nghiệm sát vào bấc đèn cồn.
D. Làm nóng đều đáy ống nghiệm rồi mới đun trực tiếp tại nơi có hoá chất.
Câu 4: Quá trình nào sau đây là sự biến đổi vật lí?
A. Cho vôi sống CaO vào nước được vôi tôi.
B. Cồn để trong lọ không kín bị bay hơi.
C. Khí carbon dioxide làm đục nước vôi trong.
D. Nung đá vôi thành vôi sống.
Câu 5: Dấu hiệu nào giúp ta có khẳng định có phản ứng hoá học xảy ra?
A. Có chất kết tủa (chất không tan).
B. Có chất khí thoát ra (sủi bọt).
C. Có sự thay đổi màu sắc.
D. Một trong số các dấu hiệu trên.
Câu 6: Cho các quá trình biến đổi hóa học sau:
(1) Đốt cháy củi, than đá, than cốc.
(2) Phân hủy đá vôi ở nhiệt độ cao (900 oC - 1000 oC) thành vôi sống.
Phát biểu nào sau đây đúng?
A. (1) là phản ứng tỏa nhiệt; (2) là phản ứng thu nhiệt.
B. (1) là phản ứng thu nhiệt; (2) là phản ứng tỏa nhiệt.
C. Cả (1) và (2) đều là phản ứng tỏa nhiệt.
D. Cả (1) và (2) đều là phản ứng thu nhiệt.
Câu 7: Cho các chất sau: H2SO4, HCl, NaCl, CuSO4, NaOH, Mg(OH)2. Số chất thuộc loại axit là:
A. 1
B. 2
C. 3
D. 4
Câu 8: Hoà tan hết 3,6 g một kim loại hoá trị II bằng dung dịch H2SO4 loãng được 3,719 lít H2 (đktc). Kim loại là:
A. Zn .
B. Mg.
C. Fe.
D. Ca.
Câu 9: Điền vào chỗ trống: "Acid là những ... trong phân tử có nguyên tử ... liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion ..."
A. Đơn chất, hydrogen, OH−
B. Hợp chất, hydroxide, H+
C. Đơn chất, hydroxide, OH−
D. Hợp chất, hydrogen, H+
Câu 10: Ở một số khu vực, không khí bị ô nhiễm bởi các chất khí như SO2, NO2,... sinh ra trong sản xuất công nghiệp và đốt cháy nhiên liệu. Các khí này có thể hòa tan vào nước và gây ra hiện tượng:
A. Đất bị phèn, chua
B. Đất bị nhiễm mặn
C. Mưa acid
D. Nước bị nhiễm kiềm
Câu 11: Tìm phát biểu đúng:
A. Bazơ là hợp chất mà phân tử có chứa nguyên tử kim loại
B. Axit là hợp chất mà phân tử có chứa một hay nhiều nguyên tử H
C. Bazơ hay còn gọi là kiềm
D. Chỉ có bazơ tan mới gọi là kiềm
Câu 12: Trong cơ thể người, pH của máu luôn được duy trì ổn định trong phạm rất hẹp khoảng:
A. 7,25-7,35
B. 7,35-7,45
C. 7,45-7,55
D. 7,55-7,65
Câu 13: Khẳng định nào đúng về định nghĩa của oxide acid?
A. oxide acid thường tạo bởi một phi kim với nguyên tố oxygen.
B. oxide acid thường tạo bởi một kim loại với nguyên tố oxygen.
C. oxide acid thường tạo bởi một hợp chất với nguyên tố oxygen.
D. oxide acid khi tác dụng với nước tại ra dung dịch bazơ tương ứng.
Câu 14: Điền vào chỗ trống: "Oxide là hợp chất của ... với một nguyên tố khác."
A. Oxygen
B. Hydrogen
C. Nitrogen
D. Carbon
Câu 15: Oxide nào sau đây là nguyên nhân gây ra hiệu ứng nhà kính?
A. CO2
B. O2
C. N2
D. H2
Câu 16: Hợp chất nào sau đây bị nhiệt phân hủy tạo ra hợp chất oxit và một chất khí làm đục nước vôi trong?
A. Muối nitrat
B. Muối sunfat
C. Muối clorua
D. Muối cacbonat không tan
Câu 17: Cho 35 gam CaCO3 vào dung dịch HCl dư, kết thúc phản ứng thu được bao nhiêu lít khí CO2 ở đktc?
A. 7,84 lít
B. 6,72 lít
C. 5,56 lít
D. 4,90 lít
Câu 18: Nhóm muối tác dụng với dung dịch axit sunfuric loãng là
A. BaCl2, CaCO3
B. NaCl, Cu(NO3)2
C. Cu(NO3)2, Na2CO3
D. NaCl, BaCl2
Câu 19: Dãy phân bón hoá học chỉ chứa toàn phân bón hoá học đơn là:
A. KNO3, NH4NO3, (NH2)2CO
B. KCl, NH4H2PO4, Ca(H2PO4)2
C. (NH4)2SO4, KCl, Ca(H2PO4)2
D. (NH4)2SO4, KNO3, NH4Cl
Câu 20: Trong các loại phân bón hoá học sau loại nào là phân đạm?
A. Ca3(PO4)2
B. NH4NO3
C. KCl
D. K2SO4
Câu 21: Để phân biệt 2 loại phân bón hoá học là: NH4NO3 và NH4Cl. Ta dùng dung dịch:
A. KOH
B. Ca(OH)2
C. AgNO3
D. BaCl2
Câu 22: Trong các loại phân bón sau, loại phân bón nào có lượng đạm cao nhất ?
A. NH4NO3
B. NH4Cl
C. (NH4)2SO4
D. (NH2)2CO
Câu 23: Khối lượng của nguyên tố N có trong 100 gam (NH2)2CO là
A. 46,67 gam
B. 63,64 gam
C. 32,33 gam
D. 31,33 gam
Câu 24: Để nhận biết 2 loại phân bón hoá học là: NH4NO3 và NH4Cl. Ta dùng dung dịch:
A. KOH
B. Ca(OH)2
C. AgNO3
D. BaCl2
Phần II. Tự luận (4 điểm)
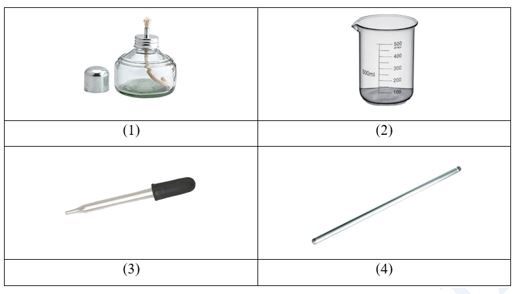
Bài 1: (2 điểm) Gọi tên các dụng cụ dưới đây:
Bài 2: (2 điểm) Từ muối CuSO4, nước cất và những dụng cụ cần thiết hãy tính toán và giới thiệu cách pha chế 50 ml dung dịch CuSO4 0,5M.
2. Đáp án
Phần I. Trắc nghiệm
|
1. B |
2. D |
3. C |
4. B |
5. D |
6. A |
7. B |
8. A |
|
9. C |
10. C |
11. D |
12.B |
13. A |
14. A |
15. A |
16. D |
|
17. A |
18. A |
19. B |
20. B |
21. C |
22. D |
23. A |
24. C |
Phần II. Tự luận
Bài 1:
(1) đèn cồn;
(2) cốc thuỷ tinh có chia vạch;
(3) ống hút nhỏ giọt;
(4) đũa thuỷ tinh.
Bài 2:
Bước 1: Tính toán
- Đổi 50 ml = 0,05 lít;
- Số mol chất tan là: nCuSO4= CM.V = 0,5.0,05 = 0,025 (mol).
- Khối lượng chất tan: mCuSO4= n.M = 0,025.160 = 4 (gam).
Bước 2: Pha chế:
- Cân lấy 4 gam CuSO4 khan cho vào cốc thủy tinh dung tích 100 ml.
- Đổ dần dần nước vào cốc thuỷ tinh và khuấy nhẹ cho đủ 50 ml dung dịch.
- Thu được 50 ml dung dịch CuSO4 có nồng độ 0,5M.
Trên đây toàn bộ nội dung tài liệu Đề thi giữa HK1 môn KHTN 8 KNTT năm học 2023-2024 Trường THCS Nguyễn Tri Phương. Để xem thêm nhiều tài liệu tham khảo hữu ích khác các em chọn chức năng xem online hoặc đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Mời các em tham khảo các tài liệu có liên quan:
- Đề thi giữa HK1 môn KHTN 8 CTST năm học 2023-2024 có đáp án Trường THCS Nguyễn Bỉnh Khiêm
- Đề thi giữa HK1 môn Công Nghệ 8 CTST năm 2023-2024 Trường THCS Bế Văn Đàn có đáp án
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.