Câu hỏi trắc nghiệm (32 câu):
-
Câu 1: Mã câu hỏi: 18111
Nguyên tử của nguyên tố R có cấu hình electron 1s22s22p3, công thức hợp chất khí với hiđro và công thức oxit cao nhất đều đúng ở cặp công thức nào sau đây?
- A. RH2, RO
- B. RH5, R2O3
- C. RH3, R2O5
- D. RH4, RO2
-
Câu 2: Mã câu hỏi: 18112
Mệnh đề nào dưới đây không đúng? Trong một chu kỳ theo chiều tăng dần của điện tích hạt nhân thì:
- A. Hóa trị trong hợp chất khí với Hidro giảm dần, tính kim loại giảm.
- B. Bán kính nguyên tử giảm dần, tính phi kim tăng dần.
- C. Hóa trị cao nhất với oxi tăng dần, độ âm điện tăng dần.
- D. Tính bazơ của hidroxit tăng dần, bán kính nguyên tử giảm dần.
-
Câu 3: Mã câu hỏi: 18116
Hòa tan hoàn toàn 8,37gam hai kim loại X, Y ở 2 chu kì liên tiếp và thuộc nhóm IA trong nước (dư), thu được 3,024 lít khí H2 (đktc). Hai kim loại X, Y là?
- A. Li, Na.
- B. K, Rb.
- C. Rb, Cs.
- D. Na, K.
-
Câu 4: Mã câu hỏi: 18117
Chỉ ra mệnh đề sai: Tính phi kim của nguyên tố càng mạnh thì
- A. Tính kim loại càng yếu.
- B. Khả năng thu electron càng lớn.
- C. Bán kính nguyên tử càng lớn.
- D. Độ âm điện càng lớn.
-
Câu 5: Mã câu hỏi: 18118
Hai nguyên tố X, Y thuộc cùng một nhóm A và hai chu kì liên tiếp có tổng điện tích hạt nhân là 22. Vị trí của X, Y trong bảng tuần hoàn là: (Biết ZX < ZY)
- A. X thuộc chu kỳ 3, nhóm IVA. Y thuộc chu kỳ 4, nhóm IVA
- B. X thuộc chu kỳ 3, nhóm VIA. Y thuộc chu kỳ 4, nhóm VIA
- C. X thuộc chu kỳ 2, nhóm IIIA. Y thuộc chu kỳ 3, nhóm IIIA
- D. X thuộc chu kỳ 2, nhóm VA. Y thuộc chu kỳ 3, nhóm VA
-
Câu 6: Mã câu hỏi: 18120
Hiđroxit nào có tính bazơ yếu nhất: (Cho 13Al, 19K, 11Na, 12Mg)
- A. Al(OH)3
- B. KOH
- C. NaOH
- D. Mg(OH)2
-
Câu 7: Mã câu hỏi: 18121
Đại lượng đặc trưng cho khả năng hút electron của nguyên tử các nguyên tố khi hình thành liên kết hoá học là:
- A. Tính phi kim.
- B. Điện tích hạt nhân.
- C. Độ âm điện.
- D. Tính kim loại.
-
Câu 8: Mã câu hỏi: 18122
X, Y là 2 nguyên tố liên tiếp nhau trong 1 nhóm A và có tổng số điện tích hạt nhân là 32 (ZX < ZY). Số hiệu nguyên tử của X, Y lần lượt là:
- A. 14; 18
- B. 7; 15
- C. 15; 17
- D. 12; 20
-
Câu 9: Mã câu hỏi: 18123
Một nguyên tố X thuộc chu kì 2, nhóm VIIA trong bảng tuần hoàn. Phát biểu nào sau đây không đúng?
- A. Phân lớp ngoài cùng của X có 5 electron.
- B. X có 2 lớp electron.
- C. X là nguyên tố có độ âm điện lớn nhất.
- D. Công thức oxit cao nhất của X là X2O7.
-
Câu 10: Mã câu hỏi: 18124
Nguyên tố X thuộc nhóm VIA. Nguyên tử của nó có tổng số hạt proton, nơtron, electron là 48. Cấu hình electron của nguyên tử X là:
- A. 1s22s22p63s23p4
- B. 1s22s22p63s23p63d54s1
- C. 1s22s22p4
- D. 1s22s22p6
-
Câu 11: Mã câu hỏi: 18125
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là ns2np4. Trong hợp chất khí của nguyên tố X với hiđrô, X chiếm 94,12% khối lượng. Phần trăm khối lượng của nguyên tố X trong oxit cao nhất là:
- A. 27,27%.
- B. 40,0%
- C. 60,0%.
- D. 50,0%.
-
Câu 12: Mã câu hỏi: 18126
Khi xếp các nguyên tố hoá học theo chiều tăng dần của điện tích hạt nhân. Tính chất nào sau đây không biến đổi tuần hoàn?
- A. Bán kính nguyên tử.
- B. Số khối.
- C. Số electron ngoài cùng.
- D. Độ âm điện.
-
Câu 13: Mã câu hỏi: 18127
Hai nguyên tố X, Y thuộc cùng một chu kì trong bảng tuần hoàn có tổng số điện tích hạt nhân = 51. Biết X thuộc nhóm IIA, Y thuộc nhóm IIIA và (ZX < ZY). Phát biểu nào sau đây đúng?
- A. Nguyên tử X có 25 proton
- B. Điện tích hạt nhân của X là 20.
- C. Nguyên tử Y có 26 electron.
- D. X và Y đều là nguyên tố s.
-
Câu 14: Mã câu hỏi: 18128
Một nguyên tố hóa học X ở chu kì III, nhóm VA. Cấu hình electron của nguyên tử X là:
- A. 1s22s22p63s23p3.
- B. 1s22s22p63s23p4.
- C. 1s22s22p63s23p5.
- D. 1s22s22p63s23p2.
-
Câu 15: Mã câu hỏi: 18132
Dãy các nguyên tố sắp xếp theo chiều tăng dần tính tính phi kim từ trái sang phải là:
- A. P, N, F, O
- B. P, N, O, F
- C. N, P, O, F
- D. N, P, F, O
-
Câu 16: Mã câu hỏi: 18134
Ion R+ có cấu hình electron phân lớp ngoài cùng là 3p6. Vị trí của R trong bảng tuần hoàn là:
- A. Chu kì 4, nhóm IA
- B. Chu kì 4, nhóm IIA
- C. Chu kì 3, nhóm VIIIA
- D. Chu kì 3, nhóm VIA
-
Câu 17: Mã câu hỏi: 18135
Trong một nhóm A(trừ nhóm VIIIA) theo chiều tăng của điện tích hạt nhân thì: (chọn mệnh đề đúng)
- A. Độ âm điện giảm, tính phi kim tăng.
- B. Tính kim loại tăng, bán kính nguyên tử giảm.
- C. Tính phi kim giảm, bán kính nguyên tử tăng.
- D. Tính kim loại tăng, độ âm điện tăng.
-
Câu 18: Mã câu hỏi: 18136
Nguyên nhân của sự biến đổi tuần hoàn tính chất của các nguyên tố là do sự biến đổi tuần hoàn của:
- A. Cấu hình electron lớp ngoài cùng của nguyên tử.
- B. Điện tích hạt nhân.
- C. Cấu trúc lớp vỏ electron của nguyên tử.
- D. Số hiệu nguyên tử.
-
Câu 19: Mã câu hỏi: 18138
Nhóm A bao gồm các nguyên tố:
- A. Nguyên tố s và nguyên tố p
- B. Nguyên tố p
- C. Nguyên tố d và nguyên tố f.
- D. Nguyên tố s
-
Câu 20: Mã câu hỏi: 18140
Một nguyên tố X thuôc chu kì 4, nhóm VA trong bảng tuần hoàn. Phát biểu đúng về X là:
- A. X có 3 electron ở lớp ngoài cùng.
- B. X là một kim loại.
- C. Nguyên tử của nguyên tố đó có 23 electron.
- D. X là phi kim
-
Câu 21: Mã câu hỏi: 18144
Nguyên tố X là phi kim có hoá trị cao nhất với oxi là x. Hoá trị trong hợp chất khí với hidro là y. Quan hệ giữa x và y là:
- A. x ≤ y.
- B. x = y.
- C. x + y = 8.
- D. x - y = 8.
-
Câu 22: Mã câu hỏi: 18145
Nguyên tử của nguyên tố X có electron ở mức năng lượng cao nhất là 3p. Y là nguyên tố nhóm A, có tổng số electron thuộc các phân lớp s bằng 7. Nguyên tử X và Y có số electron hơn kém nhau là 2. Hai nguyên tố X, Y lần lượt là:
- A. Phi kim và khí hiếm
- B. Khí hiếm và kim loại
- C. Kim loại và kim loại
- D. Phi kim và kim loại
-
Câu 23: Mã câu hỏi: 18150
Dãy nguyên tố nào có các số hiệu nguyên tử sau đây chỉ gồm các nguyên tố p?
- A. 7, 12, 15.
- B. 6, 13, 17.
- C. 16, 17, 19.
- D. 11, 14, 32.
-
Câu 24: Mã câu hỏi: 18155
Hai nguyên tử X, Y có phân lớp electron ngoài cùng lần lượt là 2sx và 3py. Tổng số electron của hai phân lớp này là 7 và hiệu số electron của chúng là 3. Số điện tích hạt nhân của A, B lần lượt là:
- A. 5 và 10
- B. 4 và 17
- C. 6 và 11
- D. 17 và 4
-
Câu 25: Mã câu hỏi: 18157
Một nguyên tố X thuôc chu kì 3, nhóm VIA trong bảng tuần hoàn. Phát biểu sai về nguyên tố X là:
- A. Nguyên tử X có 16 proton.
- B. X là nguyên tố phi kim.
- C. X có 4 electron ở lớp ngoài cùng.
- D. X là nguyên tố p.
-
Câu 26: Mã câu hỏi: 18166
Cho 27,4 gam kim loại R hóa trị 2 tác dụng hết với nước thu được 200 gam dung dịch X có nồng độ 17,1% và khí H2 bay ra. Kim loại R là:
- A. Na.
- B. Mg.
- C. Ca.
- D. Ba.
-
Câu 27: Mã câu hỏi: 18167
Nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 3s23p4. Vị trí của Y trong bảng tuần hoàn là:
- A. Chu kỳ 4, nhóm IIIA
- B. Chu kỳ 3, nhóm VIA
- C. Chu kỳ 3, nhóm IVA
- D. Chu kỳ 3, nhóm VIB
-
Câu 28: Mã câu hỏi: 18168
Oxit cao nhất của một nguyên tố có công thức XO2. Hợp chất khí của X với hiđro có chứa 75% X về khối lượng. Tên của X là
- A. Photpho.
- B. Nitơ.
- C. Cacbon.
- D. Silic.
-
Câu 29: Mã câu hỏi: 18169
Cho các nguyên tố: Tính kim loại của các nguyên tố tăng dần theo thứ tự nào sau:
- A. T < Y < R < X
- B. R < X < Y < T
- C. X < R < T < Y
- D. X < T < Y < R
-
Câu 30: Mã câu hỏi: 18170
Số hiệu nguyên tử của các nguyên tố X, Y, Z, T lần lượt là 6, 7, 21, 20. Nhận xét nào sau đây sai?
- A. Z và T thuộc nhóm IIA
- B. X thuộc nhóm IVA.
- C. Y thuộc nhóm VA.
- D. Z, T thuộc chu kỳ 4.
-
Câu 31: Mã câu hỏi: 18171
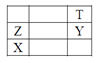
Xét vị trí tương đối trong bảng tuần hoàn của các nguyên tố X, Y, Z, T.
Tính phi kim tăng theo thứ tự nào sau đây?
- A. X < Z < Y < T.
- B. Y < Z < X < T.
- C. Z < X < Y < T.
- D. T < Y < Z < X.
-
Câu 32: Mã câu hỏi: 18172
Bán kính nguyên tử các nguyên tố 3Li, 8O, 9F, 11Na được xếp theo thứ tự tăng dần từ trái sang phải là:
- A. Li, Na, O, F
- B. F, O, Li. Na
- C. F, Li, O, Na
- D. F, Na, O, Li